Лимфома — это злокачественное заболевание, поражающее лимфатическую систему. Если точнее, то речь идет о группе заболеваний, потому что их несколько — и они отличаются разными особенностями.
Сама лимфатическая система — это сложная система, сосуды которой охватывают все внутренние органы. В нее также входят лимфоузлы, которые формируют лимфоциты, очень важные для нашего иммунитета. У этой системы несколько ключевых функций. Барьерная очищает лимфу и задерживает нежелательные для организма частицы (например, погибшие клетки). Транспортная функция доставляет питательные вещества к органам, а иммунная помогает бороться с вирусами, бактериями, любыми вредными клетками.
Если развивается лимфома, лимфатические клетки начинают делиться бесконтрольно, появляются опухоли, которые без своевременного лечения грозят пациенту в том числе и летальным исходом.
Что такое лимфома?
Лимфома – это поражение иммунной системы и внутренних органов, в которых скапливаются измененные клетки, нарушающие работу тканей.
Опухоль развивается в лимфатической системе, которая помогает нам бороться с инфекциями и другими заболеваниями. Циркулирующая в ней лимфа омывает все клетки организма и доставляет в них необходимые вещества, забирая отходы. В расположенных по всей ее сети лимфатических узлах опасные вещества обезвреживаются и выводятся из организма. Лимфосистема дополняет кровеносную и помогает жидкостям перемещаться по телу. В отличие от крови, скорость движения которой задает «насос» – сердце, лимфа медленно циркулирует самостоятельно.
Лечение зрелых Т- и В-клеточных лимфом
Для терапии зрелоклеточных лимфом применяется жесткое, но непродолжительное лечение (до полугода) с использованием высокодозной полихимиотерапии и иммунотерапии (рис. 2).
Лечение проводится короткими интенсивными курсами — от 2 до 6. Их количество зависит от стадии болезни и группы риска ребенка. Для определения группы риска учитываются такие параметры, как радикальность операции (если она была), размеры и локализация опухоли, уровень ЛДГ в крови и поражение костного мозга и центральной нервной системы.
Для терапии зрелых В-клеточных лимфом, клетки которых экспрессируют CD20-антиген, используется таргетный препарат ритуксимаб (мабтера, ацеллбия).
Рис. 2. Протокол NHL-BFM для лечения зрелых В-клеточных лимфом
Как развивается лимфома?
Онкология начинается с появления в организме всего лишь одной измененной клетки иммунной системы. Всего выделяют 2 основных их типа:
- В-лимфоциты
: вырабатывают антитела – белки, защищающие организм от бактерий и вирусов. Именно в них образуется большинство лимфом. - Т-лимфоциты
, одна часть которых уничтожает микробы и неправильные клетки, а вторая – помогает повысить или замедлить активность иммунитета.
Почти все ненормальные клетки выявляются и уничтожаются нашим иммунитетом, но некоторым из них удается выжить. Они постепенно размножаются, распространяются по всему телу, создают опухоли, скапливаются во внутренних органах и нарушают их работу.
Заболевание может возникать в любой области, где находится лимфатическая ткань, основными участками которой являются:
- Лимфатические узлы
– небольшие органы размером с горошину, представляющие из себя скопления клеток иммунной системы, в том числе лимфоцитов. В организме человека их более 500. - Селезенка
, расположенная под нижними ребрами на левой стороне тела. Она производит лимфоциты, хранит здоровые клетки крови и отфильтровывает поврежденные, а также разрушает микробов и чужеродные вещества. - Костный мозг –
губчатая ткань внутри определенных костей. Здесь образуются новые клетки крови, в том числе часть лимфоцитов. - Тимус, или вилочковая железа –
небольшой орган, расположенный за верхней частью грудины перед сердцем. В нем происходит созревание и развитие некоторых лимфоцитов. - Миндалины, или гланды –
скопления лимфатической ткани в задней части глотки. Эти органы помогают вырабатывать антитела – белки, не позволяющие размножаться вдыхаемым или проглатываемым микроорганизмам. - Пищеварительный тракт:
желудок, кишечник и многие другие органы также содержат лимфатическую ткань.
Течение заболевания во время беременности
Лимфосаркома может сочетаться с беременностью. Возможны следующие варианты:
- Зачатие наступило в состоянии ремиссии.
- Опухоль была выявлена во время внутриутробного развития плода.
- Развился рецидив новообразования в период беременности.
Беременность и роды в период стойкой ремиссии не отягощают прогноза опухоли. Однако риск рецидивирования лимфосаркомы гораздо выше для тех пациенток, у которых зачатие происходит в течение первых 2-3 лет после полной стабилизации состояния. В связи с этим женщины должны быть предупреждены о необходимости применения контрацептивов в течение этого периода.
Лимфосаркома высокого риска, которая была диагностирована в первом триместре, служит показанием к прерыванию беременности. При обнаружении опухоли во втором и третьем триместре тактика ведения подбирается индивидуально, с привлечением таких специалистов, как онколог, неонатолог, терапевт, генетик. Учитывается степень распространенности заболевания и характер ответа на лечение.
При рецидиве опухоли прогноз для беременности самый неблагоприятный. В данной ситуации требуется применение высокотоксичных препаратов, прием которых несовместим с беременностью.
Лимфома – это рак?
Раком официальная медицина России и некоторых других стран называет злокачественные опухоли – опасные для жизни новообразования, которые развиваются в эпителиальных клетках, содержащихся в коже или слизистых оболочках, и выстилающих внутреннюю поверхность органов.
Лимфома – это не рак, а онкологическое заболевание. Она образуется из лимфоцитов, а ее клетки также умеют бесконтрольно делиться, накапливаться в тканях, нарушая их работу, и создавать дополнительные очаги заболевания в различных частях тела.
Лечение лимфобластных лимфом из Т- и В-предшественников
Лечение детей с лимфобластной лимфомой — длительное, непрерывное в течение 2 лет. Оно состоит из нескольких следующих друг за другом фаз: профаза, индукция – протокол I, консолидация – протокол М, реиндукция – протокол II, профилактика поражения центральной нервной системы. Рис. 3.
Для профилактики поражения ЦНС используются введение химиопрепаратов в спинномозговой канал и лучевая терапия. Поддерживающая терапия проводится в течение 1,5 лет.
Интенсивность программы лечения зависит от стадии заболевания.
Рис. 3. Протокол NHL-BFM для лечения лимфобластных лимфом из Т- и В-предшественников
Типы лимфом
Врачи выделяют 2 их основных класса:
- Лимфома Ходжкина, или лимфогранулематоз
: чаще всего начинается в лимфатических узлах верхней части тела – на груди, шее или в подмышках. Как правило, она распространяется в различные лимфоузлы по лимфатическим сосудам, но в редких случаях на поздних стадиях проникает в кровоток и распространяется на другие части тела, такие как печень, легкие или костный мозг. Данный диагноз ставится при выявлении в организме особых клеток – Березовского-Рид-Штернберга, которые представляют из себя измененные В-лимфоциты.
- К неходжкинским лимфомам
относят все остальные типы заболевания – их насчитывается около 30. У каждого из них есть свои, особые признаки: расположение первичной опухоли, строение и скорость развития.
Профилактика
Лимфому, при которой у взрослых могут возникать симптомы по разным причинам, можно предотвратить, если соблюдать некоторые рекомендации. Профилактика поможет свести к нулю риск поражения организма.
С этой целью необходимо:
- меньше контактировать с токсичными веществами;
- не пренебрегать контрацептивами во время полового акта со случайным партнером;
- не меньше 2-х раз в год проходит курс витаминной терапии;
- соблюдать гигиену (не использовать чужих зубных щеток, полотенец);
- регулярно заниматься спортом (умеренно, хотя бы 10-15 мин. будет вполне достаточно).
Причины развития лимфом
Врачам и ученым точно не известно, почему именно в организме человека начинает развиваться заболевание. Они знают лишь о факторах, которые повышают вероятность образования каждого из типов онкологии.
Для лимфом Ходжкина
они выглядят следующим образом:
- Вирус Эпштейна – Барр
, вызывающий инфекционный мононуклеоз – поражение лимфоидной ткани, включая аденоиды, печень, селезенку и лимфатические узлы. У части пациентов части вируса обнаруживаются в клетках Березовского-Рид-Штернберга, но у большинства больных его признаков нет. - Возраст
: диагноз может быть поставлен в любом возрасте, но чаще всего он встречается у 20-летних и людей старше 55. - Пол
: среди мужчин заболевание более распространено, чем среди женщин. - Наследственность и семейный анамнез
: риск повышен для братьев и сестер, а также для однояйцевых близнецовОднояйцевые близнецы развиваются из одной яйцеклетки, оплодотворенной одним сперматозоидом. Они бывают только одного пола, имеют одинаковые гены и крайне похожи внешне. обладателей лимфомы Ходжкина. Причина этого точно не известна – возможно, все дело в том, что члены одной семьи в детстве переносят одни инфекции, либо имеют общие унаследованные генные изменения, увеличивающие вероятность развития данного типа онкологии. - Ослабленная иммунная система
. Шансы получить данный диагноз возрастают у людей с ВИЧ инфекцией и нарушениями работы иммунитета, развивающимися в том числе из-за приема подавляющих его препаратов, что нередко требуется после пересадки органов.
Список таких факторов для неходжкинских лимфом
выглядит иначе:
- К ним относят воздействие радиации
, включая ее дозы, полученные в ходе лучевой терапии, проводимой для лечения других типов онкологии. - Различные вещества
, включая гербициды и инсектициды, убивающие сорняки и насекомых, а также химиотерапевтические препараты. - Возраст
: как правило, чем старше человек, тем выше его риски – в большинстве случаев заболевание встречается в возрасте 60+, но некоторые его виды возникают и у молодых людей. - Сбои в работе иммунной системы
– влияют на шансы возникновения всех видом лимфом. - Некоторые вирусы
могут влиять на ДНК лимфоцитов, в которой зашифрована вся информация о нашем теле, и преобразовывать их в онкологические клетки. - Инфекции, постоянно стимулирующие иммунитет, и вынуждающие нашу естественную защиту работать в усиленном режиме, также повышают риск получения тяжелого диагноза.
- Наличие близких кровных родственников – родителей, детей, братьев или сестер с данным диагнозом также увеличивает вероятность развития заболевания.
- Некоторые исследования показали, что грудные имплантаты, особенно с шероховатой поверхностью, могут спровоцировать возникновение анапластической крупноклеточной лимфомы. Она развивается на коже, в лимфоузлах или рубцовых тканях, образовавшихся в месте разреза.
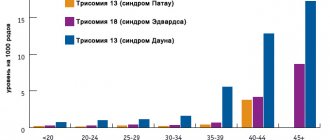
Частота возникновения неходжкинских лимфом (нхл)
Более 90% НХЛ диагностируется у взрослых больных. Чаще всего НХЛ возникают в возрасте 60-70 лет. Риск возникновения этой опухоли увеличивается с возрастом.
Персональный риск возникновения НХЛ в течение всей жизни составляет приблизительно 1 к 50.
С начала 70-х годов отмечено почти двукратное увеличение частоты НХЛ. Это явление трудно объяснить. В основном это связывают с инфекцией, вызванной вирусом иммунодефицита человека. Частично такое увеличение можно связать с улучшением диагностики.
С конца 90-х годов наблюдается стабилизация частоты возникновения НХЛ.
НХЛ чаще выявляются у мужчин по сравнению с женщинами.
В 2002 году в России было выявлено 5532 случая НХЛ у взрослых больных.
В США в 2004 году по предварительным данным ожидается 53370 случаев НХЛ у взрослых и детей.
Симптомы и признаки лимфомы
Как правило, на ранних этапах данный тип онкологии никак себя не проявляет, а ее обладатель хорошо себя чувствует и не подозревает о болезни – почти все ее симптомы появляются позже, на запущенных стадиях.
Один из наиболее частых признаков – появление припухлости на шее, в подмышках, паху или над ключицей
, которая представляет из себя увеличенный лимфатический узел. Обычно такое новообразование не болит, но со временем нередко увеличивается, а рядом с ним или в других областях тела появляются новые шишки.
Лимфомы, которые начинают развиваться или разрастаются в брюшной полости, способны вызвать отек
или
боль в животе, тошноту
и
рвоту
. Такие ощущения возникают из-за укрупнения лимфоузлов или внутренних органов, таких как селезенка или печень, либо скопления большого количества жидкости.
Изменившаяся в размерах селезенка может давить на желудок, вызывая потерю аппетита
и
чувство сытости после небольшого количества пищи
.
Увеличившиеся тимусТимус, или вилочковая железа –
небольшой орган, расположенный за верхней частью грудины перед сердцем. В нем происходит созревание и развитие некоторых лимфоцитов. или лимфоузлы грудной клетки могут оказывать давление на трахею, по которой воздух проходит в легкие. Это приводит к появлению
кашля
,
затруднению дыхания, болевым ощущениям
или
тяжести в груди
.
Поражения головного мозга способны вызывать головную боль, слабость, изменение личности, проблемы с мышлением
и
судороги
.
Другие типы заболевания могут распространяться на окружающие головной и спинной мозг ткани, из-за чего у пациента двоится в глазах, немеет лицо
и
ухудшается речь
.
Лимфомы кожи часто проявляются в виде зудящих красных бугорков
или
шишек
.
Кроме того, симптомами могут быть:
- потеря веса;
- озноб;
- ночная потливость;
- повышенная температура;
- сильная усталость;
- вздутие живота;
- частые или тяжело протекающие инфекции;
- легко появляющиеся синяки или кровотечения.
Когда необходимо обратиться к врачу
Конечно, при возникновении усталости и некоторых других симптомов по отдельности не стоит сразу списывать это на появление онкологии. Необходимо сдать анализы для того, чтобы понять причину недомогания.
Перед сдачей анализов нужно подготовиться. Человек за сутки до всех процедур исключает алкоголь и табак. Желудок должен быть пустым. Время последнего приема пищи – не менее 12 ч. Запрещено пить чай, соки (натуральные и покупные), разжевывать жевательную резинку. Допускается только употребление воды.
Еще одно важное условие – перед процедурами нельзя волноваться. Иногда предотвратить абсолютно все факторы, провоцирующие стресс, сложно. Самой частой причиной беспокойства является ожидание плохого результата анализов.
Если человек принимает какие-либо препараты, об этом следует сообщить врачу.
Если диагноз все же подтвердился, то следующий, к кому направляется пациент – это врач-онколог. После осмотра назначается терапия, диета и прогнозы на выздоровление.
Диагностика лимфомы
Большинство пациентов обращаются к врачу из-за наличия определенных признаков заболевания или плохого самочувствия. Специалисты начинают обследование с осмотра и опроса – о семейных диагнозах, возможных факторах риска и других проблемах со здоровьем. Затем изучают лимфатические узлы и другие части тела, в которых содержится лимфатическая ткань, включая селезенку и печень. После чего назначают целый ряд исследований:
- Анализы крови
: позволяют измерять уровни различных клеток в крови, обнаруживать повреждения костного мозга, оценивать работу почек и печени, а также выявлять инфекции и другие нарушения. - Биопсия
– забор частички подозрительной ткани и передача ее для исследования в лабораторию. В зависимости от течения заболевания, докторам может понадобиться биопсия лимфатических узлов, костного мозга, спинномозговойСпинномозговая жидкость омывает и защищает головной и спинной мозг., а также плевральной – содержащейся в грудной клетке, или перитонеальной – находящейся в животе жидкости. - Компьютерная томография, КТ
– позволяет выявлять очаги заболевания в брюшной полости, тазу, груди, голове и шее. - Магнитно
—
резонансная томография, МРТ
– создает подробное изображение мягких тканей. Метод обычно используется для исследования спинного или головного мозга. - Рентгенограмма
– помогает обнаруживать увеличенные лимфатические узлы в области грудной клетки или в костях. - Ультразвук, УЗИ
– используется для изучения увеличенных лимфоузлов или различных органов, таких как печень, селезенка или почки. - Позитронно
—
эмиссионная томография, ПЭТ
– позволяет выявлять лимфомы в увеличенных лимфоузлах, даже в тех, которые выглядят нормальными на КТ. Кроме того, с ее помощью можно определить, поддается ли заболевание лечению.
В онкологическом проводится полная диагностика лимфомы – быстро, без очередей и потерь драгоценного времени, на самом современном оборудовании. Наши специалисты ведут пациента «от» и «до» – от обследования до проведения любого лечения.
Первичная эпидермотропная Т-клеточная лимфома кожи
Первичная эпидермотропная Т-клеточная лимфома кожи (грибовидный микоз) является самой частой формой первичной лимфомы кожи, обусловленной пролиферацией лимфоидных Т-клеток малых и средних размеров с наличием церебриформных ядер и сопровождающейся поэтапной эволюцией пятен и папул (бляшек) в узлы. Чаще всего встречается у лиц в возрасте 50–60 лет; мужчины заболевают в два раза чаще женщин. В настоящее время общепринята клональная теория развития первичной эпидермотропной Т-клеточной лимфомы. Онкогенные мутации и появление клона злокачественных лимфоцитов этиологически связаны чаще всего с ретровирусами. В пользу этого свидетельствуют положительные результаты выделения Т-лимфотропного вируса человека I типа (HTLV-1) у больных грибовидным микозом и синдромом Сезари, а также детекция у таких больных антител к этому вирусу. Характерной чертой транскрипции эндогенных ретровирусов человека (HERV) является индивидуальная их изменчивость и избыточная экспрессия при опухолевых заболеваниях. Вместе с тем развитие первичной эпидермотропной Т-клеточной лимфомы может происходить под действием и других причин: вредностей промышленного производства, особенно химического и строительного; вредностей сельского хозяйства, лекарственных средств (антигистаминных, гипотензивных, антидепрессивных, дегтя и др.); ионизирующей радиации; инсоляции; ультрафиолетового облучения. Предрасполагающим фоном для развития первичной эпидермотропной Т-клеточной лимфомы могут служить хронические дерматозы — атопический дерматит, хронический атрофический акродерматит, псориаз и др. Однако при воздействии разнообразных мутагенных факторов возникновение клона злокачественных лимфоцитов и, следовательно, возникновение первичной эпидермотропной Т-клеточной лимфомы кожи детерминировано, в конечном счете, на генетическом уровне. Типичным патогенетическим механизмом этого заболевания является хромосомная нестабильность. Нозологические разновидности первичной эпидермотропной Т-клеточной лимфомы, особенности их клинических проявлений зависят главным образом от опухолевой прогрессии заболевания. Опухолевая прогрессия — основная составляющая патогенеза лимфом кожи. Она в свою очередь определяется степенью их дифференцировки и патологией митозов [1–5].
Классическая первичная эпидермотропная Т-клеточная лимфома кожи (ТКЛК) отличается гетерогенностью клинических подтипов и вариантов заболевания [2].
Буллезная первичная эпидермотропная ТКЛК встречается у людей пожилого возраста и характеризуется отдельными или генерализованными пузырями (субкорнеальными, интраэпидермальными, субэпидермальными), расположенными на нормальной либо гиперемированной коже туловища и/или конечностей. При нем иногда отмечаются акантоз и положительный симптом Никольского, но только без характерных для пузырчатки иммунофлюоресцентных феноменов. Появление буллезных элементов считается плохим прогностическим признаком: в течение года почти у 50% больных заболевание заканчивается летально.
Гиперпигментированная первичная эпидермотропная ТКЛК чаще наблюдается у лиц молодого возраста со смуглой кожей и проявляется бессимптомными или зудящими не шелушащимися пятнами с нечеткими границами, бляшками или узлами. Дифференциальный диагноз проводится с отрубевидным лишаем, белым лишаем, витилиго, лепрой, саркоидозом, поствоспалительной гипопигментацией. Опухолевые клетки часто имеют фенотип CD8+.
Пойкилодермическая первичная эпидермотропная ТКЛК характеризуется наличием наряду с типичными проявлениями первичной эпидермотропной Т-клеточной лимфомы участков атрофической сосудистой пойкилодермии, представленных гипер- и гипопигментацией, сухостью, атрофией кожи, телеангиэктазиями. Пойкилодермия часто развивается на месте предшествующих пятен в местах длительного трения кожи одеждой и может иметь ограниченный или распространенный характер. Дифференциальный диагноз проводится с гиперпигментированным типом первичной эпидермотропной ТКЛК.
Пигментированная пурпуроподобная первичная эпидермотропная ТКЛК характеризуется диффузной пятнистой гиперпигментацией, не связанной с «атрофической сосудистой пойкилодермией» и регрессом предшествующих элементов. Фенотип большинства опухолевых клеток представлен CD4+; CD8+ имеют реактивный характер. В ряде случаев отмечается перестройка генов клонального Т-клеточного рецептора (TCR). Эпидермальные изменения различны, однако спонгиоза и некроза кератиноцитов не отмечается. Следовательно, отличить этот тип первичной эпидермотропной Т-клеточной лимфомы от доброкачественной пигментной пурпуры можно лишь на основании тщательного динамического наблюдения.
Первичная эпидермотропная Т-клеточная лимфома «без элементов» характеризуется наличием одного очага поражения, захватывающего менее 5% поверхности кожи. Обычно поражаются те же участки кожи, что и при классическом варианте первичной эпидермотропной Т-клеточной лимфомы (грудь, подмышечные впадины, ягодицы).
Первичная эпидермотропная Т-клеточная лимфома ладоней и подошв наблюдается в 11,5% случаев заболевания, проявляется специфическими изменениями в виде кольцевидных гиперпигментных пятен, бляшек, гиперкератоза, пузырьковых, пустулезных, дисгидротических элементов, веррукозных образований, псориазиформных бляшек, изъязвлений, а также дистрофии ногтей. Высыпания ограничены ладонями, подошвами или могут распространяться на всю стопу, кисть и пальцы. Если эти высыпания не сочетаются с типичными проявлениями первичной эпидермотропной Т-клеточной лимфомы на других участках кожи, клинический диагноз сложен и устанавливается гистологически или путем обнаружения клональной перестройки генов TCR. Дифференциальный диагноз проводится с грибковыми инфекциями, дисгидротической экземой, контактным дерматитом, псориазом ладоней и подошв, бородавками, гипертрофической формой красного плоского лишая, кольцевидной гранулемой. Течение этой разновидности первичной эпидермотропной Т-клеточной лимфомы обычно вялое. Чаще всего поражения кожи не распространяются за пределы первоначальных участков, однако даже при распространении высыпаний на конечности и туловище экстракутанные поражения не описаны.
Гиперкератотическая/веррукозная первичная эпидермотропная Т-клеточная лимфома проявляется гиперкератотическими и веррукозными бляшками, нередко на фоне проявлений классического варианта первичной эпидермотропной Т-клеточной лимфомы. Высыпания напоминают проявления черного акантоза или себорейного кератоза и чаще располагаются на сгибательных поверхностях (подмышечные впадины, паховые области), шее, соске и ареоле соска молочной железы.
Ихтиозиформная первичная эпидермотропная Т-клеточная лимфома — редкая разновидность, встречается в 1,8% случаев заболевания. Клинически заболевание проявляется широко распространенными ихтиозиформными элементами, часто сочетающимися с комедоноподобными образованиями и/или фолликулярными кератотическими папулами. Ихтиозиформные элементы обычно располагаются на конечностях, хотя могут поражать всю поверхность тела и сопровождаются зудом и экскориациями.
Пустулезная первичная эпидермотропная ТКЛК проявляется пустулами, расположенными в области ладоней и подошв. Кроме того, первичная эпидермотропная Т-клеточная лимфома может проявляться высыпаниями, напоминающими хронический лихеноидный кератоз, лихеноидный парапсориаз или периоральный дерматит. В очень редких случаях первичная эпидермотропная Т-клеточная лимфома имеет экстракутанную локализацию, поражая слизистую оболочку рта и язык, конъюнктиву глаз, молочную железу (при крупноклеточной трансформации с распространением на внутренние органы можно говорить об экстракутанном варианте первичной эпидермотропной ТКЛК). Прогноз при экстракутанном варианте первичной эпидермотропной Т-клеточной лимфомы плохой. Например, при первичной эпидермотропной Т-клеточной лимфоме языка (частота которого в структуре заболевания не превышает 1%) летальный исход отмечается в сроки до 3 лет после поражения полости рта. В запущенных стадиях первичной эпидермотропной Т-клеточной лимфомы экстракутанное распространение происходит наряду с поражением внутренних органов.
Основной рабочей классификацией для первичных лимфом кожи является классификация Всемирной Организации Здравоохранения (ВОЗ) и Европейской организации по исследованию и лечению рака (European Organization for Research and Treatment of Cancer, EORTC). В классификации ВОЗ/EORTC особо выделяют следующие варианты первичной эпидермотропной ТКЛК [2, 6].
Фолликулотропный — редкий вариант первичной эпидермотропной ТКЛК, встречается главным образом у взрослых. Клинически фолликулотропный вариант первичной эпидермотропной Т-клеточной лимфомы проявляется интенсивно зудящими сгруппированными фолликулярными или акнеформными папулами, уплотненными бляшками (в первую очередь, в области бровей), узлами (чаще на голове и шее), иногда алопецией (волосистая часть головы, брови). Фенотипически характеризуется CD4+. Методом ПЦР выявляется клональная перестройка генов, кодирующих b- или γ-цепь TCR. Дифференциальный диагноз проводится с себорейным и атопическим дерматитом. Прогноз в связи с трансформацией в крупноклеточную лимфому хуже, чем при классической форме первичной эпидермотропной Т-клеточной лимфомы.
Педжетоидный ретикулез — вариант первичной эпидермотропной ТКЛК. Классическая клиническая разновидность педжетоидного ретикулеза с ограниченными проявлениями (тип Ворингера–Колоппа (Woringer–Kolopp)) характеризуется развитием четко отграниченных, слегка инфильтрированных бляшек округлой, овальной или неправильной формы, цвет которых варьирует от красного до красно-коричневого или красно-фиолетового. Бляшки локализуются на коже дистальных отделов конечностей. Поверхность их гладкая, блестящая с незначительным шелушением на отдельных участках, иногда местами гиперкератотическая, бородавчатая. Поражения отличаются медленным периферическим ростом с одновременным разрешением в центре и формированием атрофии и гиперпигментации. Края образованных таким образом очагов имеют кольцевидную или дугообразную конфигурацию, могут возвышаться над уровнем кожи, но, в отличие от базалиомы, не имеют возвышенного валика. Иногда на поверхности бляшки имеется сеточка, напоминающая сетку Уэкхема. Мужчины регистрируются в два раза чаще женщин. При разновидности Ворингера–Колоппа не поражаются внутренние органы. Заболевание протекает с поражением внутренних органов и часто приводит к летальному исходу. Диссеминированная разновидность (тип Кетрона–Гудмана (Kettron–Goodman)), ранее также относившаяся к педжетоидному ретикулезу, в настоящее время классифицируется в зависимости от фенотипа как агрессивная эпидермотропная CD8+ лимфома или γ/8+ Т-клеточная лимфома. Фенотип опухолевых клеток — CD3+, CD4+, CD5+, CD8–, описаны случаи с CD8+ фенотипом. Опухолевые клетки также могут экспрессировать CD30. Молекулярно-генетическое исследование демонстрирует клональную перестройку генов β- или γ-цепей TCR. Дифференциальный диагноз локализованной формы педжетоидного ретикулеза проводится с болезнью Боуэна, псориазом, экстрамаммарной болезнью Педжета. Диссеминированный педжетоидный ретикулез клинически сходен с классической первичной эпидермотропной Т-клеточной лимфомой кожи; дифференциация проводится на основании клинико-морфологических данных. Течение длительное с медленным развитием очагов поражения, иногда с их спонтанным регрессом. Следовательно, прогноз для жизни при локализованном варианте относительно благоприятный, хотя возможна диссеминация даже после многолетнего, относительно спокойного течения локализованного процесса. В случае диссеминации патологического процесса возможно поражение внутренних органов и летальный исход.
Синдром гранулематозной «вялой» кожи — чрезвычайно редкий вариант первичной эпидермотропной ТКЛК, чаще поражает лиц мужского пола. Клинически характеризуется наличием в крупных складках складчатых, инфильтрированных и лишенных эластичности образований. Иммунофенотип опухолевых клеток при ограниченной форме идентичен таковому при классической первичной эпидермотропной ТКЛК. В редких случаях опухолевые клетки экспрессируют СDЗ0-антиген. Гигантские клетки экспрессируют гистиоцитарные маркеры CD68 и CD163. При молекулярно-биологическом исследовании выявляется перестройка генов TCR. Клиническое течение в большинстве случаев вялое.
Синдром Сезари — форма ТКЛК, при которой практически сразу происходит лейкемизация. Первым проявлением заболевания является эксфолиативная эритродермия с лимфаденопатией и лишь иногда пятна, бляшки или опухоли. Диагноз подтверждается при наличии в периферической крови более 5% атипичных лимфоцитов (клеток Сезари). По иммунофенотипу и генотипу идентичен первичной эпидермотропной Т-клеточной лимфоме. Перестройка генов Т-клеточных рецепторов обнаруживается в опухолевых Т-клетках периферической крови и лимфатических узлах. Трансформация в более агрессивную крупноклеточную лимфому может происходить как в коже, клинически проявляясь изъязвленными узлами, так и в лимфатических узлах даже после разрешения эритродермии [2].
Международная классификация первичной эпидермотропной ТКЛК по TNM и стадиям включает следующие стадии [7]:
- IА стадия — Т1 (пятна, папулы или бляшки, занимающие < 10% поверхности тела), N0 (периферические лимфатические узлы не увеличены, при их гистологическом исследовании данных за ТКЛК нет), М0 (внутренние органы не поражены);
- IB стадия — Т2 (пятна, папулы или бляшки, занимающие > 10% поверхности тела), N0, M0;
- IIA стадия — Т1–2, N1 (периферические лимфатические узлы увеличены, при их гистологическом исследовании данных за ТКЛК нет), М0;
- IIB стадия — Т3 (одно или более опухолевидное образование на коже), N0–1, M0;
- III стадия — Т4 (эритродермия), N0–1, M0;
- IVA стадия — Т1–4, N2 (лимфатические узлы не увеличены, при их гистологическом исследовании имеются данные за ТКЛК) или N3 (лимфатические узлы увеличены, при их гистологическом исследовании имеются данные за ТКЛК), М0;
- IVB стадия — Т1–4, N0–3, М1 (внутренние органы поражены, при их гистологическом исследовании имеются данные за ТКЛК).
При классической форме клинически выделяют три стадии первичной эпидермотропной ТКЛК. Стадирование должно включать тщательное физикальное обследование, клинический анализ крови с подсчетом формулы, развернутый биохимический анализ, применение лучевых методов, а также биопсию и пункцию костного мозга при необходимости.
Стадия I (эритематозная) проявляется единичными или множественными красными пятнами, подверженными шелушению отрубевидными, мелко- и крупнопластинчатыми чешуйками. Интенсивность шелушения весьма различна: от слабого до псориазиформного. В последнем случае возникает сходство с псориазом. На фоне пятен, особенно крупных, иногда сохраняются островки здоровой кожи, что имеет определенное диагностическое значение. В пятнах может развиваться отечность с возможным формированием на их поверхности пузырьков. Пузырьки, вскрываясь, образуют эрозии, а подсыхая — корки. В результате эритематозные пятна приобретают экземаподобный вид. В начале заболевания пятна немногочисленны, со временем их число увеличивается, и они распространяются по кожному покрову с преимущественной локализацией на ягодицах, туловище и лице. Нередко генерализованные пятна, сливаясь между собой, поражают весь или почти весь кожный покров (рис. 1). Высыпания первичной эпидермотропной ТКЛК в I стадии, особенно на ранних этапах, склонны к спонтанному регрессу с последующими рецидивами, причем рецидивы у одного и того же больного клинически могут имитировать разные дерматозы. Такой клинический симптомокомплекс свидетельствует о реактивной (дермотропной) природе поражения лимфатических узлов. Продолжительность эритематозной стадии различна: от нескольких месяцев до десятков лет, обычно 4–5 лет. Возможны ремиссии, порой весьма длительные [1, 8].
Стадия II (бляшечная) развивается с переходом эритематозной стадии в бляшечную незаметно и обычно продолжительно. Бляшки возникают либо в результате инфильтрации эритематозных пятен, либо на видимо здоровой коже, легко отграничены, имеют округлые или чаще неправильные очертания, плоскую или выпуклую форму и темно-красную, буроватую или синюшно-багровую окраску. Сухая и шероховатая на ощупь поверхность бляшек лишена волос, включая пушковые, покрыта чешуйками, порой в большом количестве. При пальпации определяют очень плотную консистенцию (рис. 2). Нередко бляшки подвергаются спонтанному регрессу, оставляя после себя гиперпигментацию или, наоборот, депигментацию, а также легкую атрофию. Регрессу может подвергаться лишь центр бляшек. Бляшки в этих случаях принимают кольцевидные и полулунные очертания, а их распространение и слияние приводит к образованию гирляндоподобных фигур (рис. 3 (А)). Со временем бляшки в результате периферического роста и слияния друг с другом образуют обширные очаги поражения, на фоне которых сохраняются островки здоровой кожи. Кожа в области таких очагов утолщена, неподатлива, ее лишь с трудом удается собрать в складку; дермографизм здесь, как правило, белый. Они очень схожи с очагами атопического дерматита, особенно при локализации на сгибательной поверхности конечностей. Подкожные лимфатические узлы изменены, как и в I стадии, по реактивному (дерматропному) типу [1, 8].
Стадия III (опухолевая) характеризуется проявлением опухолевых высыпаний. Опухоли развиваются из предшествующих бляшек или на видимо неизмененной коже, резко выступают над кожей как плоские, полушаровидные или куполовидные образования, насыщенно красного, синюшно-красного или багрово-синюшного цвета диаметром от 1–2 см до 4–5 см. Возможны и более крупные опухоли диаметром до 10–15 см и даже 20 см. На ощупь опухоли плотные. Их вначале гладкая поверхность покрывается чешуйками, затем подвергается мацерации, эрозированию и изъязвлению. Поверхность эрозированных опухолей имеет вид насыщенно красной ссадины. Язвы могут быть обширными и глубокими, проникая нередко до фасций, мышц и даже костей. Дно язвенных дефектов может быть покрыто гнойно-кровянистым и некротическим налетом или буровато-черными корками (рис. 3 (Б-Д)). Такие язвенные очаги источают зловонный запах. Примерно у каждого пятого больного опухоли трансформируются в крупноклеточную саркому. Локализация опухолей может быть различна, нередко, кроме туловища и конечностей, поражаются лицо и волосистая часть головы. Поражение лица может протекать по типу Facies leonina. Помимо опухолей, на коже пациентов располагаются эритематозные и бляшечные высыпания, типичные для I и II стадий заболевания, что придает пораженной коже пестрый вид, зуд в опухолевой стадии может смягчаться. Течение заболевания обычно не превышает 2–3 года. Опухолевый процесс примерно у половины больных выходит за пределы кожного покрова, поражая лимфатические узлы, внутренние органы и костный мозг [1, 8].
Трансформация первичной эпидермотропной ТКЛК в анапластическую крупноклеточную лимфому детерминируется морфологическими признаками: более 25% крупных клеток или очаговый характер роста крупных клеток. При первичной эпидермотропной ТКЛК повышенный уровень внутридермальных CD30+ клеток (более 4,7%), индекс пролиферативной активности Ki-67+ (более 14% позитивных внутридермальных лимфоидных клеток) являются неблагоприятными прогностическими факторами [2]. Типичный иммунофенотип опухолевых клеток — CD2+, CD3+, CD4+, CD5+, CD45 RO+, TCRB+ (клон bF1). Характерна аберрантная экспрессия пан-Т-клеточных антигенов: менее 50% СD2-позитивных, СD3-позитивных и/или СD5-позитивных клеток по сравнению с CD4-позитивными клетками; часто отмечается утрата антигена CD7 (< 10% позитивных клеток). Следует обращать внимание на дискордантную экспрессию эпидермальными и дермальными клетками линейно ограниченных Т-клеточных антигенов — CD2, CD3, CD5. При первичной эпидермотропной ТКЛК CD4+ опухолевые клетки не экспрессируют цитотоксические белки. Экспрессия цитолитических белков возможна при прогрессировании заболевания или в тех редких случаях первичной эпидермотропной ТКЛК, при которых опухолевая популяция представлена CD8+ лимфоидными клетками с цитотоксическими свойствами. При первичной эпидермотропной ТКЛК присутствует разной степени выраженности популяция цитотоксических CD8+ лимфоцитов. В плане дифференциальной диагностики с актиническим ретикулоидом важно иметь в виду, что преобладающими клетками при хроническом фотодерматите являются поликлональные CD8+ лимфоциты [9–11].
В некоторых случаях первым проявлением первичной эпидермотропной ТКЛК служит эксфолиативная эритродермия. Она может возникать вновь или развиваться в результате прогрессии предшествующих элементов Т-клеточной лимфомы. Кожа при этом диффузно ярко-красная (иногда с симметричными не пораженными островками), шелушится. Характерны зуд, повышение температуры тела, слабость, снижение массы тела, лимфаденопатия, алопеция, эктропион, ониходистрофия. Гистологическая картина не отличается от таковой при классическом варианте первичной эпидермотропной ТКЛК. Диагноз устанавливают на основании комплекса клинических, морфологических, иммунофенотипических и молекулярно-генетических исследований, направленных на выявление клональной перестройки генов γ-, β-цепей TCR [2, 9].
Первичная эпидермотропная ТКЛК в течение нескольких лет или десятилетий протекает благоприятно, медленно прогрессируя в лимфому высокой степени злокачественности. После начала опухолевой стадии продолжительность жизни больных не превышает 3 лет [9]. На ранних стадиях изменения в лимфатических узлах носят реактивный характер и соответствуют дерматопатическому лимфадениту, на поздних — характеризуются специфическим поражением; в процесс также могут вовлекаться внутренние органы, кровь, костный мозг.
При первичной эпидермотропной ТКЛК, сопровождающейся патологическими изменениями показателей общего анализа крови (лейкоцитарно-лимфоцитарных популяций клеток), необходимо исследование костного мозга. При пальпируемых лимфатических узлах проводится их гистологическое исследование. Для оценки состояния средостенных, забрюшинных и тазовых лимфатических узлов, особенно в стадиях ТЗ и Т4 (по классификации TNM), проводят рентгенографию либо компьютерную томографию грудной клетки и/или брюшной полости и полости таза.
Диагностика лимфопролиферативных заболеваний кожи является одной из самых сложных проблем в дерматоонкологии. В большинстве случаев только комплексное обследование, включающее гистологический, иммуногистохимический, цитогенетический и молекулярно-биологический методы исследования в сочетании с анализом клинических данных, позволяет установить правильный диагноз. Применение иммуногистохимического исследования клеток лимфоидного инфильтрата, генотипирование лимфоцитов повышает возможности диагностики злокачественных лимфом кожи до 80–90% [9]. Объективным стандартизированным клиническим показателем степени тяжести течения ТКЛК служит индекс тяжести (ИТ) ТКЛК, при расчете которого суммируются баллы, оценивающие степень вовлечения в патологический процесс кожи, лимфатических узлов, периферической крови и внутренних органов (табл.).
Индекс также позволяет прогнозировать 5-летнюю выживаемость пациентов. Для вычисления индекса тяжести ТКЛК подсчитывается сумма баллов во всех категориях. Значения индекса колеблются от 0 до 75 баллов. Вероятная выживаемость (%) вычисляется по формуле:
124 – 2 × ИТ ТКЛК
Сходство ранних проявлений ТКЛК с другими многочисленными дерматозами весьма затрудняет своевременную диагностику заболевания. Возможность установления диагноза лимфом кожи только клиническими методами не превышает 50%, а использование цитоморфологических и гистологических методов в динамике заболевания при достаточной квалификации патоморфолога повышает достоверность диагностики до 75%. Ряд авторов выделяют особенности клиники и течения первичной эпидермотропной ТКЛК, позволяющие более достоверно провести дифференциальную диагностику, учитывая сходство начальных проявлений первичной эпидермотропной ТКЛК с множеством доброкачественных дерматозов и высокую частоту диагностических ошибок, которые включают: развитие заболевания в пожилом и старческом возрасте при отсутствии в анамнезе указаний на ранее установленный хронически протекающий дерматоз (постоянный интенсивный зуд кожи, не связанный с временем суток, характером питания и не устраняющийся при приеме антигистаминных препаратов); парестезии и озноб перед появлением свежих высыпаний; локализация очагов поражения в местах, не типичных для заболеваний, которые они клинически имитируют (псориаз, экзема, нейродермит и др.); застойно-синюшный цвет очагов поражения; вариабельность начальных клинических проявлений, что приводит к частой смене диагноза на протяжении всего периода заболевания; отсутствие стойкого положительного эффекта от обычно проводимой противовоспалительной и гипосенсибилизирующей терапии; нарастание инфильтрации в очагах поражения по мере развития заболевания [2, 12]. Зарубежные авторы [13] придерживаются следующих диагностических критериев для клинической диагностики ранней первичной эпидермотропной ТКЛК: прогрессирующие или персистирующие пятна/бляшки; поражение недоступных для ультрафиолетового облучения участков кожи; вариация размера/очертаний очагов поражения; наличие пойкилодермии.
Гистологическое исследование на ранних стадиях первичной эпидермотропной ТКЛК, являющееся обязательным, не всегда проясняет диагноз, так как на этом этапе заболевания клеточный инфильтрат еще не успевает сформироваться, а количество атипичных лимфоцитов в клеточном составе дермы крайне невелико и воспалительный компонент морфологической картины превалирует над пролиферативным. Ряд авторов в гистологической диагностике ТКЛК считают значимым следующее изменение эпидермиса: на ее ранних стадиях клетки, проникающие в эпидермис, обладают более высокой пролиферативной активностью, чем лимфоциты в дермальном пролиферате. Это подтверждает важную роль лимфоэпидермального взаимодействия в патогенезе лимфом кожи [2, 9, 12]. Гистологическая картина ТКЛК бывает наиболее яркой на поздней, опухолевой стадии заболевания, когда сформирован выраженный инфильтрат и в его клеточном составе доминирует пул атипичных клеток.
Рациональную терапию первичной эпидермотропной ТКЛК следует разрабатывать не только с учетом клинических и морфологических параметров, в соответствии со стадией патологического процесса, но и с учетом токсичности применяемых лекарственных средств при медленном течении болезни на ранних стадиях.
При первичной эпидермотропной ТКЛК в стадии Iа (процесс ограничен кожей (Т1, N0) с поражением < 10% кожного покрова) используют: местные кортикостероиды; фототерапию УФ-В; системные глюкокортикоидные гормоны, отдавая предпочтение преднизолону. Первоначальную суточную дозу 60 мг (12 таблеток) сохраняют до регресса клинических проявлений или значительного улучшения. Последующее снижение суточной дозы проводят по 5 мг (1 таблетка) в неделю до 20 мг (4 таблетки) в сутки. В этой дозе преднизолон принимают в течение 4 недель. Затем продолжают его снижение по 2,5–5 мг в неделю до полной отмены. Как правило, наступает продолжительная ремиссия, особенно при лечении преднизолоном сроком не менее 6 месяцев. В стадии Ib (процесс ограничен кожей (Т2, N0) с поражением > 10% кожного покрова) применяют: фототерапию УФ-В; ПУВА-терапию; Ре-ПУВА-терапию; ПУВА-терапию с интерфероном-α; местное облучение кожи пучком электронов; местную лучевую терапию отдельных элементов. В стадии II и при первичной эпидермотропной ТКЛК с дерматопатической лимфаденопатией (Т1–3, N0–1) назначают такое же лечение, как при стадии Ib. В стадии III и при первичной эпидермотропной ТКЛК с поражением лимфатических узлов (Т1–4, N2) проводят: системную (поли-) химиотерапию; локальную лучевую терапию опухолей. В стадии IV и первичной эпидермотропной ТКЛК с поражением внутренних органов (Т1–4, N2 б, M1) проводят такое же лечение, как в стадии III [2, 11, 14].
При генерализации процесса, а также при первичной эпидермотропной ТКЛК высокой степени злокачественности независимо от стадии основным методом лечения является полихимиотерапия с использованием схемы ЦАВП (в первый день — внутривенно циклофосфамид, 750 мг/м2, адриамицин, 50 мг/м2, винкристин, 1,4 мг/м2, и в 1–5 дни — преднизолон, 40 мг/м2 внутрь). Схема состоит из 6–8 циклов, которые проводят каждые 4 недели под контролем крови; эффективность ее — 45% [2].
При ихтиозиформной первичной эпидермотропной Т-клеточной лимфоме эффективна системная терапия ретиноидами в комбинации с ПУВА- или УФ-А-терапией. Фолликулотропный вариант первичной эпидермотропной ТКЛК в связи с глубоким расположением дермальных инфильтратов менее чувствителен к местной терапии, рентгенотерапии и ПУВА-терапии, в связи с чем рекомендуется прием внутрь сульфонов, глюкокортикоидов (в том числе в сочетании с цитостатиками), обкалывание гидрокортизоном, системное применение интерферона-α, облучение кожи электронным пучком. При педжетоидном ретикулезе лечение хирургическое: иссечение, внутриочаговые инъекции кортикостероидных гормонов, ПУВА-терапия, лучевая терапия. При синдроме гранулематозной «вялой» кожи используется лучевая терапия, сильные местные глюкокортикоиды. Элементы часто рецидивируют после хирургического удаления. Терапией первой линии синдрома Сезари является экстракорпоральная фотохимиотерапия, эффективность которой достигает 73% с полной ремиссией в 21% случаев. Кроме того, проводится терапия быстрыми электронами. При трансформации в агрессивную крупноклеточную лимфому — полихимиотерапия. Методы лечения опухолевой стадии первичной эпидермотропной ТКЛК остаются неудовлетворительными. Болезнь быстро прогрессирует, несмотря на применение полихимиотерапии [1, 2, 8]. По мнению Beyer M. с соавт. комбинация препаратов бексаротин и вориностат является перспективной стратегией повышения эффективности лечения первичной эпидермотропной ТКЛК и снижения частоты побочных эффектов [15].
Таким образом, проблема первичных Т-клеточных кожных лимфом является одной из важнейших и приоритетных проблем современной медицины как в связи с их высокой распространенностью, так и чрезвычайной сложностью диагностики и лечения, требующих учета многих факторов и использования широкого спектра современных методов обследования (гистологических, иммунологических, молекулярно-генетических), позволяющих правильно определить прогноз и оптимизировать терапию.
Литература
- Потекаев Н. С. Грибовидный микоз. Клиническая дерматовенерология. Руководство для врачей под ред. Ю. К. Скрипкмна, Ю. С. Бутова. М.: ГЭОТАР-Медиа, 2009. Т. 2. C. 576–589
- Молочков А. В., Ковригина А. М., Кильдюшевский А. В. с соавт. Лимфома кожи. Издательство БИНОМ, 2012. 184 с.
- Петренко Е. В. Совершенствование ранней диагностики Т-клеточных лимфом кожи на основе оценки экспрессии TsPO (периферического бензодиазепинового рецептора) как маркера интенсивности пролиферации опухолевых клеток: Автореф. дисс. … канд. мед. наук. М., 2011. 23 с.
- Подцубная И. В. Неходжкинские лимфомы. Клиническая онкогематология. Под. ред. М. А. Волковой. М.: Медицина, 2001. С. 336.
- Pilvi Maliniemi, Michelle Vincendeau, Jens Mayer, Oliver Frank et al. Human endogenous retrovirus type w envelope expression in mycosis fungoides provides new Insights in cutaneous T-сеll lymphomas. EORTC CLTF 2012. Targets for therapy in cutaneous lymphomas. 2012. Р. 27.
- Willemze R., Jaffe E. S., Durg G. et al. WHO-EORTC classification for cutaneous lymphomas // Blood. 2005. Vol. 105, № 10. P. 3768–3785.
- Клинические рекомендации. Дерматовенерология. Под ред. А. А. Кубановой. М.: ДЭКС-Пресс, 2010. 428 с.
- Короткий Н. Г., Уджуху М. В. Современные взгляды на этиопатогенез грибовидного микоза и схемы его лечения // Лечащий Врач. 2007. № 4. С. 35–37.
- Молочков В. А., Ковригина А. М., Овсянникова Г. В. Т-клеточные лимфомы кожи: современные походы к клинико-морфологической диагностике (согласно классификации ВОЗ/ЕОRТС) и лечению // Росс. журн. кож. вен. болезней. 2009. № 3. С. 4–9.
- Потекаев Н. Н. Реактивные дерматозы // Клиническая дерматология и венерология. 2010. № 1. С. 83–86.
- Доронин В. А. Диагностика и лечение первичных Т-клеточных лимфом кожи // Лечащий Врач. 2005. № 7. С. 15–19.
- Овсянникова Г. В., Лезвинская Е. М. Злокачественные лимфомы кожи. Consilium Medicum. 2005. Т. 7. № 1. С. 21–23
- Rook A., Wysocka M. Citokines and other biologic agents as immunotherapeutics for cutaneous T-cell lymphoma // Adv. Dermatol. 2002; 18; 29–43.
- Kim E. J., Hess S., Richardson S. K. et al. Immunopathogenesis and therapy of cutaneous T-cell lymphoma // J. Clin. Inv. 2005. Vol. 115, № 5. Р. 798–812.
- Beyer M., Humme D., Sterry W. Current status of combination therapies in Mycosis fungoides/Sezary syndrome. EORTC CLTF 2012. Targets for therapy in cutaneous lymphomas, 2012. Р. 23.
Л. А. Юсупова1, доктор медицинских наук З. Ш. Гараева, кандидат медицинских наук Е. И. Юнусова, кандидат медицинских наук Г. И. Мавлютова, кандидат медицинских наук
ГБОУ ДПО КГМА МЗ РФ, Казань
1 Контактная информация
Стадии лимфомы
Сразу после обнаружения заболевания врачи определяют его стадию – выясняют, как далеко оно успело распространиться и какие ткани повредило. Данная информация крайне важна для специалистов, поскольку она позволяет не только понимать прогнозы пациента, но и подбирать для него самое подходящее лечение.
Стадии лимфомы Ходжкина:
I
: измененные клетки обнаружены только в одной группе лимфатических узлов или одном лимфоидном органе, таком как миндалины.
II
: они присутствуют в 2 или более группах лимфоузлов, расположенных по одну сторону от диафрагмыДиафрагма – это мышца, которая отделяет грудную полость от брюшной., либо распространились из одного поврежденного лимфоузла на соседний орган.
III
: клетки лимфомы есть в лимфоузлах по обе стороны диафрагмы; либо не только в лимфатических узлах над диафрагмой, но и в селезенке.
IV
: заболевание распространилось по крайней мере в один орган, не входящий в лимфатическую систему, такой как печень, костный мозг или легкие.
Стадии неходжкинских лимфом:
I
: измененные клетки обнаруживаются только в 1 группе лимфатических узлов или одном лимфоидном органе, например, миндалинах; либо в 1 области одного органа за пределами лимфатической системы.
II
: они присутствуют в 2 или более группах лимфоузлов по 1 сторону от диафрагмы; либо в лимфатических узлах и 1 области расположенного рядом одного органа, или в еще одной группе лимфоузлов на той же стороне диафрагмы.
III
: клетки лимфомы есть в лимфоузлах по обе стороны от диафрагмы; либо они присутствуют и в лимфатических узлах над диафрагмой, и в селезенке.
IV
: заболевание распространилось по крайней мере в один орган, не входящий в лимфатическую систему, такой как печень, костный мозг или легкие.
Определение стадии (степени распространения) неходжкинских лимфом
После детального обследования, включающего все вышеперечисленные методы, уточняется стадия лимфомы (сI — по IV) в зависимости от степени распространения опухолевого процесса.
При наличии у больного общих симптомов к стадии добавляется символ Б (или латинская буква В), а при их отсутствии — символ А.
Для прогнозирования скорости роста опухоли и эффективности лечения разработан международный прогностический индекс (МПИ), который учитывает 5 факторов, включая возраст больного, стадию заболевания, поражение не только лимфатических узлов, но и других органов, общее состояние больного, уровень лактатдегидрогеназы (ЛДГ) в сыворотке крови.
К благоприятным прогностическим факторам относятся: возраст менее 60 лет, стадии I-II, отсутствие поражения органов, хорошее общее состояние, нормальные уровни ЛДГ.
К неблагоприятным прогностическим факторам относятся: возраст пациента выше 60 лет, стадии III и IV, поражение лимфатических узлов и органов, неудовлетворительное общее состояние и повышение уровней ЛДГ.
Лечение лимфомы
Лечение лимфомы – задача непростая. Для ее решения требуется не один доктор, а целая команда профессионалов своего дела – химиотерапевта, радиолога, хирурга, онколога, гематолога и других.
В онкологическом есть все необходимые специалисты – врачи мирового уровня, которые проводят полную диагностику заболевания и любую необходимую терапию.У нас вам не придется пересдавать анализы, переделывать исследования и задаваться вопросом «что делать дальше?». Мы полностью ведем пациента и даем ему четкий план действий, следуя которому он получает лучший результат из возможных.
Для борьбы с данным типом онкологии применяется несколько методов:
Основным из них является химиотерапия
– препараты, которые уничтожают измененные клетки. Они принимаются в виде таблеток или вводятся в вену, попадают в кровоток и распространяются по всему телу. Лечение проводится циклами, каждый из которых длится несколько недель, после чего следует период отдыха, за время которого организм восстанавливается.
Трансплантация костного мозга
или стволовых клеток, из которых образуются клетки крови. Процедура позволяет назначать более высокие дозы химиотерапии, иногда вместе с лучевой терапией, благодаря чему лимфома уничтожается эффективнее. Пересадка возможна не только донорского, но и своего собственного, собранного за несколько недель до вмешательства материала.
Лучевая терапия
– уничтожение измененных клеток с помощью радиации. Данный метод подходит для большинства пациентов, и особенно хорошо работает, если заболевание успело поразить небольшое количество тканей. Его применяют как самостоятельно, так и в сочетании с химиотерапией.
Иммунотерапия
– препараты, которые помогают собственной иммунной системе человека лучше распознавать и разрушать неправильные клетки. Существует несколько их типов, применяемых при лимфомах. К ним относят:
- моноклональные антитела – белки, разработанные для атаки определенного вещества на поверхности лимфоцитов;
- ингибиторы иммунных контрольных точек – лекарства, не позволяющие измененным клеткам маскироваться под здоровые;
- Т-клеточная терапия: изъятие из крови пациента и изменение в лаборатории иммунных клеток, их размножение и возвращение в организм, где они отыскивают и уничтожают очаги заболевания.
Хирургия
: часто используется для получения образцов подозрительных тканей и определения их типа, но редко – для терапии как таковой. В редких случаях операции назначаются при поражениях селезенки или других органов, которые не входят в лимфатическую систему – например, щитовидная железа или желудок.
Виды лимфом по агрессивности
Поскольку заболеваний, которые входят в эту группу, много, их принято делить на группы по разным признакам. Один из них — агрессивность течения.
Так называемые вялые лимфомы (они же индолентные) развиваются медленно и в течение нескольких лет не угрожают жизни пациента. При своевременном лечении высоки шансы на долгую и стойкую ремиссию. В эту группу включают лимфоцитарную, а также фолликулярную лимфому.
Агрессивные формы, к которым относятся диффузные (смешанные и крупноклеточные) формы, способны убить организм в течение месяцев, а высокоагрессивные — даже в течение недель. К последним, например, относятся Т-клеточная лейкемия, лимфома Беркитта. В лечении любого заболевания и в поддержании адекватного состояния пациента большую роль играет своевременность профессиональной помощи.
Диспансерное наблюдение при НХЛ
Динамическое наблюдение за детьми и подростками проводится в течение не менее 3-х лет после завершения лечебной программы.
В первые 3 месяца пациент обследуется каждый мес, в последующие 9 месяцев – каждый квартал, затем раз в полгода.
Обследование включает осмотр пациента с оценкой жалоб, клинический и биохимический анализы крови с определением ЛДГ, УЗИ очагов первичного поражения, рентгенограмм грудной клетки, по показаниям используются КТ/МРТ.
В последние годы для динамического наблюдения за излеченными больными с целью ранней диагностики рецидива широкое распространение получил метод ПЭТ/КТ всего тела с глюкозой.