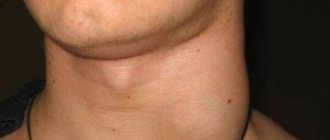
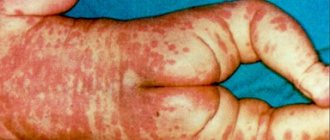
Нейтрофилы – это самая многочисленная группа гранулоцитов, основной функцией которых является фагоцитоз (уничтожение) патогенной флоры в организме человека.
Нейтропения – это уменьшение количества нейтрофилов в крови, что приводит к риску возникновения бактериальных и грибковых инфекций.
В здоровом состоянии защиту иммунных «границ» предоставляют зрелые сегментоядерные нейтрофилы. Помогают «контролировать» ситуацию и более молодые – палочкоядерные нейтрофилы, но их намного меньше (это хорошо видно по результату анализа крови, где в норме зрелых нейтрофилов насчитывается от 42-72%, а молодых всего от 1-6%).
Но, в случае возникновения тех или других заболеваний, соотношение всех видов нейтрофилов (сегментоядерных, палочкоядерных, миелоцитов, метамиелоцитов) резко нарушается, что приводит к патологическому повышению нейтрофилов или их уменьшению (нейтропении).
При этом количество нейтрофилов в крови человека — не стабильно, в отличие от других клеточных групп лейкоцитарной формулы. На созревание, развитие и нормальное соотношения данных гранулоцитов, влияют не только врожденные, приобретенные патологии, но и резкое эмоциональное потрясение, стресс нарушение рациона питания и т.д.
Нейтропения у детей должна быть тщательным образом исследована, чтобы предотвратить как тяжелые патологии, так и радикальное лечение без серьезных на то причин.
Классификация степеней тяжести нейтропении:
- Легкая (1-1,5 х 109/л);
- Умеренная (0,5-1 х109/л);
- Тяжелая (меньше 0,5 х109/л).
Если уровень нейтрофилов критически снижается – это приводит к развитию инфекции в кишечнике, во рту, вызывая тем самым расстройство пищеварительной системы, гингивиты, стоматиты, грибковые поражения кожи и т.д.
Тяжелая нейтропения при наличии онкопатологии крайне неблагоприятно влияет на работу иммунной системы, приводя к прогрессирующим воспалениям и инфекциям, вплоть до летального исхода.
Этиология
Нейтрофилы развиваются в костном мозге в течение 15 дней, находятся в кровеносном русле около 8 часов, составляют подавляющую клеточную часть лейкоцитарной формулы и при обнаружении «вредителей» тут же отправляются на их ликвидацию.
Основные причины нейтропении, которые нарушают данный физиологический процесс:
- Развитие патогенной флоры в организме (бактерии, вирусы, грибки).
- Воздействие радиации, проведение химиотерапии.
- Патологии в работе костного мозга.
- Дефицит фолиевой кислоты.
- Врожденные патологии внутренних органов, желез и систем.
Нейтропения у детей, также может развиться в связи с нарушением работы поджелудочной железы и заторможенным умственным развитием (синдром Швахмана-Даймонда-Оски).
Нейтропения разделяется на:
- Острую;
- Хроническую.
Острая нейтропения развивается стремительно на фоне быстрого потребления/разрушения нейтрофилов, хроническая — из-за сокращения выработки гранулоцитов или же избыточной селезеночной секреции.
- Первичную;
- Вторичную.
Первичная нейтропения связанная с внутренними нарушениями (врожденные патологии, идиопатическая нейтропения, циклическая нейтропения, доброкачественная этническая), вторичная — обусловлена влиянием внешних факторов на созревание и развитие клеток костного мозга.
Уход
Рекомбинантный гранулоцитарно-колониестимулирующий фактор препараты, такие как филграстим[21] может быть эффективным у людей с врожденными формами нейтропении, включая тяжелую врожденную нейтропению и циклическую нейтропению;[22] количество (дозировка), необходимое для стабилизации количества нейтрофилов, значительно варьируется (в зависимости от состояния человека).[23] Рекомендации по диете при нейтропении в настоящее время изучаются.[24]
Большинство случаев неонатальной нейтропении являются временными. Профилактика антибиотиками не рекомендуется из-за возможности стимулирования развития штаммов бактерий с множественной лекарственной устойчивостью.[1]
Нейтропению можно лечить с помощью гемопоэтических факторов роста, гранулоцитарно-колониестимулирующего фактора (G-CSF) или гранулоцитарно-макрофагального колониестимулирующего фактора (GM-CSF). Это цитокины (химические вещества, вызывающие воспаление), которые естественным образом присутствуют в организме. Эти факторы регулярно используются при лечении рака у взрослых и детей. Эти факторы способствуют восстановлению нейтрофилов после противоопухолевой терапии.[1]
Введение внутривенных иммуноглобулинов (ВВИГ) имело определенный успех в лечении нейтропений аллоиммунного и аутоиммунного происхождения с частотой ответа около 50%. Переливания крови оказались неэффективными.[1]
Пациентам с нейтропенией, вызванной лечением рака, можно назначать противогрибковые препараты. Кокрановский обзор [25] обнаружили, что липидные препараты амфотерицина B имели меньше побочных эффектов, чем обычный амфотерицин B, хотя неясно, есть ли особые преимущества перед обычным амфотерицином B при применении в оптимальных условиях. Еще один Кокрановский обзор [26] не удалось обнаружить разницу в действии между амфотерицином B и флуконазолом, потому что имеющиеся данные испытаний проанализировали результаты таким образом, чтобы не благоприятствовать амфотерицину B.
Вторичная нейтропения
Вторичная нейтропения чаще всего развивается вследствие:
- Приема определенных препаратов (антибиотики, антигистаминные средства, жаропонижающие, барбитураты, анальгетики);
- Развития инфекций;
- Иммунных реакций;
- Инфильтрации костного мозга.
Вторичная нейтропения провоцирует патологии:
- Печени, селезенки, почек;
- Поджелудочной железы, щитовидки;
- Апластическая анемия;
- Мегалобластная анемия;
- Миелодиспластические расстройства;
- Миелофиброз, лейкоз;
- Сепсис, ВИЧ, синдром Фелти;
- Резус-конфликтная нейтропения;
- Лимфопролиферативные заболевания и т.д.
В случае с вторичной нейтропенией лечить нужно не «анализ» крови, а пациента с конкретными симптоматическими проявлениями.
Первичную и вторичную нейтропению стоит различать, так как в первом случае понижение уровня нейтрофилов – это единственное проявление, тогда как вторичные развиваются на основе инфекций, системных аутоиммунных патологий и онко неоплазий.
Тяжелая врожденная нейтропения (SCN)
SCN— гетерогенная группа заболеваний, в основе которых лежит нарушение гранулоцитопоэза на уровне промиелоцитов со снижением числа нейтрофилов ниже 0,2*109/л в периферической крови. Заболевание манифестирует в первые дни жизни. SCN подразделяют на несколько форм по типу наследования и генам, мутации в которых приводят к заболеванию:
| Форма SCN | Тип наследования | Ген |
| SCN1 (OMIM 202700) | АД | ELANE |
| SCN2 (OMIM 600871) | АД | GFI1 |
| SCN3 (OMIM 610738) | АР | HAX1 |
| SCN4 (OMIM 612541) | АР | G6PC3 |
*Синим цветом выделены гены, анализ которых проводится в ООО «Центр Молекулярной Генетики».
Данные формы SCN клинически не различимы.
По литературным данным в Европе 60% случаев SCN имеют аутосомно-доминантный тип наследования.
Также описаны другие наследственные формы тяжелой наследственной нейтропении, например, X-сцепленная тяжелая наследственная нейтропения OMIM300299 (мутации в гене WAS).
Клинические проявления
В большинстве случае нейтропения протекает без каких-либо признаков. Симптомы снижения нейтрофилов обычно возникают только тогда, если развилась вторичная нейтропения, на фоне тех или других патологий.
Общая симптоматика нейтропении:
- Повышение температуры тела;
- Рецидивирующие стоматиты, гингивиты, глосситы;
- Выраженная слабость;
- Усиленное потоотделение;
- Озноб;
- Нарушение мочеиспускания (жжение);
- Кашель (на фоне пневмонии, воспалительного процесса в легких);
- Грибковые поражения кожи.
В результате резкого понижения гранулоцитов, также может развиться фебрильная нейтропения. Это лихорадочное состояние отягощенное тахикардией, тремором, ознобом, повышением АД, вплоть до развития сердечно-сосудистого коллапса.
Фебрильная нейтропения обычно развивается вследствие онкопатологий, воздействия лучевой или химиотерапии, в виде гиперергической реакции организма на токсические влияния (цитостатиков, распад здоровых и онкоклеток).
Может проявляться и на фоне тяжелого инфекционного процесса, который провоцируют стафилококки, стрептококки, клостридии, реже грибки и вирусы. В более редких случаях фебрильная нейтропения может развиться на основе первичной аутоиммунной нейтропении.
Когда следует обращаться к своему медицинскому сотруднику?
Немедленно свяжитесь со своим медицинским сотрудником, если у вас появился какой-либо из следующих признаков инфекции:
- температура 100,4 °F (38 °C) или выше;
- потрясающий озноб;
- непроходящая тошнота и рвота;
- покраснение лица;
- потливость;
- кашель;
- предобморочного состояния или головокружения;
- диарея (жидкий или водянистый стул);
- запоры (опорожнение кишечника происходит реже, чем обычно);
- Язвы во рту
- Головная боль
- боль в новом месте;
- Раздражительность
- боль или жжение при мочеиспускании (когда ходите в туалет по-маленькому);
- чувство слабости, особенно в сочетании с симптомами гриппа (такими как повышенная температура, боль в горле и озноб).
Вернуться к началу
Диагностика
Диагностика может быть плановой, внеплановой (при наличии специфической симптоматики), а также может проводиться при наличии каких-либо подозрений у лечащего врача (необычные или часто повторяющиеся инфекции).
Плановое исследование крови у детей до 1 года проводится 1 раз в 3 месяца, после года – 1 раз в 6 месяцев (включая взрослых).
Если диагностика засвидетельствовала понижение нейтрофилов в крови, дополнительно должно быть назначено:
- Скрининговое исследование нейтропении;
- Дифференциация нейтропении с другими патологиями;
- Уточнение формы нейтропении;
- Исследование механизмов развития данного состояния у пациента.
Далее проводится оценка динамики показателей лейкоцитарной формулы (после перенесенных инфекций, между ними, после выздоровления), включая СОЭ (скорость оседания эритроцитов), цветовой показатель и т.д.
Определение причины нейтропении может включать такие диагностические манипуляции:
- Визуальный осмотр.
- Физикальный осмотр (оценка состояния всех слизистых оболочек).
- Рентгенографию.
- КТ, ЭКГ, УЗИ, МРТ.
- Лабораторные исследования крови (общий анализ, биохимический), мочи.
- Культуральный посев (на определение вида бактерий и грибков).
- Биопсию.
- Исследования костного мозга (для определения причины специфической нейтропении, при лейкемии, апластической анемии, миелофиброзе).
В случае тяжелой нейтропении в острой форме — комплексная диагностика должна быть выполнена максимально оперативно.
Если рассматривается врожденная патология, диагностика включает молекулярно-генетическое исследование нейтропении.
По одному анализу крови, который показал низкий уровень гранулоцитов, невозможно поставить окончательный диагноза. Так как это единственные клетки крови, концентрация которых может меняться ежедневно, ввиду короткой «жизни» в кровяном русле (6-8 часов).
Для точного подтверждения состояния пациента, анализ крови нужно повторить с небольшим интервалом времени (время сдачи анализов устанавливает врач).
Одним из наиболее частых и опасных побочных эффектов цитостатической терапии является нейтропения. Цитостатики, действуя на быстроделящиеся клетки, затрагивают и систему кроветворения. Циркулирующие нейтрофилы живут в среднем 6–9 часов, и система гемопоэза постоянно вырабатывает около 50 млн этих клеток в 1 минуту для замещения выбывших. Снижение продукции нейтрофилов после воздействия химиопрепаратов приводит к быстрому уменьшению содержания этих клеток в периферической крови, что повышает риск развития инфекционных осложнений.
Длительная нейтропения зачастую не позволяет проводить химиотерапию (ХТ) в запланированные сроки, заставляет редуцировать дозы цитостатиков, что в свою очередь снижает эффективность противоопухолевого лечения. Кроме того, инфекционные осложнения на фоне нейтропении в отсутствие адекватной терапии характеризуются стремительным течением и высокой летальностью. В связи с этим существует необходимость тщательной оценки миелотоксического потенциала современных режимов химиотерапии и выявления групп больных с высоким риском развития нейтропении, которым требуется профилактическое назначение колониестимулирующих факторов (КСФ).
Повышенный риск развития инфекции на фоне нейтропении обусловил выделение симптомокомплекса “фебрильная нейтропения” (ФН). Согласно руководству NCCN (National Comprehensive Cancer Network) [1], ФН характеризуется повышением температуры в ротовой полости выше 38,5 °С при однократном измерении или выше 38,0 °С при двух последовательных измерениях в течение 2 часов при абсолютном числе нейтрофилов (АЧН) в крови менее 0,5 × 109/л или ожидаемом снижении < 0,5 × 109/л.
Перед первым циклом ХТ пациента необходимо оценить риск развития ФН. При этом должны учитываться: • режим ХТ (высокодозная, дозоинтенсивная, стандартная); • тип опухоли; • дополнительные факторы риска; • цель проводимой ХТ (направленная на выздоровление, паллиативная).
Риск развития ФН напрямую связан с интенсивностью химиотерапевтического режима. Согласно рекомендациям NCCN [1], химиотерапевтические режимы, вызывающие ФН более чем в 20 % случаев, должны рассматриваться как режимы с “высоким риском” развития ФН. В подобных ситуациях рекомендуется назначение гранулоцитарных КСФ (Г-КСФ) в качестве первичной профилактики. Аналогичные рекомендации дают Американское общество клинической онкологии (ASCO – American Society Clinical Oncology) [2] и Европейская организация по исследованию и лечению рака (EORTC – European Organization Research and Treatment of Cancer) [3].
При “промежуточном риске” вероятность развития ФН или нейтропенической инфекции составляет 10–20 %. Вне зависимости от цели проводимого лечения NCCN рекомендует в этой ситуации рассматривать вопрос о необходимости назначения КСФ в каждом индивидуальном случае. При этом следует учитывать соотношение риска и пользы от применения КСФ, вероятность развития ФН, потенциальные последствия нейтропенической инфекции, а также отдаленные результаты лечения онкологических больных, получавших химиопрепараты в редуцированных дозах. Когда проводимое лечение не направлено на выздоровление и оно является симптоматическим, а риск определя-
ется режимом ХТ, рекомендуется рассматривать альтернативные способы профилактики ФН (использование менее миелосупрессивных режимов ХТ, редукцию доз химиопрепаратов). В данной ситуации применение КСФ нецелесообразно.
Пациентам с “низким риском” ФН (< 10 %) рутинное использование КСФ не рекомендуется. КСФ могут применяться только в тех случаях, когда больной получает адъювантную ХТ или существует высокий риск развития серьезных осложнений ФН, а редукция доз химиопрепаратов приводит к снижению эффективности противоопухолевого лечения.
Ниже приводятся химиотерапевтические режимы с высоким (табл. 1) и промежуточным (табл. 2) риском развития ФН.
. Режимы ХТ с высоким риском развития ФН.
. Режимы ХТ с промежуточным риском развития ФН.
Помимо вышеописанных основных факторов риска развития ФН существуют дополнительные, которые необходимо учитывать при определении общего риска ФН. Дополнительные факторы могут повышать общий риск до более высокой категории.
К дополнительным факторам относятся возраст пациента старше 65 лет (выше риск развития ФН, более высокие показатели частоты осложнений и смертности); проводимая ранее ХТ;наличие в анамнезе глубокой нейтропении (АЧН < 100/мкл), нейтропении протяженностью >10 дней или ФН после ХТ; вовлечение в опухолевый процесс костного мозга; лучевая терапия в анамнезе; недавно перенесенное оперативное вмешательство; наличие раневого процесса; плохой соматический статус пациента; нарушение функции печени и почек; пневмония; присоединившаяся грибковая инфекция.
Риск развития инфекционных осложнений у больных нейтропенией обусловлен не только уменьшением АЧН, но и нарушением функциональных свойств нейтрофилов (ослабление хемотаксиса и фагоцитоза; нарушение экзогенной продукции ростовых факторов, таких как интерлейкин-1, интерлейкин-3, гранулоцитарно-макрофагального КСФ, Г-КСФ; изменение активности ферментов; снижение образования активных форм кислорода).
Оценка риска развития ФН должна проводиться перед каждым курсом ХТ. Если пациент в течение предыдущего цикла ХТ перенес эпизод ФН или дозолимитирующей нейтропенической инфекции и проводимая ХТ направлена на выздоровление, проведение последующих курсов ХТ в прежних дозах влечет за собой “высокий риск” развития ФН. В таких случаях необходимо рассмотреть вопрос об использовании КСФ. Если пациент перенес эпизод ФН, несмотря на использование КСФ, NCCN рекомендует провести редукцию доз химиопрепаратов во время последующих циклов или изменить режим ХТ.
Эти рекомендации основаны на результатах крупных рандомизированных исследований, показавших, что риск развития ФН может быть значи-тельно снижен благодаря проведению первичной профилактики с использованием КСФ.
Vogel и соавт. [4] в двойном слепом рандомизированном плацебо-контролируемом многоцентровом исследовании установили, что при первом и всех последующих циклах ХТ профилактическое назначение КСФ (пегилированный филграстим) значительно снижает риск развития ФН при режимах ХТ, которые прежде ассоциировались с “высоким риском” этого осложнения. В исследование были включены больные РМЖ, получавшие доцетаксел 100 мг/м2 каждые 3 недели. Пациентки были распределены в 2 группы: 1-я группа (465 жен-щин) получала инъекции плацебо; 2-я группа (463 женщины) – пегфилграстим подкожно (вводился через 24 часа после завершения цикла ХТ). В группе плацебо частота развития ФН составила 17 %, в группе пегфилграстима – 1 %. Потребность в госпитализации уменьшилась с 14 до 1%, а в использовании внутривенной антибактериальной терапии (АБТ) – с 10 до 2 % (p < 0,001).
В исследовании Timmer–Bonte и соавт. [5] 175 больных МРЛ получали лечение комбинацией циклофосфан +доксорубицин + этопозид. В последующем все пациенты были рандомизированы в 2 группы: в 1-й группе проводилась профилактическая АБТ (ципрофлоксацин + рокситромицин); 2-я группа получала АБТ + Г-КСФ (в 4–13-й дни цикла). После первого цикла ХТ развитие ФН отмечено у 20 (24 %) пациентов группы, получавшей только антибиотики, по сравнению с 9 (10 %) больными, получавшими АБТ + Г-КСФ (p = 0,01).
Таким образом, у пациентов с “высоким риском” развития ФН первичная профилактика с помощью КСФ в сочетании с АБТ значительно снижает риск развития инфекционных осложнений [6, 7].
В некоторых исследованиях (Labro М.Т., 2000; Nelson S., 2001) было установлено, что Г-КСФ усиливают действие АБТ за счет повышения внутриклеточной концентрации антибиотика в нейтрофилах, что в свою очередь оказывает модифицирующий эффект на функциональную активность нейтрофилов. Повышается их антителозависимая цитотоксичность по отношению к опухолевым клеткам; ускоряется фагоцитоз бактерий и грибов; происходит миграция нейтрофилов из периферической крови в очаги инфекции и воспаления.
К применяемым в настоящее время Г-КСФ относятся филграстим, пегфилграстим и сарграмостим. Филграстим рекомендуется использовать в ежедневной дозе 5 мкг/кг/сут подкожно через 24–72 часа после введения последней дозы противоопухолевых препаратов до достижения стабильного и достаточного АЧН. Пегфилграстим (используется только для профилактики ФН) вводится подкожно 1 раз в общей дозе 6 мг через 24–72 часа после введения последней дозы противоопухолевых препаратов. Применяют его при химиотерапевтических режимах, курс которых составляет 3 недели. Сарграмостим вводится по 250 мкг/м²/сут подкожно через 24–72 часа после введения последней дозы противоопухолевых препаратов до достижения стабильного и достаточного АЧН. Следует обратить внимание, что условие введения Г-КСФ через 1–3 суток после последней дозы цитостатиков связано с чувствительностью активно пролиферирующих миелоидных клеток к миелосупрессивной ХТ.
Первым из препаратов Г-КСФ, доступным для клинического применения, стал филграстим, полученный с использованием рекомбинантной технологии в культурах Escherichia coli. В настоящее время существует много препаратов филграстима, одним из которых является Граноген.
Этот Г-КСФ стимулирует пролиферацию колониеобразующих клеток – предшественников нейтрофильного ростка костного мозга, ускоряет их дифференцировку и выход зрелых нейтрофилов из костного мозга в периферическую кровь, усиливает эффекторные функции нейтрофилов (хемотак- сис, фагоцитоз, окислительный метаболизм). Граноген вызывает быстрое, специфическое и дозозависимое увеличение числа нейтрофилов в периферической крови, что объясняется укорочением времени созревания с 5 до 1 дня, повышением количества клеточных делений и ускоренным выходом клеток в периферическую кровь. Граноген уменьшает частоту, тяжесть и продолжительность нейтропении и ФН у больных, получающих миелосупрессивную терапию, что позволяет снижать частоту инфекционных осложнений, уменьшать потребность в АБТ.
Побочные эффекты при применении Г-КСФ, в т. ч. Граногена, встречаются редко; они маловыраженны.
Для лечения нейтропении после курса цитотоксической терапии Граноген вводят в дозе 0,5 млн ЕД (5 мкг) на 1 кг массы тела, 1 раз в сутки, ежедневно, подкожно или в виде коротких (в течение 30 минут) внутривенных инфузий. Граноген не совместим с 0,9 %-ным раствором натрия хлорида. Предпочтителен подкожный путь введения. Увеличение числа нейтрофилов обычно наблюдается через 1–2 дня после начала лечения. Для достижения стабильного терапевтического эффекта необходимо продолжать терапию до тех пор, пока количество нейтрофилов не перейдет через ожидаемый минимум (надир) и не вернется в диапазон нормальных значений. Не рекомендуется отменять препарат преждевременно. Лечение прекращают, если АЧН после надира достигло 1 × 109/л. После ХТ, проведенной по поводу сóлидных опухолей, длительность лечения может составлять до 14 дней. При увеличении числа лейкоцитов > 50·× 109/л Граноген следует немедленно отменять.
Успех лечения ФН во многом зависит от раннего распознавания возможной инфекции и раннего начала терапии. Нейтропения значительно ослабляет иммунный ответ организма, что не позволяет развиваться характерным клиническим проявлениям инфекции, затрудняя ее клиническую диагностику у онкологических больных. Гипертермия у пациентов с нейтропенией часто бывает единственным признаком инфекционного процесса.
Согласно клиническим рекомендациям ESMO, необходимо проводить тщательные первичный осмотр и обследование на выявление возможных очагов инфекции [8]: 1. Наличие длительно стоящего центрального венозного катетера. 2. Симптомы и признаки наличия инфекции дыхательной системы, сердечно-сосудистой системы, желудочно-кишечного тракта, кожных покровов, мочеполовой системы, центральной нервной системы. 3. Данные о предшествующих положительных результатах микробиологического анализа. 4. Рутинные лабораторные и инструментальные исследования: • общий и биохимический анализы крови, коагулограмма, С-реактивный белок; • посев крови (минимум 2 раза), включая посев из центрального венозного катетера; микроскопическое исследование и посев мочи; • микроскопическое исследование мокроты и ее посев; • микроскопическое исследование кала и его посев (при диарее); • исследование очагов инфекции на коже (аспират, биопсия, мазок); • рентгенография органов грудной клетки. 5. Дальнейшие исследования (при длительной и глубокой нейтропении): компьютерная томография органов грудной клетки (если лихорадка сохраняется, несмотря на адекватную АБТ, более 72 часов).
Немедленный подсчет формулы крови для установления числа нейтрофилов параллельно с другими исследованиями, представленными выше, имеют ключевое значение для определения необходимости начала ранней терапии ФН.
Международной ассоциацией поддерживающей терапии при раке (MASCC) разработан прогностический индекс [9, 10]. Он позволяет быстро оценивать риск осложнений – до того, как станет известно содержание нейтрофилов в крови пациента. Эффективность данного метода подтверждена во многих проспективных исследованиях.
Критерии индекса MASCC представлены в табл. 3.
Показателем “низкого риска” осложнений является сумма баллов > 21. Частота серьезных осложнений при этом не превышает 6 %, а смертность – 1 %. При сумме баллов < 15 смертность достигает 36 %.
Стандартом лечения ФН является немедленное назначение эмпирической терапии антибиотиками широкого спектра действия. Такая терапия должна быть направлена против грамположительных и грамотрицательных микроорганизмов, обеспечивать быстрое бактерицидное действие и иметь низкую токсичность. При выборе способа введения антибиотиков необходимо руководствоваться следующим принципом: пероральная АБТ может быть безопасно применена пациентами с ФН “низкого риска”. К данной категории больных относятся те, кто гемодинамически стабилен, у кого нет признаков органной недостаточности, длительно стоящего центрального венозного катетера или тяжелой инфекции. Внутривенная АБТ должна проводиться пациентам с ФН “высокого риска”. После 48-часовой внутривенной АБТ больным, не имеющим лихорадки, могут быть назначены пероральные антибиотики [11].
По данным многочисленных исследований показано, что монотерапия фторхинолонами не менее эффективна, чем комбинированное применение фторхинолонов и амоксициллина/клавуланата. Однако данное утверждение не относится к пациентам с “высоким риском” ФН.
Обособленно от стандартной терапии антибиотиками широкого спектра действия стоит большое число клинических ситуаций, когда требуется применение специфических режимов лечения. Так, например, в случае пневмонии необходимо назначать антибактериальные препараты, которые перекрывали бы спектр ати-пичных микроорганизмов (Legionella, Mycoplasma), например макролиды и β-лактамные антибиотики. Высокие дозы ко-тримоксазола – терапия выбора при подозрении на инфекцию, вызванную Pneumocystis jerovecii [12].
Во всех случаях катетерассоциированной инфекции (КАИ) при ФН требуется определиться с выбором и путем введения антибиотиков, необходимостью удаления катетера. Если при подозрении на КАИ состояние пациента стабильное, катетер не следует удалять без микробиологического доказательства наличия инфекции. Рекомендовано назначение гликопептидов (ванкомицина) через катетер. В этом случае перекрывается грамположительная флора [13]. При КАИ, вызванной коагулазонегативным стафилокококком, попытка сохранения катетера может быть оправданной только при условии стабильного состояния пациента. Сохранение катетера в большинстве случаев не влияет на разрешение бактериемии, вызванной коагулазонегативным стафилокококком, но является значимым фактором риска рецидива инфекции [14]. Удаление катетера показано при наличии воспаления в месте стояния катетера или порта, персистирующей лихорадки и бактериемии, сохраняющихся на адекватную АБТ, при наличии атипичной микобактериальной инфекции и кандидемии. При КАИ, вызванной Staphylococcus aureus, рекомендуется удаление катетера [15].
При развитии диареи необходимо проводить исследование на Clostridium dеfficili, а при подозрении на клостридиальную инфекцию – начинать терапию метронидазолом. При вирусной инфекции показан ацикловир. Ганцикловир следует назначать только при высокой степени подозрения на инвазивную цитомегаловирусную инфекцию. В случае развития кандидоза препаратом первой линии явля- ется флуконазол. Противогрибковую терапию следует продолжать до разрешения нейтропении, а больным с доказанной микотической инфекцией – в течение 14 дней.
Терапия при подозрении на инвазивный аспергиллез должна включать каспофунгин, либо липосомальный амфотерицин В, либо вариконазол. Последние два препарата можно комбинировать с эхинокандином в случае отсутствия ответа на терапию [16–18]. При подозрении на менингит показано выполнение люмбальной пункции. При бактериальном менингите следует назначать цефтазидим в сочетании с ампициллином (для прикрытия от Listeria monocytogenes) или меропенем [19].
Если имеются клинические или микробиологические доказательства интраабдоминального или тазового сепсиса, следует начинать терапию метронидазолом. Длительность лечения ФН может быть различной. Если число нейтрофилов повысилось до 0,5 × 109/л и более, в течение 48 часов отмечается нормальная температура тела, посев крови не выявляет возбудителя, АБТ можно прекратить. При количестве нейтрофилов < 0,5 × 109/л, отсутствии осложнений и лихорадки в течение 5–7 дней АБТ также можно завершить. Исключением являются ситуации, когда сохраняется “высокий риск” развития осложнений. В этом случае АБТ продолжается до 10 дней или до тех пор, пока количество нейтрофилов не составит 0,5 × 109/л и более. Больным с сохраняющейся лихорадкой при числе нейтрофилов 0,5 × 109/л и более целесообразно назначfть антимикотическую терапию.
Таким образом, несмотря на значительные успехи в профилактике и лечении ФН, она остается одним из наиболее грозных осложнений ХТ злокачественных опухолей и ведет к изменению сроков применения цитостатиков, редукции доз химиопрепаратов, что отрицательно сказывается на эффективности противоопухолевого лечения. Широкое внедрение в клиническую практику Г-КСФ позволяет значительно уменьшать степень выраженности и длительность нейтропении, снижать риск развития ФН при проведении миелосупрессивной ХТ. Все это позволяет сохранять запланированную дозовую интенсивность режима, а иногда и интенсифицировать режим за счет сокращения интервалов между курсами.
Лечение
Интермиттирующая нейтропения обычно проходит без симптомов и тяжелых инфекционных осложнений, поэтому в терапевтическом лечении не нуждается. Особенно в том случае, если пациент тщательно соблюдает правила личной гигиены, употребляет в пищу продукты, которые прошли термическую обработку (блюда из сырой рыбы, мясо с кровью при нейтропении нельзя), пользуется перчатками во время уборки, защищает кожу от длительного воздействия солнца.
При вторичной нейтропении лечение направлено, в первую очередь, на ликвидацию основного заболевания, которое и повлекло за собой патологическое снижение гранулоцитов.
В «Клинике Спиженко» лечение нейтропении проводится с учетом причины возникновения и клинических симптомов и может включать:
- Антибактериальную терапию.
- Противогрибковую терапию.
- Иммунотерапию.
- Применение глюкокортикоидов.
Включая лечение ассоциированных состояний (язвы, стоматит, гингивит) с помощью полосканий солевым раствором ротовой полости, применения антисептиков (хлоргексидина), нистатина, клотримазола, флуконазола (при кандидозах).
При острых поражениях слизистых, дополнительно назначается диета (с преобладанием в рационе жидкой пищи) и местное обезболивание.Если снижение нейтрофилов произошло в результате приема лекарственных средств, выход из ситуации – прекратить их использование и перейти на альтернативное лечение.
Лекарственные
препараты, что приводят к нейтропении:
- Противосудорожные (Диазепам, Фенитоин, Вальпроат натрия).
- Антидепрессанты (Клозапин, Галоперидол).
- Антибиотики (Доксициклин, Линкомицин, Цефалоспорин, Пенициллин, Ванкомицин).
- Противовирусные (Ацикловир, Зидовудин).
- Антигельминтные (Левомизол, Мебензадол).
- Противотуберкулезные (Стрептомицин, Рифампицин, Изониазид, Этамбутол).
- Противогрибковые (Гризеофульвин, Микозолон, Аморолфин).
Включая анальгетики (Ибупрофен, Индометацин, Амидопирин, Ацетилсалициловая кислота, Фенилбутазон).
Лечение фебрильной нейтропении
Фебрильная нейтропения требует незамедлительного медицинского вмешательства (в течение 1 часа!).
При нейтропенической лихорадке назначается:
- Противомикробная терапия;
- Неотложная диагностика (посев крови, мочи, выделений изо рта, места катетеризации, влагалища/уретры, УЗИ внутренних органов, рентгенография).
Основа современного антибактериального лечения ФН (фебрильной нейтропении) — бета-лактамные антибиотики.
В «Клинике Спиженко» вы сможете пройти комплексное исследование нейтропении, установить точную причину и получить наиболее корректное лечение (при необходимости).
Нейтропения – это не «приговор», но и не повод оставлять данную ситуацию без компетентного медицинского внимания.
Рекомендации
- ^ абcdежграммчасяj
Олс, Робин (2012).
Гематология, иммунология и инфекционная неонатология: вопросы и противоречия
. Филадельфия, Пенсильвания: Эльзевьер / Сондерс. ISBN 978-1-4377-2662-6 : Доступ предоставлен Питтсбургским университетом. - ^ аб
Newburger PE, Дейл, округ Колумбия (июль 2013 г.). «Обследование и ведение пациентов с изолированной нейтропенией».
Семинары по гематологии
.
50
(3): 198–206. Дои:10.1053 / j.seminhateol.2013.06.010. ЧВК 3748385. PMID 23953336. - ^ абc
«Клиническая картина нейтропении: история болезни, физикальное обследование».
emedicine.medscape.com
. Получено 8 декабря 2015. - «Нейтропения». Национальный центр биотехнологии, Национальная медицинская библиотека. Получено 8 декабря 2015.
- «Нейтрофилы». Национальный центр биотехнологии, Национальная медицинская библиотека. Получено 8 декабря 2015.
- ^ абc
Фунг М., Ким Дж., Марти FM, Шварцингер М., Ку С. (2015). «Мета-анализ и сравнение стоимости эмпирических и превентивных противогрибковых стратегий у больных гематологическими злокачественными новообразованиями с фебрильной нейтропенией высокого риска».
PLOS One
.
10
(11): e0140930. Bibcode:2015PLoSO..1040930F. Дои:10.1371 / journal.pone.0140930. ЧВК 4640557. PMID 26554923. - ^ аб
Хорвиц М.С., Кори С.Дж., Граймс Х.Л., Тидвелл Т. (февраль 2013 г.). «Мутации ELANE при циклической и тяжелой врожденной нейтропении: генетика и патофизиология».
Гематологические / онкологические клиники Северной Америки
.
27
(1): 19–41, vii. Дои:10.1016 / j.hoc.2012.10.004. ЧВК 3559001. PMID 23351986. - Боксер Л.А. (8 декабря 2012 г.). «Как подойти к нейтропении». Гематология. Американское общество гематологии. Образовательная программа
.
2012
(1): 174–82. Дои:10.1182 / asheducation.v2012.1.174.3798251. PMID 23233578. - Накаи, Юкиэ; Исихара, Тикако; Огата, Сагири; Шимоно, Цутому (июль 2003 г.). «Устные проявления циклической нейтропении у японского ребенка: история болезни с 5-летним наблюдением». Детская стоматология
.
25
(4): 383–388. ISSN 0164-1263. PMID 13678105. - Хазински, Мэри Фрэн (4 мая 2012 г.). Уход за тяжелобольным ребенком
. Elsevier Health Sciences. п. 835. ISBN 978-0323086035 . - Донадье Дж, Бопен Б., Феннето О, Белланне-Шантело С. (ноябрь 2017 г.). «Врожденная нейтропения в эпоху геномики: классификация, диагностика и естествознание». Британский журнал гематологии
.
179
(4): 557–574. Дои:10.1111 / bjh.14887. PMID 28875503. - Muturi-Kioi V, Lewis D, Launay O, Leroux-Roels G, Anemona A, Loulergue P и др. (4 августа 2021 г.). «Нейтропения как нежелательное явление после вакцинации: результаты рандомизированных клинических испытаний на здоровых взрослых и систематического обзора». PLOS One
.
11
(8): e0157385. Bibcode:2016PLoSO..1157385M. Дои:10.1371 / journal.pone.0157385. ЧВК 4974007. PMID 27490698. - ^ абcdе
Уильямс, Марк (2007).
Комплексная больничная медицина — доказательный подход
. Филадельфия: Сондерс Эльзевьер. ISBN 978-1-4160-0223-9 ; Доступ предоставляется Питтсбургским университетом - Шварцберг Л.С. (1 января 2006 г.). «Нейтропения: этиология и патогенез». Клинический краеугольный камень
. 8 Приложение 5: S5-11. Дои:10.1016 / с1098-3597 (06) 80053-0. PMID 17379162. — через ScienceDirect (Может потребоваться подписка или контент может быть доступен в библиотеках.) - Дейл, округ Колумбия, Болярд А.А. (январь 2021 г.). «Обновленная информация о диагностике и лечении хронической идиопатической нейтропении». Текущее мнение в гематологии
.
24
(1): 46–53. Дои:10.1097 / MOH.0000000000000305. ЧВК 5380401. PMID 27841775. - Макарян В., Розенталь Е.А., Болярд А.А., Келли М.Л., Боул Дж.Э., Бамшад М.Дж. и др. (Июль 2014 г.). «Врожденная нейтропения, связанная с TCIRG1». Человеческая мутация
.
35
(7): 824–7. Дои:10.1002 / humu.22563. ЧВК 4055522. PMID 24753205. - Левен, Малькольм I .; Lewis, S.M .; Bain, Barbara J .; Имельда Бейтс (2001). Практическая гематология Dacie & Lewis
. Лондон: В. Б. Сондерс. п. 586. ISBN 978-0-443-06377-0 . - «Пациенты с нейтропенией и нейтропенические режимы | Пациенты». Пациент
. Получено 8 декабря 2015. - ^ аб
Шей М.М., Эверхарт Дж. Э., Берд-Холт Д. Д., Тисдейл Дж. Ф., Роджерс Г. П. (апрель 2007 г.). «Распространенность нейтропении среди населения США: возраст, пол, статус курения и этнические различия».
Анналы внутренней медицины
.
146
(7): 486–92. Дои:10.7326/0003-4819-146-7-200704030-00004. PMID 17404350. - «Калькулятор абсолютного количества нейтрофилов». reference.medscape.com
. Получено 8 декабря 2015. - Schouten HC (сентябрь 2006 г.). «Управление нейтропенией» (PDF). Анналы онкологии
. 17 Прил. 10 (Прил. 10): x85-9. Дои:10.1093 / annonc / mdl243. PMID 17018758. - Джеймс Р.М., Кинси С.Е. (октябрь 2006 г.). «Исследование и лечение хронической нейтропении у детей». Архив детских болезней
.
91
(10): 852–8. Дои:10.1136 / adc.2006.094706. ЧВК 2066017. PMID 16990357. - Агранулоцитоз — достижения в области исследований и лечения: издание 2012 г.: ScholarlyBrief
. Научные издания. 26 декабря 2012. с. 95. ISBN 9781481602754 . - Jubelirer SJ (6 апреля 2011 г.). «Польза нейтропенической диеты: факт или вымысел?». Онколог
.
16
(5): 704–7. Дои:10.1634 / теонколог.2011-0001. ЧВК 3228185. PMID 21471277. - Йохансен HK, Gøtzsche PC (сентябрь 2014 г.). «Жирорастворимые препараты амфотерицина B по сравнению с амфотерицином B у онкологических больных с нейтропенией». Кокрановская база данных систематических обзоров
(9): CD000969. Дои:10.1002 / 14651858.cd000969.pub2. ЧВК 6457843. PMID 25188673. - Йохансен HK, Gøtzsche PC (сентябрь 2014 г.). «Амфотерицин B по сравнению с флуконазолом для борьбы с грибковыми инфекциями у пациентов с нейтропеническим раком». Кокрановская база данных систематических обзоров
(9): CD000239. Дои:10.1002 / 14651858.cd000239.pub2. ЧВК 6457742. PMID 25188769. - «Нейтропения». eMedicine
. MedScape. Получено 8 декабря 2015. - Андерсен К.Л., Тесфа Д., Сирсма В.Д., Сандхолдт Х., Хассельбалч Х., Бьеррум О.В. и др. (Июнь 2016). «Распространенность и клиническое значение нейтропении, обнаруженные при рутинном общем анализе крови: продольное исследование». Журнал внутренней медицины
.
279
(6): 566–75. Дои:10.1111 / joim.12467. PMID 26791682.