В знаменитом сериале «Доктор Хаус» от хореи Гентингтона страдала героиня Оливии Уайлд. Благодаря фильму об этой болезни узнало больше людей. Но можно ли было вылечить героиню или перспективы у нее не радужные? Обсудим подробнее эту болезнь.
АЛЕНА ПАРЕЦКАЯ
Врач-патофизиолог,иммунолог, членСанкт-Петербургскогообщества патофизиологовВАЛЕНТИНА КУЗЬМИНАК.м.н., врач-невролог «СМ-Клиника»Хорея Гентингтона – это серьезное заболевание, которое поражает молодых людей в возрасте от 20 до 40 лет, встречается с частотой один случай на 10 тысяч населения, приводит к тяжелым последствиям.
Что такое хорея Гентингтона
– По современному определению, болезнь Гентингтона – это хроническое, постепенно прогрессирующее наследственное аутосомно-доминантное заболевание нервной системы, – говорит врач-невролог Валентина Кузьмина. – Болезнь проявляется нарушением речи, расстройствами памяти и присутствием навязчивых вычурных движений (человек принимает нелепые позы, дергается, кривится). Со временем приводит к инвалидности, достаточно молодому человеку нужен постоянный уход и присмотр со стороны окружающих. К сожалению, пока болезнь относится к неизлечимым, хотя попытки ее лечения есть, постоянно тестируются новые методы.
Патогенез
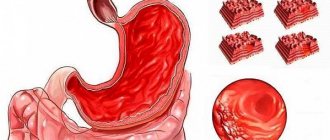
Доказано, что хорея Гентингтона развивается в результате увеличения числа тринуклеотидных повторов — цитозин-аденин-гуанин, расположенных в первом экзоне гена. Триплет цитозин-аденин-гуанин кодирует аминокислоту глутамин, поэтому в белке образуется удлиненный полиглутаминовый тракт. Формируя подобие «замка-застежки», расширенный полиглутаминовый участок белка гентингтина изменяет свою собственную информацию и прочно соединяется с другими белками. В результате происходит агрегация белков, нарушаются межбелковые взаимодействия, что приводит к апоптозу клеток.
Причины хореи Гентингтона у взрослых
Это патология, которая наследуется от родителей, если они передают ребенку дефектные гены, причем, сами они не болеют.
Врач-невролог Валентина Кузьмина поясняет: болезнь Гентингтона наследуется по аутосомно-доминантному типу, то есть, даже если ребенок унаследовал один ген, он проявит себя и даст начало болезни. Распространенность этой болезни составляет 4 — 8 случаев на 100 000 населения. Причина в том, что генетический дефект при болезни Гентингтона преждевременно вызывает гибель определенных популяций нейронов экстрапирамидной путей ЦНС.
Из-за дефекта в генах нервная система становится очень хрупкой, ранимой, ее клетки достигая определенного возраста, начинают отмирать и не восстанавливаются. Особенно страдает экстрапирамидная система, которая отвечает за наши произвольные и непроизвольные движения, помогает нам держать позу, координировать свои действия, регулировать тонус мышц.
Модели для изучения болезни Хантингтона
Модели БХ на животных появились более 30 лет назад. Первыми были модели, основанные на введении в стриатум нейротоксических веществ (например, хинолиновой кислоты — агониста NMDA-рецепторов), которые вызывали гибель нейронов. В настоящее время большинство исследователей работает на моделях трансгенных животных, среди которых есть не только мыши и крысы, но и беспозвоночные животные — мушка Drosophila melanogaster и червь Caenorhabditis elegans.
Мышиные модели болезни Хантингтона отличаются друг от друга количеством CAG-повторов и уровнем экспрессии трансгена — искусственно внесенного гена хантингтина. Т.к. именно от этих факторов зависит развитие БХ, разные линии мышей отличаются друг от друга скоростью развития патологий. К наиболее широко используемым моделям относят линии мышей R6/2, R6/1 и YAC128, которые были использованы и в нашей работе. У мышей этих линий симптомы заболевания наиболее выражены и проявляются достаточно быстро. Кроме того, у этих животных с возрастом прогрессируют когнитивные и моторные нарушения, развивается частичная потеря нейронов в стриатуме и коре.
Еще одним из способов моделирования БХ является использование клеточной культуры. В самом простом случае используются культуры клеток со стабильной трансфекцией гена хантингтина. Например, это клетки линии PC12, содержащие индуцибельный трансген первого экзона хантингтина или нейроны стриатума с экспрессией фрагментов хантингтина разной длины. Кроме того, можно использовать первичные культуры из нейронов трансгенных мышей или иммортализованные нейроны.
Признаки хореи Гентингтона у взрослых
– Болезнь обычно проявляется на 3 — 5-ом десятилетии жизни, – уточняет врач-невролог Валентина Кузьмина. – Изначально она дает о себе знать едва заметными признаками, но постепенно проявляется в виде генерализованного хореического гиперкинеза, а именно:
- присутствием навязчивых вычурных движений;
- нарушением речи;
- нарушением памяти;
- эмоционально-личностными расстройствами.
Хорея обычно начинается с лица или дистальных отделов конечностей (пальцы рук либо ног), затем постепенно распространяется и нарушает произвольные движения. Больные не могут долго держать высунутым язык или сжимать кисть в кулаке. Походка становится неустойчивой, «танцующей», замедленной и напряженной. Речь – сложной для понимания, нечеткой, смазанной.
Позднее развивается дисфагия (нарушение глотания пищи и воды), что является причиной аспирации (поперхивание и попадание пищи в бронхи), ведущей к удушью и пневмонии. Также появляется недержание мочи.
Способность гена проявлять себя близка к 100% – к 70 годам болезнь проявляется практически у всех его носителей. Такие пациенты получают инвалидность.
Оптогенетика
Оптогенетика — метод, объединяющий подходы генетики и оптики для тонкого контроля электрической активности электровозбудимых клеток (нейронов и мышечных волокон) [9]. Для этого в изучаемые клетки вводят гены специальных светочувствительных белков — микробных опсинов, которые являются ионными каналами или насосами (рис. 7). Первая работа, показавшая возможность управлять электрической активностью нейронов при использовании опсина, была опубликована в 2005 году. За последующие несколько лет появился еще ряд экспериментальных работ, позволивших доработать эту методику и доказать ее применимость в различных экспериментальных условиях.
За последние годы было открыто множество различных опсинов, из которых наибольшее применение в оптогенетике нашли галородопсины и каналородопсины. При доставке гена опсина с помощью методов генной инженерии в нейрон, на плазматической мембране появляются светочувствительные каналы, а сама клетка становится светочувствительной. При действии синего света открывается пора каналородопсина (максимум поглощения — 470 нм), который вызывает движение положительно заряженных ионов внутрь клетки, обеспечивая деполяризацию мембраны нейрона и генерацию потенциалов действия. При действии желтого света активируется галородопсин (максимум поглощения — 580 нм), мембрана нейрона гиперполяризуется, вызывая торможение нейрона. Высокое временное разрешение метода оптогенетики позволяет обеспечить очень тонкую регуляцию синаптических событий и является, таким образом, важным инструментом для изучения межнейронных связей.
Совместное применение оптогенетики и классических методов электрофизиологии позволяет извлечь выгоду из положительных качеств каждого из этих подходов. Точность электрофизиологической регистрации объединяется с возможностью использовать световые стимулы разной длительности и интенсивности, что помогает ученым подробно изучать работу нейронных связей.
Электрическая активность нейронов выражается в резких скачках напряжения на клеточной мембране и появлении вследствие этого электрического тока. Эти резкие скачки называются спайками или потенциалами действия и длятся несколько миллисекунд (рис. 8). Мы выяснили, что чем дольше нейрон освещается синим светом, тем больше спайков он за это время создает. Если освещаемый нейрон связан синаптическим контактом с другим нейроном, то на втором нейроне можно зарегистрировать ответную активность — тоже в виде отдельных спайков.
Рисунок 8. Пример записи, получаемой при электрофизологической регистрации активности нейрона. Спайки (потенциалы действия) отражаются на записи в виде вертикальных линий, показывающих резкие скачки мембранного тока.
В наших экспериментах мы использовали пару молодых (14 дней) нейронов коры и стриатума, связанных синаптическим контактом. Нейрон коры активировали синим светом, а на нейроне стриатума производили регистрацию ответной активности. Оказалось, что для возникновения ответа на нейроне стриатума нужна определенная длительность освещения (порог активации). Если длительность освещения была ниже порогового значения, то спайк на нейроне стриатума возникал в ответ не на каждую вспышку света. И что самое важное: порог активации для нейронов из мозга здоровых мышей отличался от мышей YAC128 (с мутацией в гене хантингтина). Наиболее ярко эта разница была видна при 50%-активации нейрона стриатума, т.е. длительности освещения, при которой спайк возникает в ответ на каждую вторую вспышку света. Порог 50%-активации нейрона стриатума в ответ на облучение кортикального нейрона для культуры клеток YAC 128 был примерно в два раза (точнее в 2,3±0,8) выше по сравнению с положительным контролем [10].
Получается, что мутация в белке хантингтине приводит к тому, что синаптическая передача ухудшается уже в молодых нейронах, и при этом нарушения происходят на функциональном уровне (без морфологических изменений). Может ли быть так, что именно эти функциональные нарушения в дальнейшем приводят к появлению морфологических изменений, таких как исчезновение шипиков у старых нейронов стриатума?
Чтобы ответить на этот вопрос, мы снова обратились за помощью к оптогенетике, но теперь с ее помощью мы подавляли светом активность нейронов (рис. 9а). Если наше предположение верно, то временное отсутствие активирующего воздействия коры должно привести к исчезновению шипиков на нейронах стриатума в культуре YAC128. Действительно, после эксперимента количество шипиков в положительном контроле осталось неизменным, но в культуре YAC128 значительно снизилось (рис. 9б, в). Получается, что моделирующие БХ нейроны особенно чувствительны к ослаблению активирующего воздействия нейронов коры, поэтому длительное ослабление синаптической связи между этими нейронами приводит к уменьшению количества шипиков на 20 день культивирования [10].
Рисунок 9. Влияние на нейроны с помощью оптогенетики. а — подавление активности нейрона коры с помощью оптогенетики. При освещении нейрона желтым светом (оранжевая полоса) он становится неактивен — на электрофизиологической записи в этот промежуток времени почти нет спайков. б — влияние длительного оптогенетического торможения на морфологию нейронов. На микрофотографиях видно уменьшение количества шипиков на дендрите нейрона YAC128. в — изменение плотности дендритных шипиков после оптогенетического торможения. В культуре дикого типа количество шипиков не изменяется, а в культуре YAC128 плотность шипиков значительно снижается.
Таким образом, мы обнаружили, что в нашей модели БХ наблюдается нарушение синаптической передачи, которое развивается в два этапа. На ранней стадии (молодые нейроны, на 14 день культивирования нейронов) происходит функциональное ослабление сипаптической связи, которое на более поздней стадии (старые нейроны, на 20 день культивирования) приводит к морфологическим нарушениям синаптических контактов.
Современные методы лечения
– Лечение болезни Гентингтона, – объясняет врач-невролог Валентина Кузьмина, – исключительно симптоматическое. Для уменьшения гиперкинеза используют нейролептики, миоспазмолитики как в таблетках, так и инъекционные. Для уменьшения акинетико-ригидной формы проявления болезни используют антипаркинсонические средства.
При депрессии, соответственно, назначают трициклические антидепрессанты, селективные ингибиторы обратного захвата серотонина. При вспышках агрессии – нейролептики. Реабилитация поможет расширить функциональные способности больных.
Улучшить функциональные возможности и социальную адаптацию таких пациентов – это приоритетная задача врача.
Вывод: нарушение синаптической передачи и нейродегенеративные заболевания
Исследование подтвердило нашу первоначальную догадку: нарушение работы стриатума при БХ связано, прежде всего, с нарушением синаптической передачи. Нейроны стриатума перестают «слышать» команды нейронов коры, и, в результате, человек начинает терять контроль над своими движениями. Но на ранней стадии заболевания эти нарушения носят функциональный характер и, вероятно, обратимы. Если выяснить причины, ведущие к нарушению работы синапсов, то возможно разработать лекарственное средство, которое поможет остановить патологические изменения, обеспечит нейронам стриатума необходимый уровень активации и, таким образом, предотвратит развитие необратимых морфологических нарушений.
Результаты этой работы подталкивают и к другому важному заключению: при изучении нейродегенеративных заболеваний ученым следует обратить больше внимания на синаптическую передачу и взаимодействие нейронов. Мы знаем достаточно много о том, как влияет накопление амилоидных агрегатов при болезни Альцгеймера на жизнедеятельность клетки, и какие нейроны погибают при развитии болезни Паркинсона, но это все еще не привело к появлению эффективной терапии. Возможная причина этих неудач — мы не учитываем последствия нарушения синаптических связей — те, которые мы открыли при исследовании болезни Хантингтона. Хочется надеяться, что наши находки подскажут исследователям направление для разработки эффективных способов лечения болезни Хантингтона, и Тринадцатая наконец-то будет здоровой!
Исследование было проведено в лаборатории молекулярной нейродегенерации СПбГПУ (зав. лаб. — проф. Техасского университета Илья Борисович Безпрозванный) под руководством к.б.н. Дмитрия Николаевича Артамонова.
Профилактика хореи Гентингтона у взрослого в домашних условиях
– В настоящее время, – говорит врач-невролог Валентина Кузьмина, – применима реабилитация с использованием комплексной программы лечебных мероприятий с обучением родственников командой специалистов: врачом ЛФК, врачом физиотерапевтом, логопедом, клиническим психологом и врачом-неврологом.
Так как хорея Гентингтона – это наследственное заболевания, в качестве профилактики можно предложить проведение пренатальной диагностики или доимплантационного генетического тестирования эмбрионов (ПГТ-М), то есть, медико-генетическое консультирование семьи.
Основы диагностики
Диагностика проводится с использованием методов физикального осмотра и психологического обследования, которые помогают установить основные признаки заболевания и оценить степень распространения заболевания. *МРТ снимок (слева — болеющий хореей Хантингтона, справа — здоровый человек)
Из инструментальных методов диагностики основное место занимает компьютерная и магнитно-резонансная томография, которые визуализируют место повреждения головного мозга. Так результаты КТ или МРТ показывают зону атрофии или глиоза в области полосатого тела.
С помощью магнитно-резонансной спектроскопии можно определить еще один диагностический признак – увеличение уровня лактата в ткани базальных ядер.
Из скрининговых методов «золотым стандартом» является генетическое тестирование, которое основано на выявлении увеличенного числа тринуклеотидных остатков ЦАГ в гене HD. В случае, когда их количество составляет 38 и более, заболевание со временем возникнет в 100%. При этом существует закономерность, что чем больше количество остатков, тем в более раннем возрасте проявится хорея.
Эпидемиология
Синдрому Хантингтона Больше всего подвержены европейцы, а среди них — американцы. В сравнении: часто заболевания среди европейцев составляет 10 случаев на 100000 человек, а среди прочих рас, всех вместе взятых: один случай на 100000 человек. В США данной болезнью страдает более 7000 человек. Хорея Хантингтона встречается как у женщин, так и у мужчин. Однако в процентном соотношении, у сильного пола она встречается намного чаще. Заболевание генетическое и передаётся по наследству примерно в половине случаев. При чём, от больного отца риск рождения ребёнка с болезнь Хантингтона гораздо выше, чем от больной матери. Кроме того, у ребёнка, который унаследовал заболевание по отцовской линии, наблюдается наиболее значительное увеличение тринуклеотидных повторов и течение болезни, как правило носит ювенильную форму. Причина более выраженной наследственности от отца неизвестна.
Список источников
- Шток В. Н., Иванова-Смоленская И. А., Левин О. С. Экстрапирамидные расстройства: Руководство по диагностике и лечению. — М.: Медпресс информ, 2002. — 700 с.
- Шток В. Н., Левин О. С. Лекарственные экстрапирамидные расстройства //В мире лекарств. — 2000. — № 2. — С. 3-7.
- Селивёрстов Ю.А. и др. // Нервные болезни. 2014. № 3. С. 24.
- Тюрин Н.А., Артамонова В.А., Александрова К.А. и др. Особенности современного течения малой хореи у детей. Педиатрия. 1987; 2: 20–23.
- Детская ревматология (Руководство для врачей) / Под ред. Баранова А.А., Баженовой Л.К., 2002; 49.