Подкожная эмфизема – причины, симптомы, лечение пузырьков воздуха под кожей
Содержание
скрыть
1 Подкожная эмфизема – причины, симптомы, лечение пузырьков воздуха под кожей
2 Что такое эмфизема?
3 Каковы причины подкожного пневмоторакса?
4 Симптомы подкожного пневмоторакса – как распознать воздух под кожей?
5 Лечение пневмоторакса – как избавиться от пузырьков воздуха? 5.1 Похожие записи:
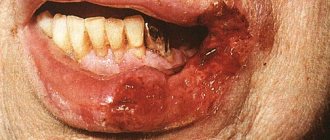
Подкожная эмфизема – это состояние, при котором под кожей видны пузырьки воздуха. Обычно подкожная эмфизема располагается на груди, шее или лице. Причина – травмы в этих областях, медицинские процедуры (например, после лапароскопии, трахеотомии) или стоматологические процедуры (например, после удаления зуба). Симптомы пневмоторакса включают боль и чувство распирания в шее и затрудненное дыхание. Лечение подкожного пневмоторакса обычно не требуется, так как воздух самовсасывается.
Fotolia
Что такое эмфизема?
Подкожная эмфизема – это наличие воздуха в подкожной клетчатке. Причин его возникновения много. Он часто сосуществует с пневмотораксом средостения (воздух в средостении) или пневмотораксом (воздух в плевральной полости), откуда воздух проходит под кожей шеи.
Наиболее важные причины подкожного пневмоторакса :
- перфорация желудочно-кишечного тракта,
- травма груди,
- травма структур дыхательных путей (гортани, трахеи, бронхов),
- осложнение медицинских процедур,
- инфекция мягких тканей (газовая гангрена).
Подкожный пневмоторакс у новорожденных , напротив , может возникнуть после тяжелых родов.
Каковы причины подкожного пневмоторакса?
Подкожная эмфизема может возникнуть в результате травмы грудной клетки, например, во время дорожно-транспортного происшествия. При этом часто повреждаются стенки клетки (ребра) и паренхима легкого. Травма вызывает попадание воздуха в плевральную полость или средостение. Отсюда воздух в поисках выхода проникает в мягкие ткани, вызывая гиподерму на шее и отек лица .
Причиной подкожного пневмоторакса также может быть перелом ребер, вызванный травмой или интенсивным продолжительным кашлем (например, во время приступа астмы). По статистике каждый четвертый пациент с переломом ребра страдает коморбидной гиподермией.
Про
Диагностика
Диагностические мероприятия осуществляет врач-пульмонолог. При травматическом генезе симптома требуется участие травматолога, при поражениях лица необходима консультация челюстно-лицевого хирурга. Во время сбора анамнеза специалист выясняет, что происходило в период, предшествующий формированию эмфиземы, выявляет другие жалобы, оценивает динамику развития заболевания. Проводят следующие процедуры:
- Внешний осмотр
. О наличии подкожного скопления воздуха свидетельствует неравномерное увеличение объема мягких тканей, иногда создающее впечатление «раздутости». Ощупывание безболезненно, пальпаторно определяется нежный хруст. Возможны отставание половины грудной клетки в акте дыхания, расширение подкожных вен, вынужденное положение больного. - Рентгенография
. При патологиях ОГК обязательно делают обзорный снимок, опционально – прицельный. Возможно обнаружение переломов ребер, гемо- и пневмоторакса, пневмомедиастинума. При травмах лица выполняют рентгенограммы орбиты, костей носа, скуловой кости. Иногда требуется рентгенография черепа для исключения переломов его мозговой части. - Компьютерная томография
. КТ ОГК производится для уточнения характера повреждений, выявления ателектазов, пневмо- и гемоторакса, других патологий, выполняется нативно или с контрастом. Пациентам также могут быть показаны КТ легких или КТ средостения. Для детализации изменений, обнаруженных на рентгенограммах костей лица, могут быть назначены КТ орбиты и другие исследования. - Магнитно-резонансная томография
. МРТ легких информативна при разграничении воспалительных и невоспалительных поражений, изучении легочной ткани, сосудистых структур, лимфатической системы и скоплений жидкости. Выполняется на заключительном этапе обследования в рамках дифференциальной диагностики, планирования торакальных вмешательств. - Эндоскопические методы
. Подозрение на перфорацию пищевода является показанием к эзофагоскопии. Трахеобронхоскопию осуществляют при перфорации трахеи, бронхиальных свищах, других патологиях. В некоторых случаях для уточнения диагноза и проведения лечебных мероприятий необходима торакоскопия. - Другие методики
. Сцинтиграфия рекомендована для оценки капиллярного кровотока и легочной вентиляции, применяется при ателектазах, пневмонии, обструктивных патологиях. Плевральная пункция позволяет установить характер и количество экссудата при плевритах, гемотораксе и гидротораксе.
Подкожная эмфизема на рентгене
Симптомы подкожного пневмоторакса – как распознать воздух под кожей?
Больные пневмотораксом жалуются на ощущение пузырьков воздуха под кожей . Ощущение сильного дискомфорта в области шеи и груди. Дополнительно могут быть:
- проблемы с дыханием,
- трудности с глотанием и речью
- изменение тембра голоса,
- ощущение распирания в шее.
Больные жалуются на боль в горле, хрипы или боль в шее . Ткани вокруг пневмоторакса могут быть немного опухшими. При осмотре скрип кожи при прикосновении характерен для подкожного пневмоторакса .
Про
Эмфизема средостения, или пневмомедиастинум, — это патологическое состояние, заключающееся в инфильтрации воздухом клетчатки средостения [4].
Считается, что спонтанная эмфизема средостения (СЭС) — редкое, самостоятельное заболевание, характеризующееся доброкачественным течением и возникающее без определенных причин, оно поражает в основном мужчин молодого возраста [9, 19, 23, 36].
Первое упоминание о СЭС датировано 1617 г., когда акушерка королевы Франции Louise Bourgeois в своих воспоминаниях описала внезапно возникшую у нее при родах одутловатость шеи [12]. Данное патологическое состояние впервые описал Rene Laennec в 1819 г. в трактате «О выслушивании стетоскопом» [24]. О СЭС как о самостоятельном заболевании первым сообщил Louis Hamman [5, 10, 19, 23, 25] в 1939 г. Он описал грубую крепитацию, синхронную с сердечными сокращениями, которая аускультативно выслушивается вдоль левого края грудины в третьем-шестом межреберьях, не исключая и другие зоны, в положении сидя. Этот клинический симптом получил название симптома Хэммана.
Патофизиологию данного заболевания на основании экспериментов на лабораторных животных описали в 1944 г. M. Macklin и С. Macklin [5, 10, 23, 25]. В эксперименте на животных они показали, что СЭС возникает в результате резкого понижения градиента давления между альвеолами и межуточной тканью легких, что приводит к разрыву альвеол. Описанный механизм в сочетании с патологическими изменениями альвеоляро-капиллярной мембраны и/или интерстициальной ткани легких может привести к прорыву альвеолы в межуточное пространство [31]. Прорыв альвеолы в легочный интерстиций ведет к накоплению в нем воздуха, который распространяется вдоль градиента давления, периваскулярно и перибронхиально, центростремительно к воротам легких, а затем в средостение (эффект Macklin) [20]. Это происходит потому, что давление в средостении ниже, чем на периферии легких. Большинство авторов сходятся во мнении, что заболевание возникает в результате разрыва терминальных альвеол, расположенных в корне сегмента (доли) легкого и прилежащих к рыхлой клетчатке, окружающей сосуды и бронхи [5, 16, 23]. Оказавшись в средостении, воздух может распространяться на клетчаточные пространства шеи, мягких тканей грудной клетки, в полость сердечной сорочки и даже (в зависимости от количества) в забрюшинное клетчаточное пространство [8].
Частота СЭС у госпитализированных больных варьирует, по различным данным, от 1:3578 [16] до 1:44 511[25].
Существуют разные триггерные механизмы или факторы, способствующие возникновению СЭС. I. Macia и соавт. [25] считают целесообразным разделять эти факторы на: предрасполагающие — вредные привычки и/или заболевания в анамнезе, которые создают благоприятные для развития заболевания условия, и провоцирующие — состояния, которые непосредственно предшествуют возникновению СЭС.
К предрасполагающим факторам многие авторы относят такие легочные заболевания, как бронхиальная астма [5, 9, 16, 19, 25, 29], воспалительные заболевания верхних дыхательных путей [5, 19], идиопатические фиброзирующие заболевания легких [9], хронические обструктивные заболевания легких [9]. Из перечисленных выше заболеваний, согласно публикациям в мировой литературе, только бронхиальная астма рассматривается как предрасполагающий фактор в развитии СЭС практически всеми авторами [5, 9, 16, 19, 25, 29, 35, 36]. J. Chapdelaine и соавт. [11] установили это заболевание в анамнезе почти у 50% больных, A. Newcomb и C. Clarke [29] — у 39% пациентов с СЭС. Нужно отметить, что в мировой литературе авторы редко связывают развитие СЭС с буллезной эмфиземой легких. А.Г. Высоцкий [2] описал 4 наблюдения пневмомедиастинума как осложнения локальной буллезной эмфиземы легких. И.И. Платов и В.С. Моисеев [4] считают, что развитие СЭС связано с теми же причинами, которые приводят к развитию спонтанного пневмоторакса, а именно с буллезной болезнью, кистозными образованиями легких врожденного генеза, респираторными воспалительными заболеваниями.
Некоторые авторы полагают, что курение является предрасполагающим фактором в развитии заболевания [9, 25]. J. Macia и соавт. [25] сравнили количество курильщиков, больных СЭС, с количеством курильщиков среди населения Каталонии (Испания), что составило 34,1 и 37,5%, соответственно. I. Abolnik и соавт. [6] отметили, что количество курильщиков среди больных СЭС незначительно отличалось от таковых в общей популяции.
Описано много провоцирующих факторов, которые непосредственно могут вызвать развитие заболевания. Следует выделить пробу Вальсальвы, интенсивный кашель, чихание, сильную рвоту, истерический крик, роды, акт дефекации, физическую нагрузку, бронхоспазм, спирометрию, игру на духовых инструментах, надувание шаров, употребление ингаляционных наркотических веществ [1, 5, 9, 10, 18, 23, 25, 26, 28, 32].
В сообщении М. Caceres и соавт. [9] доминирующим среди провоцирующих факторов была рвота, которая предшествовала началу заболевания в 36% наблюдений, на втором месте по частоте был приступ бронхиальной астмы, это состояние отмечалось у 21% больных. Кашель также является одним из частых триггерных факторов, и по разным данным, предшествует СЭС в 7,3% [25] и в 40% наблюдений [28]. Описано также возникновение СЭС на фоне диабетического кетоацидоза [36], химиотерапии [34], болезни Ходжкина [21].
Однако не всегда удается выявить предрасполагающие и/или провоцирующие факторы, СЭС нередко возникает в покое [9].
О разнообразии симптомов клинической манифестации СЭС сообщалось многими авторами [25, 36]. Чаще всего отмечается триада клинических симптомов — загрудинная боль (являющаяся самым частым и постоянным симптомом), затруднение дыхания, одутловатость шеи [1, 5, 15, 16, 19, 25, 29, 35, 36]. I. Abolnik и соавт. [6] отмечали наличие боли за грудиной у 88% больных СЭС, I. Macia и соавт. [25] — у 85%, M. Gerazounis и соавт. [16] — у 72,7%, G. Koullias и соавт. [23] — у 66,6%, M. Caceres и соавт. [9] — у 54% больных. Пациент также может предъявлять жалобы на боль в горле, спине, плече, пояснице, слабость, дисфагию, одинофагию, ринофонию, изменение тембра голоса. Некоторые авторы к симптомам заболевания относят и кашель, хотя он еще является и провоцирующим возникновение СЭС фактором [23]. М. Caceres и соавт. и G. Koullias и соавт. выделяли кашель как один из симптомов заболевания, он отмечался в 41 и 32% собственных наблюдений СЭС и являлся соответственно вторым и третьим по частоте симптомом после загрудинной боли [9, 23].
Из клинических симптомов заболевания, выявляемых при физикальном обследовании, чаще всего отмечается подкожная эмфизема мягких тканей шеи и/или груди [1, 2, 5, 7, 16, 25, 36]. В зависимости от количества воздуха, поступившего в клетчатку средостения, эмфизема мягких тканей может распространяться на область лица и нижних отделов грудной клетки, но это бывает редко [5]. В сообщении I. Macia и соавт. [25] у 95% пациентов с СЭС при пальпации определялась подкожная эмфизема мягких тканей, у 66% — шеи и у 29% больных — грудной стенки. J. Jougon и соавт. [19] констатировали наличие этого симптома у 100% больных СЭС. M. Gerazounis и соавт. [16] описали наличие ринофонии (гнусавости) у 5 пациентов, которая отмечалась совместно с эмфиземой мягких тканей шеи и развивалась вследствие диссекции воздухом тканей ретрофарингеального клетчаточного пространства. Этот симптом довольно редкий, но встречаются наблюдения, в которых он служит первым проявлением СЭС и основным клиническим симптомом заболевания [17].
Симптом Хэммана нельзя назвать специфичным для СЭС, так как, по утверждению Ю.В. Халева [5], подобная крепитация может выслушиваться и при левостороннем пневмотораксе без медиастинальной эмфиземы, а также при буллезной эмфиземе язычковых сегментов, пневмоперитонеуме с высоким стоянием диафрагмы, расширении желудка. Распространенность симптома Хэммана у больных СЭС, по данным разных источников, варьирует от 0 до 56% [6, 9, 10, 15, 23, 25, 29, 36].
При пневмомедиастинуме у больных также могут иметь место уменьшение сердечной тупости, глухость сердечных тонов при аускультации. I. Abolnik и соавт. [6] у 2 больных СЭС отмечали наличие парадоксального пульса. У большинства больных может быть один или несколько симптомов, но иногда при объективном исследовании не удается выявить ни одного симптома [5].
Основными методами диагностики СЭС являются рентгенография груди в прямой и боковых проекциях, КТ груди и рентгеноконтрастное исследование пищевода.
A. Yellin и соавт. [36] указали на необходимость выполнения рентгенографии (как рутинного метода первичной диагностики) всем пациентам молодого возраста с болью в груди неясного генеза и затруднением дыхания. По данным многих авторов, этот метод исследования оказался информативным у абсолютного большинства больных СЭС [6, 16, 23, 36], при этом они подчеркивают необходимость выполнения исследования в двух проекциях — прямой и боковой, потому что при небольшом скоплении газа в средостении при обзорной рентгенографии груди в прямой проекции пневмомедиастинум может быть не выявлен [23, 25].
При возникновении пневмомедиастинума на рентгеновском снимке обнаруживаются полосы просветления или пузырьки газа, окружающие органы средостения, приподнимающие медиастинальную плевру и часто распространяющиеся на шею и/или грудную стенку [14].
S. Bejvan и J. Godwin [8] сообщают, что при рентгенографии в прямой проекции свободный газ в средостении часто выявляется по левому контуру сердца и покрывает внутреннюю поверхность медиастинальной плевры, создавая хорошо заметную плевральную линию латеральнее легочного ствола и дуги аорты. На рентгенограммах в боковой проекции свободный газ образует линии просветления вдоль контуров восходящей аорты, дуги аорты и ее ветвей, легочных артерий и трахеи с главными бронхами [8]. Газ также локализуется вдоль линии прикрепления диафрагмы к грудине, вдоль вилочковой железы и плечеголовных вен [13].
Полипозиционная рентгенография — основной и очень эффективный метод исследования при данном заболевании, но если имеется инфильтрация газом мягких тканей грудной стенки, то его информативность сводится практически к нулю. В таких ситуациях, а также в случае настороженности по отношению к заболеваниям с похожей клинической картиной и при необходимости установления причины заболевания, если рентгенологический метод недостаточен, целесообразно выполнение КТ груди [30]. T. Kaneki и соавт. [20] отметили, что у 30% пациентов с СЭС при рентгенографии не удалось выявить пневмомедиастинум, окончательный диагноз был установлен при КТ груди. G. Koullias и соавт. [23] выполняли КТ после первичного рентгенологического исследования всем 25 больным, хотя и считали рентгенографию «золотым стандартом» диагностики СЭС, так как оба этих диагностических метода в 100% наблюдений оказались информативными в отношении пневмомедиастинума. КТ, несомненно, наиболее эффективный метод диагностики пневмомедиастинума [20], так как с его помощью легко выявляется наличие газа в средостении и при поперечных сечениях хорошо определяется его анатомическая локализация. Однако следует отметить, что по простоте выполнения и лучевой нагрузке на пациента этот метод проигрывает рентгенографии, также не стоит забывать об экономическом аспекте. A. Newcomb и C. Clarke [29] считают, что если пневмомедиастинум определяется с помощью рентгенографии и нет подозрения на присутствие какого-либо грозного заболевания как причины этого патологического состояния, то можно ограничиться только этим методом диагностики.
В некоторых наблюдениях СЭС, приведенных в мировой литературе, выполнялось рентгеноконтрастное исследование пищевода. Этот дополнительный метод диагностики применялся в тех ситуациях, когда необходимо было исключить наличие такого опасного состояния, как разрыв пищевода. Используется водорастворимый контрастный препарат и/или взвесь бария сульфата [15, 16, 19, 36]. D. Weissberg [35] пользовался этим методом исследования с целью исключения разрыва пищевода, если возникновению СЭС предшествовала рвота.
В число дополнительных методов исследования при данном заболевании входят эзофагоскопия, бронхоскопия и электрокардиография. Эти методы являются вспомогательными и применяются для подтверждения диагноза СЭС в сомнительных ситуациях.
Дифференциальная диагностика СЭС проводится с заболеваниями сердечно-сосудистой (острый коронарный синдром, перикардит), дыхательной (спонтанный пневмоторакс, эмболия легочной артерии, перфорация трахеобронхеального дерева) и пищеварительной (спонтанный разрыв пищевода) систем [32].
По мнению зарубежных авторов [15, 25, 29, 35, 36] оптимальные сроки стационарного наблюдения и лечения больных СЭС составляют от 2 до 5 дней.
СЭС хорошо поддается консервативному лечению, которое включает постельный режим, обезболивание и оксигенотерапию [6, 9, 15, 23, 29]. При этом наблюдается довольно быстрая регрессия симптомов и в большинстве наблюдений происходит полное разрешение пневмомедиастинума к 8-м суткам [29, 36]. Обычно вскоре после прорыва альвеол в легочный интерстиций они спадаются, так как давление в них снижается и прекращается поступление воздуха [19]. G. Koullias и соавт. [23] всем пациентам проводили антибактериальную профилактику медиастинита. Они использовали третье поколение цефалоспоринов с добавлением к терапии клиндамицина при подозрениях на перфорацию пищевода и когда заболевание сопровождалось повышением температуры тела и лейкоцитозом. Очень редко эмфизема клетчатки шеи, грудной и брюшной стенок, лица прогрессирует и развивается напряженный пневмомедиастинум. Средостение при этом, по выражению Зауербруха, «раздувается как шар», тонкостенные магистральные вены средостения сдавливаются с падением сердечной деятельности, нарушением дыхания и возможным смертельным исходом [3]. В таких ситуациях показана верхняя медиастинотомия по Tiegel с туннелизацией претрахеальной клетчатки до уровня бифуркации трахеи с дренированием средостения и последующей аспирацией, что обеспечивает декомпрессию средостения [4]. J. Moore и соавт. [27] у детей грудного возраста с напряженной эмфиземой средостения выполняли дренирование средостения через субксифоидный доступ. Для декомпрессии мягких тканей и средостения при данном осложнении некоторые авторы предлагают супрастернальную пункцию средостения и стернотомию [33], пункцию надключичных областей [6] и трахеостомию [22]. Если, несмотря на эти меры, наблюдается нарастание напряженной эмфиземы средостения, требуется срочная чресплевральная широкая медиастинотомия [4].
Описаны единичные наблюдения рецидива СЭС [16, 25]. Первыми в литературе рецидив заболевания описали A. Yellin и соавт. [36], они наблюдали пациентов в течение 52 мес после выписки из стационара, повторное возникновение эмфиземы средостения у одного пациента произошло через 14 мес после первого эпизода без предрасполагающих причин.
Таким образом, спонтанная эмфизема средостения является заболеванием, поражающим чаще молодых мужчин трудоспособного возраста. Ее возникновение требует дифференциальной диагностики с рядом серьезных патологических состояний. В редких ситуациях напряженная эмфизема средостения может привести к гемодинамическим и дыхательным нарушениям.
Лечение пневмоторакса – как избавиться от пузырьков воздуха?
Подкожная эмфизема подозревается у пациентов с характерным анамнезом (например, после травмы грудной клетки, медицинских процедур) и типичным потрескиванием подкожной клетчатки. Кроме того, диагноз ставится после рентгена, который показывает наличие воздуха под кожей . Часто пациенты сопровождаются рентгенологическими признаками пневмоторакса , пневмонии средостения или перфорации пищевода.
Течение пневмоторакса обычно легкое. В большинстве случаев в лечении подкожного пневмоторакса нет необходимости , и остаточный воздух со временем абсорбируется спонтанно. Если объем воздуха под кожей велик и приводит к массивному пневмотораксу, вызывающему сильный дискомфорт у пациента, врач может принять решение о его дренировании.
Если причиной пневмоторакса является перфорация пищевода или разрыв и повреждение дыхательных путей, требуется быстрое хирургическое вмешательство. Пациентам с подкожной эмфиземой следует отдых и при необходимости принимать обезболивающие.
Воробьева Марина
Невролог высшей квалификационной категории (стаж работы 14 лет), врач нейрофункциональной диагностики (стаж работы 12 лет); автор научных публикаций по вертеброневрологии; участникнаучных конференций по неврологии и функциональной диагностике всероссийского и международного значения.
Как лечить буллы в легких
Пациенту необходимо отказаться от курения и оставить работу на вредной производственной деятельности, иначе все лечебные мероприятия будут бессмысленны. В неосложненных случаях и на ранних стадиях эмфиземы (или буллезной болезни) лечение консервативное, комбинированное. Терапия назначается врачом-пульмонологом и может включать:
- Медикаменты (диуретики, бронхолитики, гормональные препараты);
- Особый курс ЛФК и дыхательной гимнастики;
- Регулярную кислородотерапия с применением кислородного концентратора.
- Регулярные диагностические мероприятия (КТ легких, спирометрия, консультация пульмонолога).
Положительным аспектом является то обстоятельство, что полный и пожизненный отказ от курения у большинства пациентов приостанавливает развитие буллезной эмфиземы, а применение кислородотерапии у серьезно больных пациентов может продлить жизнь на 5-10 лет.
Хирургическое лечение булл (эндоскопическое «сшивание») может быть показано при рецидивирующих пневмотораксах на фоне растущих полостей. Пациенту проводятся операции буллэктомия и плевродез. Однако абсолютный успех такого лечения не может быть гарантирован.