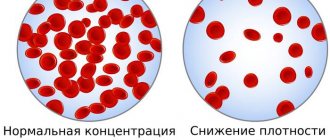
Если ваши суставы опухают и болят по ночам, врач-ревматолог предложит вам проверить ревматологический профиль. Это обследование поможет поставить точный диагноз, проследить динамику заболевания и назначить правильное лечение.
При подозрении на ревматическую болезнь используют следующие исследования:
- анализ крови на уровень мочевой кислоты;
- анализ крови на антинуклеарные антитела;
- исследование крови на ревматоидный фактор;
- исследование крови на АЦЦП (антитела к циклическому цитруллин-содержащему пептиду);
- анализ крови на С-реактивный белок.
Анализ крови на уровень мочевой кислоты
Мочевая кислота – это окончательный продукт распада пуринов. Ежедневно человек получает пурины вместе с продуктами питания, преимущественно с мясными продуктами. Затем с помощью определенных ферментов, пурины перерабатываются с образованием мочевой кислоты.
В нормальных физиологических количествах мочевая кислота нужна организму, она связывает свободные радикалы и защищает здоровые клетки от окисления. Кроме того, она так же, как и кофеин, стимулирует клетки головного мозга. Однако повышенное содержание мочевой кислоты имеет вредные последствия, в частности может приводить к подагре и некоторым другим заболеваниям.
Исследование уровня мочевой кислоты дает возможность диагностировать нарушение обмена мочевой кислоты и связанные с этим заболевания.
1
Ревматологическое обследование
2 Ревматологическое обследование
3 Ревматологическое обследование
Когда нужно провести обследование:
- при впервые возникшей атаке острого артрита в суставах нижних конечностей, возникшей без очевидных причин;
- при рецидивирующих атаках острого артрита в суставах нижних конечностей;
- если у вас в роду есть родственники страдающие подагрой;
- при сахарном диабете, метаболическом синдроме;
- при мочекаменной болезни;
- после проведения химиотерапии и/или лучевой терапии злокачественных опухолей (и особенно лейкозов);
- при почечной недостаточности (почки выводят мочевую кислоту);
- в рамках общего ревматологического обследования, необходимого для выяснения причины воспаления сустава;
- при продолжительном голодании, посте;
- при склонности к чрезмерному употреблению спиртных напитков.
Уровень мочевой кислоты
Уровень мочевой кислоты определяют в крови и в моче.
Мочевая кислота в крови называется урекемия, в моче – урикозурия. Повышенное содержание мочевой кислоты – гиперурикемия, пониженный уровень мочевой кислоты – гипоурикемия. Патологическое значение имеет только гиперурикемия и гиперурикозурия.
Концентрация мочевой кислоты в крови зависит от следующих факторов:
- количества пуринов, поступающих в организм с едой;
- синтеза пуринов клетками организма;
- образования пуринов вследствие распада клеток организма из-за болезни;
- функции почек, выводящих мочевую кислоту вместе с мочой.
В обычном состоянии наш организм поддерживает уровень мочевой кислоты в норме. Увеличение ее концентрации так или иначе связано с обменными нарушениями.
Нормы содержания мочевой кислоты в крови
У мужчин и женщин может наблюдаться различная концентрация мочевой кислоты в крови. Норма может зависеть не только от пола, но и возраста человека:
- у новорожденных и детей до 15 лет – 140-340 мкмоль/л;
- у мужчин до 65 лет – 220-420 мкмоль/л;
- у женщин до 65 лет – 40- 340 мкмоль/л;
- у женщин старше 65 лет – до 500 мкмоль/л.
Если превышение нормы происходит в течение длительного времени, то кристаллы соли мочевой кислоты (ураты) откладываются в суставах и тканях, вызывая различные болезни.
Гиперурикемия имеет свои признаки, но может протекать и бессимптомно.
Причины повышения содержания мочевой кислоты:
- прием некоторых лекарственных препаратов, например мочегонных;
- беременность;
- интенсивные нагрузки у спортсменов и людей, занимающихся тяжелым физическим трудом;
- длительное голодание или употребление продуктов, содержащих большое количество пуринов;
- некоторые болезни (например, эндокринные), последствия химиотерапии и облучения;
- нарушенный обмен мочевой кислоты в организме из-за дефицита некоторых ферментов;
- недостаточное выделение мочевой кислоты почками.
Как снизить концентрацию мочевой кислоты
Те, кто болен подагрой, знают, сколько неприятностей может доставить повышенная концентрация мочевой кислоты. Лечение этого недуга должно быть комплексным и обязательно включать прием препаратов, снижающих концентрацию мочевой кислоты в крови (ингибиторы ксантиноксидазы). Рекомендуется употребление большего количества жидкости и снижение потребления продуктов богатых пуринами.
Важно также постепенно избавиться от лишнего веса, поскольку ожирение обычно ассоциируется с повышением мочевой кислоты. Диета должна быть составлена так, чтобы количество продуктов, богатых пуринами было ограничено (красное мясо, печень, морепродукты, бобовые). Очень важно отказаться от алкоголя. Необходимо ограничить употребление винограда, томатов, репы, редьки, баклажанов, щавеля – они повышают уровень мочевой кислоты в крови. Зато арбуз, наоборот, выводит мочевую кислоту из организма. Полезно употреблять продукты, ощелачивающие мочу (лимон, щелочные минеральные воды).
Обмен пуринов представляет собой сложный биохимический процесс, в котором принимают участие многие ферментные системы. Большая часть мочевой кислоты в организме образуется в процессе метаболизма нуклеиновых кислот, однако описаны и другие пути ее синтеза. Во всех вариантах важнейшим промежуточным звеном является инозиновая кислота, которая в дальнейшем подвергается гидролизу. Образующийся гипоксантин под влиянием фермента ксантиноксидазы преобразуется в ксантин и мочевую кислоту. С точки зрения биохимии нарушения пуринового обмена представляют собой различные варианты дисбаланса между ферментными системами, отвечающими за синтез и транспортировку мочевой кислоты и ее предшественников.
Содержание пуринов в организме складывается из их поступления с продуктами питания и эндогенного синтеза. Считается, что в организме взрослого здорового человека содержится около 1000 мг мочевой кислоты. При подагре этот показатель может возрастать в несколько раз. Содержание мочевой кислоты в организме не является жестким и основным клиническим показателем состояния пуринового обмена. Диапазон нормальных значений мочевой кислоты крови колеблется в широких пределах, и у мужчин он находится в пределах 200-360 мкмоль/л, у женщин – 160340 мкмоль/сут. У здоровых людей за сутки выводится и вновь синтезируется примерно 750 мг, или 2/3 от общего объема мочевой кислоты. Из этого количества около 80%, или 600 мг экскретируется почками, оставшиеся 20% выводятся через желудочно-кишечный тракт. По расчетам П.М. Клименко и соавт. (2010), клиренс мочевой кислоты в норме составляет 5,4-9,0 мл/мин [1].
Обмен уратов в почках представляет собой сложный и многоступенчатый процесс. В клубочках происходит фильтрация уратов плазмы. Попавшие в ультрафильтрат ураты практически полностью реабсорбируются в проксимальном канальце, а затем секретируются. Некоторая часть секретированных уратов заново реабсорбируется. Процесс активной секреции уратов очень чувствителен к различным химическим агентам. Считается, что почечную секрецию уратов повышают оротовая кислота, лозартан, эстрогены, продукты распада тетрациклина. Почечную экскрецию уратов понижают этамбутол, тиазиды и тиазидоподобные диуретики, в меньшей степени фуросемид и ацетазоламид [2]. Склонность тиазидов и индапамида уменьшать почечную экскрецию уратов и повышать их сывороточную концентрацию делает эти препараты противопоказаными при подагре и гиперурикемии.
При нарушениях пуринового обмена происходит гиперпродукция мочевой кислоты, что проявляется повышением ее концентрации в крови (гиперурикемия) и моче (гиперурикурия).
КЛИНИЧЕСКИЕ ВАРИАНТЫ НАРУШЕНИЯ ОБМЕНА ПУРИНОВ
Сами по себе нарушения обмена пуринов не являются нозологическими единицами, подобно тому, как не являются заболеваниями различные врожденные и приобретенные ферментопатии без клинических проявлений. Однако заболевания, связанные нарушениями пуринового обмена, в реальной урологической практике встречаются сравнительно часто, что делает этот аспект актуальным. Большинство врачей-урологов хорошо знакомы с особенностями уратного нефролитиаза, и в то же время в большинстве случаев совершенно не имеют даже представления о существовании других, подчас более тяжелых заболеваний, обусловленных нарушениями пуринового обмена. Между тем все они встречаются с разной частотой в урологических стационарах, а также при консультативной работе.
Наиболее клинически значимым следствием нарушений пуринового обмена является повышение уровня мочевой кислоты в крови – гиперурикемия, которая и является основным патогенетическим фактором различных патологических состояний. В зависимости от этиологии гиперурикемия подразделяется на первичную и вторичную по отношению к какому-либо заболеванию.
Клиническим следствием первичной гиперурикемии является подагра в широком понимании этого термина. Сюда входит и классический острый микрокристаллический артрит, а также другие варианты поражения опорно-двигательной системы, и различные варианты подагрической нефропатии, одним из которых является уратный нефролитиаз, и тофусы различной локализации, и осложнения всех этих состояний.
Вполне очевидно, что для врачауролога больший интерес представляют заболевания органов мочеполовой системы, обусловленные гиперурикемией. В нефрологической и общетерапевтической практике для определения поражения почек вследствие гиперурикемии несколько десятилетий назад было введено понятие «подагрическая почка», которое в современной медицине трансформировалось в «подагрическую нефропатию». Учитывая экспериментально доказанное повреждающее действие гиперурикурии на почечные структуры, также предлагался термин «уратная нефропатия». Эти понятия являются обобщающими и объединяют несколько достаточно сильно различающихся по своему патогенезу процессов: острую мочекислую нефропатию, уратный нефролитиаз и хронический тубулоинтерстициальный нефрит. Некоторые авторы также отмечают возможность иммунокомплексного гломерулонефрита вследствие нарушения обмена пуринов [3].
В урологической практике наиболее часто встречаются пациенты с уратным нефролитиазом. До 80% таких пациентов хотя бы один раз в жизни имели эпизод артрита, причем совершенно необязательно классической локализации – I плюснефалангового сустава. В последнее время все чаше встречаются атипичные варианты артрита, например, гонит. Кроме того, широкое и бесконтрольное применение нестероидных противовоспалительных средств зачастую смазывает клиническую картину, увеличивая удельный вес артритов с меньшей активностью воспалительного процесса. Можно отметить, что сочетание артрита и уратного нефролитиаза является не обязательным, а, скорее, характерным.
Клиническая картина конкремента почки, мочеточника хорошо известна всем урологам, поэтому еще раз ее подробно описывать смысла нет. Однако необходимо отметить, что при наиболее тяжелом, «злокачественном» течении наряду с образованием уратных камней в просвете мочевых путей, возможно и отложение кристаллов мочевой кислоты в почечном интерстиции, что носит название нефрокальциноз. В отличие от нефролитиаза, нефрокальциноз при подагре всегда двухсторонний. Нефрокальциноз не имеет каких-либо специфических симптомов. Клинические проявления сводятся к прогрессированию почечной недостаточности за счет прогрессирования нефросклероза. Нефрокальциноз в большинстве случаев выявляется при ультразвуковом сканировании.
Тубулоинтерстициальный нефрит является характерным и частым вариантом подагрической нефропатии. Однако в виду меньшей яркости клинической картины, он известен, главным образом, специалистамнефрологам и ревматологам.
На начальных стадиях тубулоинтерстициального нефрита патологический процесс затрагивает, в основном, канальцы и почечный интерстиций, поэтому ведущим симптомом является нарушение концентрационной функции почек – полиурия с низкой плотностью мочи (гипостенурия). Протеинурия не превышает 1 г/сут или вовсе отсутствует – она связана с нарушением реабсорбции белка канальцами. Для подагрического интерстициального нефрита характерна стойкая уратурия, а также стойкая или эпизодическая микрогематурия, особенно после перенесенной респираторной вирусной инфекции. При иммуногистохимическом исследовании почечных биоптатов у части пациентов с клинической картиной подагрического тубулоинтерстициального нефрита было отмечено свечение С3-фракции комплемента и IgG, что характерно для иммунокомплексных гломерулонефритов. Это позволило выделить хронический гломерулонефрит как отдельный вариант подагрической нефропатии [3].
При прогрессировании подагрического тубулоинтерстициального нефрита характерно развитие артериальной гипертензии и нефросклероза.
Острая мочекислая нефропатия (острая подагрическая почка) в своей основе имеет обструкцию почечных канальцев кристаллами мочевой кислоты, что приводит к острой почечной недостаточности. Заболевание начинается с олигурии. Часть пациентов одновременно предъявляет жалобы на болевой синдром по типу почечной колики, макрогематурию, что может объясняться миграцией крупных кристаллов уратов по мочеточнику. Патогномоничной является высокая уратурия, не характерная для острой почечной недостаточности другой этиологии. Предположение об острой мочекислой нефропатии основывается на сочетании трех клинических признаков – высокоактивного артрита с характерной локализацией, резкого уменьшения диуреза и кирпично-бурого цвета мочи. Диагноз тем более вероятен, если имеются указания в анамнезе на гипогидратацию любого генеза – от посещения бани до неадекватной инфузионной терапии и передозировки мочегонных, а также на употребление значительного количества мясных продуктов и/или алкоголя. При естественном течении заболевания олигурия практически всегда прогрессирует до анурии с развернутой клинической картиной острой почечной недостаточности.
Проблема острой мочекислой нефропатии тесно связана с вторичным гиперурикемиям. Причины повышения уровня мочевой кислоты в сыворотке крови довольно многочисленны и разнообразны. Среди них: хроническая почечная недостаточность, независимо от этиологии, ожирение, особенно высоких степеней, плохо компенсированный сахарный диабет 2 типа, дислипидемия, акромегалия, гипотиреоз, гипопаратиреоз, токсикоз беременности, миелопролиферативные заболевания, хроническая интоксикация свинцом, хронический алкоголизм, тяжелые формы псориаза, химиои лучевая терапия. В большинстве случаев выраженность гиперурикемии при этих заболевания небольшая, реже – умеренная. Таким образом нарушения пуринового обмена довольно редко значимо отражаются на клинической картине заболевания. Однако их наличие влияет на развитие осложнений, а также повышает относительный риск кардиоваскулярной и общей смертности.
Самым ярким и клинически значимым вариантом вторичной гиперурикемии является «синдром лизиса опухоли» («синдром распада опухоли»), развивающийся при химиотерапии и радиотерапии лимфопролиферативных заболеваний, реже опухолей другой локализации. Ключевым компонентом этого синдрома, наряду с гиперфосфатемией и гиперкалиемией, является гиперпродукция мочевой кислоты, приводящая к развитию острой мочекислой нефропатии, причем нередко на неизмененных почках [4].
МЕДИКАМЕНТОЗНАЯ ТЕРАПИЯ ЗАБОЛЕВАНИЙ, ОБУСЛОВЛЕННЫХ НАРУШЕНИЯМИ ПУРИНОВОГО ОБМЕНА
Терапия нарушений обмена пуринов складывается из нескольких составляющих. Обязательно назначается диета с ограничением продуктов, богатых пуринами. Специфическими препаратами являются аллопуринол и цитрат.
Аллопуринол показан при подагрическом тубулоинтерстициальном нефрите, острой мочекислой нефропатии, уратном нефролитиазе в сочетании с гиперурикемией, а также при химиотерапии злокачественных новообразований для профилактики развития вторичной гиперурикемии и острой почечной недостаточности. Минимально эффективная дозировка – 200 мг/сут, среднетерапевтическая – 300-400 мг/сут. При химиотерапии злокачественных новообразований требуются высокие, близкие к максимальным дозировки аллопуринола – 600-900 мг/сут [2].
Цитратная терапия является неотъемлемой составляющей медикаментозного лечения подагрической нефропатии. Действие солей лимонной кислоты на процесс кристаллобразования в моче многогранно. Растворимость мочевой кислоты значительно меняется в зависимости от реакции среды. В кислой среде ураты имеют очень плохую растворимость и легко переходят в твердую фазу – кристаллизуются. При нейтральной или щелочной реакции растворимость этих солей увеличивается. Основным эффектом цитратов является способность уменьшать кислотность мочи, что предотвращает кристаллизацию уратов и создает условия для растворения уже сформированных кристаллов. На этом основана литолитическая терапия. Однако при щелочной реакции среды уменьшается растворимость фосфатов. Наслоение пленки фосфата на уратный камень делает практически бесперспективным процесс дальнейшего литолиза. Это диктует необходимость тщательного контроля за реакцией мочи на протяжении всего курса лечения. В современных условиях на смену эмпирическому применению растительного сырья, богатого лимонной кислотой и ее солями, пришли лекарственные средства, включающие в себя химически чистый цитрат и набор тест-полосок для мониторирования реакции мочи.
Помимо ощелачивания цитратом, для перевода мочевой кислоты в растворимую кето-форму необходимы ионы калия и натрия. Именно их количество определяет «ионную силу раствора». Соотношение же этих ионов между собой также немаловажно, т.к. показано, что избыток ионов натрия провоцирует образование кальциевой «корки» на камне.
Исследования 80-90-х годов продемонстрировали эффективность литолиза уратных камней с применением цитратов в режиме монотерапии порядка 75-80% [5, 6]. В настоящее время в результате совершенствования методики эффективность литолиза удалось поднять до 85-90%, в зависимости от особенностей химического состава конкрементов [1, 7, 8].
В последние годы появились работы, свидетельствующие о целесообразности включения препаратов цитрата в многокомпонентные схемы терапии. В частности, при уратных камнях мочеточника, особенно его дистальной трети, комбинированная терапия, включающая цитрат и тамсулозин, привела к самостоятельному отхождению 84,8% конкрементов, что достоверно отличается от групп пациентов, получавших монотерапию этими препаратами (68,8% и 58,8% соответственно), а также от пациентов, получавших плацебо (26,1%) [9].
Имеются убедительные доказательства эффективности комбинации аллопуринола и цитрата при подагрическом интерстициальном нефрите. Двенадцатинедельный курс комбинированной терапии, включающей Калия-натрия-гидрогенцитрат 3 гр/сут и аллопуринол 100-200 мг/сут, привел к росту скорости клубочковой фильтрации в среднем на 15 мл/мин по сравнению с контрольной группой монотерапии аллопуринолом. Также существенно повысился и клиренс мочевой кислоты и отмечалось большее ее снижение в крови. Отметим при этом низкую дозировку аллопуринола. Можно сделать предположение о возможном потенцировании эффектов аллопуринола и Калия-натриягидроген-цитрат. Дополнительным позитивным следствием должно быть снижение частоты побочных действий аллопуринола, что является существенным лимитирующим фактором при медикаментозном лечении подагрической нефропатии. Особенно значимым стало повышение клиренса креатинина при начальных стадиях хронической почечной недостаточности. [10]
Более яркий эффект цитрата в отношении функции почек отмечен при лечении хронического интерстициального нефрита, обусловленного гиперурикемией, у пациентов, страдающих ожирением [11].
Механизм действия цитрата не ограничивается защелачиванием мочи. Цитрат является одним из физиологических ингибиторов кристаллообразования. Так как моча в норме представляет собой пересыщенный солевой раствор, присутствие в ней ингибиторов кристаллообразования служит необходимым условием адекватного функционирования всей системы мочевыделения. Гипоцитратурия является самой распространенной метаболической аномалией у больных с камнеобразованием. Кроме этого, хелатные свойства цитратной молекулы по отношению к ионам кальция делают цитрат-ион незаменимым в профилактике рецидивов кальцийсодержащих камней. Цитрат + тиазидный диуретик – стандартное сочетание для метафилактики кальций-оксалатного нефролитиаза. Более того, такая терапия способствует увеличению плотности костной ткани. Этим может объясняться эффективность цитратов не только при уратном, но и при кальций-оксалатном нефролитиазе [12-14].
В связи с широким использованием ДЛТ и чрескожной нефролитотомии цитратная терапия стала активно применяться как до, так и после процедуры в течение 3х-4хнедель. Прием цитрата перед ДЛТ позволяет разрыхлить поверхность и структуру камня, что повышает успешность дробления камня при меньшей травматизации почки. А длительный прием после процедуры способствует ускоренному клиренсу фрагментов камня и препятствует рецидивированию литогенеза.
Наряду в вышеописанными механизмами действия, соли лимонной кислоты дополнительно обладают антисептическим, цитопротективным и метаболическим эффектами, которые также могут находить применение в клинической практике. В частности, Strassner C. и Friesen A. сообщают об исчезновении кандидурии у 16 пациентов из 18 на фоне терапии цитратами, что, вероятно, связано с изменением реакции мочи [15]. Заключение о цитопротективном эффекте цитрата сделано на основании успешных попыток Brühl P. et al. предотвращать с его помощью химическую травму слизистой мочевого пузыря при терапии препаратами из группы оксазафосфоринов – циклофосфамидом и ифосфамидом [16] (в современной онкологической и нефрологической практике с этой целью применяется препарат из группы муколитиков месна, практически не влияющий на КЩС). Также имеются сообщения об использовании цитрата для коррекции ацидоза вследствие уретеросигмостомии [17].
Основная сложность при цитратной терапии уратного нефролитиаза заключается в подборе адекватной дозировки препарата. Н.К.Дзеранов, на протяжении многих лет изучавший и разрабатывавший этот аспект, рекомендует начинать с назначения диеты и оценки реакции мочи в течение 5 дней в строго определенное время суток. На основании полученных средних значений рН мочи определяется начальная доза препарата и, главное, ее распределение в течение суток. Через 5 дней лечения снова определяются средние показатели реакции мочи в строго аналогичное время суток и, при необходимости, проводится коррекция дозировки препарата [18]. «Интерактивное», то есть в реальном времени, изменение дозировки цитрата неэффективно и даже небезопасно, так как приводит к скачкам рН, что может вызвать кристаллизацию фосфата.
Так как цитрат в норме присутствует в организме, лекарственные средства на его основе практически лишены токсичности. Тем не менее, существуют клинические ситуации, когда применение этих препаратов требует осмотрительности. Применение цитратных смесей нежелательно при острой мочекислой нефропатии и вообще при острой почечной недостаточности любой этиологии. Лимитирующим фактором выступает не цитратион как таковой, а калий, выведение которого в этой клинической ситуации затруднено. При острой мочекислой нефропатии целесообразно введение 4% раствора гидрокарбоната натрия, физиологического раствора и т.д. в сочетании с петлевыми диуретиками. Необходимо поддерживать диурез на уровне не менее 100-150 мл/час, рН мочи не ниже 6,5 [3, 4].
При тяжелой недостаточности кровообращения лимитирующим фактором является повышенное поступление в организм натрия. Иногда в этой ситуации предпочтительнее оказывается ацетазоламид. Этот препарат из группы диуретиков сильно, а главное, неконтролируемо защелачивает мочу, что делает его неконкурентоспособным по сравнению с цитратом при медикаментозной терапии уратного нефролитиаза. Однако ацетазоламид – практически единственная возможность повысить рН мочи, не прибегая к введению солей, что в условиях тяжелой сердечной недостаточности крайне нежелательно.
Таким образом, медикаментозное лечение пациентов с нарушениями обмена пуринов представляет собой сложную и многогранную проблему, требующую междисциплинарного подхода.
Резюме:
В статье рассмотрены основные клинические варианты нарушений пуринового обмена, встречающиеся в урологической практике. Кратко отражена патофизиология нарушений метаболизма пуринов. Рассмотрены все клинические варианты подагрической нефропатии, в том числе особенности патогенеза и клинические проявления. В статье подробно рассмотрены основные подходы к медикаментозной терапии этих состояний с акцентом на специфическую терапию цитратом. Проанализирована доступная литература по данному вопросу. Продемонстрированы возможности применения цитрата как в режиме монотерапии, так и в комбинации с другими лекарственными средствами. Определены показания и противопоказания к применению этих препаратов.
ЛИТЕРАТУРА
1.Клименко П.М., Чабанов В.А., Акиншевич И.Ю. Возможности консервативного лечения больных уратным нефролитиазом. // Новости медицины и фармации. 2010. №3. С.5-7.
2. Федеральное руководство по использованию лекарсвенных средств (формулярная система). Выпуск Х. 2009 год. Под редакцией Чучалина А.Г., Белоусова Ю.Б., Яснецова В.В. Москва. ЗАО РИЦ «Человек и лекарство».
3. Нефрология. Руководство для врачей. Под редакцией И.Е. Тареевой. Москва. Медицина. 2000. 688с.
4. Нефрология. Национальное руководство. Под редакцией Н.А. Мухина. Москва. ГЭОТАР–Медиа. 2009. 716с.
5. Chugtai M.N., Khan F.A., Kaleem M., Ahmed M. Management of uric acid stone. // J Pak Med Assoc. 1992 Jul;42(7):153-5.
6. Petritsch P.H. Uric acid calculi: results of conservative treatment. // Urology. 1977 Dec;10(6):536-8.
7. Елисеев М.С., Денисов И.С., Барскова В.Г. Применение цитрата Уралит–У у больных подагрой и нефролитиазом. // Совpeменная ревматология. 2012. № 3. С.13-15.
8. Пасечников С.П., Митченко М.В. Современные аспекты цитратной терапии при мочекаменной болезни. Опыт применения препарата Уралит-У. // Здоровье мужчины. 2007. №3. С.109-113.
9. El-Gamal O., El-Bendary M., Ragab M., Rasheed M. Role of combined use of potassium citrate and tamsulosin in the management of uric acid distal ureteral calculi // Urological Research June 2012, Volume 40, Issue 3, pp 219-224.
10. Saito J., Matsuzawa Y., Ito H., Omura M., Ito Y., Yoshimura K., Yajima Y., Kino T., Nishikawa T. рЈe alkalizer citrate reduces serum uric Acid levels and improves renal // Endocr Res 2010;35(4):145-154.
11. Saito J., Matsuzawa Y., Ito H., Omura M., Kino T., Nishikawa T. Alkalizer Administration Improves Renal Function in Hyperuricemia Associated with Obesity. // Japanese Clinical Medicine 2013:4.
12. Butz M. Oxalate stone prophylaxis by alkalinizing therapy. // Urologe A. 1982 May;21(3):142-6.
13. Ito H. Combined administration of calcium and citrate reduces urinary oxalate excretion. // Hinyokika Kiyo. 1991 Oct;37(10):1107-10.
14. Berg C., Larsson L., Tiselius H.G. Effects of different doses of alkaline citrate on urine composition and crystallization of calcium oxalate. // Urological Research February 1990, Volume 18, Issue 1, pp 13-16.
15. Strassner C., Friesen A. Therapy of candiduria by alkalinization of urine. Oral treatment with potassium-sodium-hydrogen citrate. // https://www.ncbi.nlm.nih.gov/pubmed/7498850
16. Bruhl P., Hoefer-Janker H., Scheef W., Vahlensieck W. Prophylactic alkalization of the urine during cytostatic tumor treatment with the oxazaphosphorine derivatives, cyclophosphamide and ifosfamide. // Onkologie. 1979 Jun;2(3):120-4.
17. Sasagama I., Nakada T., Ishgooka M., Kubota Y., Sawamura T. Efect of standardized mixture of potassium and sodium citrate and citric acide (Uralit-U) on the correction of postoperative acidosis in patients who underwent uireterosigmostomy. // Nephron 1994;66:477-478.
18. Дзеранов Н.К., Рапопорт Л.М. Литолитическая терапия. Практические рекомендации. Москва. ООО «Информполиграф». 2011. 16с.
| Прикрепленный файл | Размер |
| 346.13 кб |
‹ Молекулярно-генетические нарушения как критерии в дифференциальной диагностике редких опухолей почки Вверх Ноктурия: современные гендерные аспекты эпидемиологии, патогенеза и диагностики ›
Антинуклеарные антитела (АНА)
С помощью АНА теста можно определить наличие в крови антинуклеарных антител (антител к ядерным антигенам).
АНА – это группа специфических аутоантител, которые производит иммунная система нашего организма в случае аутоиммунных нарушений. Антитела оказывают повреждающее действие на клетки организма. При этом человек испытывает различные болезненные симптомы, например боль в мышцах и суставах, общую слабость и др.
Обнаружение в сыворотке крови антител принадлежащих к группе АНА (например, антител к двуспиральной ДНК) помогает выявить аутоимунное заболевание, контролировать течение болезни и эффективность его лечения.
1 Исследование крови на АЦЦП
2 Анализ крови на С-реактивный белок
3 Исследование крови на АЦЦП
Когда необходим анализ крови на антинуклеарные антитела
Выявление антинуклеарных антител может быть признаком следующих аутоиммунных заболеваний:
- полимиозит;
- дерматомиозит;
- системная красная волчанка;
- смешанное заболевание соединительной ткани;
- склеродермия;
- синдром и болезнь Шегрена;
- синдром Рейно;
- аутоиммунный гепатит
Как выполняется тест на антинуклеарные антитела
Кровь на антинуклеарные антитела берется из вены на локтевом сгибе, натощак. Перед исследованием можно не придерживаться никакой диеты.
В некоторых случаях, для того чтобы дифференцировать различные аутоиммунные заболевания, могут потребоваться дополнительные уточняющие тесты на аутоантитела из группы антинуклеарных антител, так называемый иммуноблот АНА.
Что обозначают данные теста
Антинуклеарные антитела (другое название — антинуклеарный фактор) указывают на наличие какого-то аутоиммунного нарушения, однако не указывают точно на болезнь, вызвавшую его, поскольку тест на АНА является скрининговым исследованием. Цель любого скрининга – выявить людей с повышенным риском того или иного заболевания.
У здорового человека с нормальным иммунитетом антинуклеарных антител в крови быть не должно или их уровень не должен превышать установленные референсные значения.
Нормальное значение АНА подразумевает титр антител, не превышающий значение 1: 160. Ниже этого значения анализ считается отрицательным.
Положительный анализ на антинуклеарные антитела (1:320 и более) указывает на повышение антинуклеарных антител, и наличие у человека заболевания аутоиммунной природы.
В настоящее время для выявления антинуклеарных антитела используются две методики: непрямую реакцию иммунофлюоресценции с использованием так называемой клеточной линии Нер2 и иммуноферментный анализ. Оба теста дополняют друг друга, в связи с чем их рекомендуют выполнять одновременно.
Можно выделить следующие виды антинуклеарных тел АНА в реакции непрямой иммунофлюоресненции:
- гомогенная окраска — может быть при любом аутоиммунном заболевании;
- пятнистая или крапчатая окраска может быть при системной красной волчанки, склеродермии, синдроме Шегрена, ревматоидном артрите, полимиозите и смешанном заболевании соединительной ткани;
- периферическая окраска – характерна для системной красной волчанки;
При положительном анализе на антинуклеарные антитела необходимо провести иммуноблот антинуклеарных антител для уточнения типа аутоиммунного заболевания и постановки диагноза.
Ревматоидный фактор
Исследование крови на ревматоидный фактор направлено на выявление специфических антител класса IgM к антителам класса IgG.
Лабораторный тест на ревматоидный фактор является скрининговым исследованием, направленным на выявление аутоиммунных нарушений. Главная задача исследования на ревматоидный фактор – выявление ревматоидного артрита, болезни и синдрома Шегрена и ряда других аутоиммунных болезней.
Анализ на ревматоидный фактор может потребоваться при следующих симптомах:
- боли и отечность в суставах;
- ограничение подвижности в суставах;
- чувство сухости в глазах и во рту;
- кожные высыпания по типу кровоизлияний;
- слабость, упадок сил.
1 Ревматоидный артрит
2 Ревматологическое обследование
3 Ревматологическое обследование
Нормы ревматоидного фактора в крови
Теоретически в здоровом организме ревматоидного фактора быть не должно. Но все же в крови у некоторых даже здоровых людей этот фактор присутствует в небольшом титре. В зависимости от лаборатории верхняя граница нормы ревматодного фактора варьирует от 10 до 25 международных единиц (МЕ) на 1 миллилитр крови.
Ревматоидный фактор одинаковый у женщин и мужчин. У людей пожилого возраста показатель ревматоидного фактора будет несколько выше.
Ревматоидный фактор у ребенка должен составлять в норме 12,5 МЕ на миллилитр.
Анализ на ревматоидный фактор используется для диагностики следующих заболеваний:
- ревматоидный артрит;
- системные аутоиммунные заболевания;
- риоглобулинемия.
Другие причины повышения ревматоидного фактора
Дополнительные причины повышения ревматоидного фактора могут быть следующими:
- сифилис;
- краснуха;
- инфекционный мононуклеоз;
- малярия;
- туберкулез;
- грипп;
- гепатит;
- лейкемия;
- цирроз печени;
- сепсис
Если причина повышенного ревматоидного фактора – инфекционные заболевания, например, инфекционный мононуклеоз, то титр ревматоидного фактора обычно меньше, чем при ревматоидном артрите.
Тем не менее, анализ на ревматоидный фактор прежде всего помогает распознать ревматоидный артрит. Однако следует подчеркнуть, что ставить диагноз лишь на его основании нельзя. Поскольку ревматоидный фактор может быть повышенным при многих других патологических состояниях аутоиммунной и не аутоиммунной природы. Кроме этого, примерно у 30% больных ревматоидным артритом анализ крови на ревматоидный фактор может оказаться отрицательным (серонегативный вариант ревматоидного артрита).
Анализ крови на ревматоидный фактор проводят утром натощак (с последнего приема пищи должно пройти от 8 до 12 часов).
Причины снижения мочевой кислоты
Если мочевая кислота в крови понижена, то говорят о гипоурикемии. Выделяют следующие основные причины снижения уровня концентрации мочевой кислоты:
- Синдром Фанкони – всасываемость почечных канальцев нарушено, заболевание является врожденным
- Гепатоцеребральная дистрофия – патология, передающаяся по наследству, характеризуется проблемами с обменом микроэлементов (медь в частности). Первыми поражаются центральная нервная система и печень.
- Приобретённый дефицит ксантиноксидазы. Основной причиной заболевания является нарушение функций печени, лекарственные препараты с содержанием вещества аллопуринол. На выработку ферментов, отвечающих за синтез кислоты, влияет действующее вещество препарата.
- Наследственный дефицит ксантиноксидазы – организм не может самостоятельно синтезировать мочевую кислоту. Встречается реже чем приобретённый.
- Алкоголизм.
- Неправильное питание.
Нередко снижение концентрации кристаллов наблюдается у женщин, ожидающих ребёнка. Связано это увеличением у беременных количество крови. А концентрация клеток и растворенных минералов снижается. Другой причиной является увеличение эстрогена, влияющего на образование кристаллов кислоты.
АЦЦП
Анализ крови на АЦЦП заключается в определении титра антител к циклическому цитруллинированному пептиду и является одним из точных методов для подтверждения диагноза ревматоидного артрита. С его помощью болезнь можно обнаружить за несколько лет до возникновения симптомов.
Что показывает анализ АЦЦП
Цитруллин – это аминокислота, которая является продуктом биохимической трансформации другой аминокислоты – аргинина. У здорового человека цитруллин не принимает участия в синтезе белка и полностью выводится из организма.
Но при ревматоидном артрите цитруллин начинает встраиваться в аминокислотную пептидную цепочку белков синовиальной оболочки и хрящевой ткани суставов. «Новый» видоизмененный белок, имеющий в своем составе цитруллин, воспринимается иммунной системой как «чужой» и в организме начинают производиться антитела к цитруллин-содержащему пептиду (АЦЦП).
АЦЦП – это специфический маркер ревматоидного артрита, своеобразный предвестник заболевания на ранней стадии, обладающий высокой специфичностью. Антитела к циклическому цитруллинированному пептиду обнаруживаются задолго до первых клинических признаков ревматоидного артрита и остаются в течение всей болезни.
Методика анализа и его значение
Для выявления АЦЦП используют иммунноферментный анализ. Анализ крови на АЦЦП проводят по принципу «инвитро» (в переводе с латинского — в пробирке), исследуется сыворотка из венозной крови. АЦЦП анализ крови может быть готов уже через сутки (зависит от вида лаборатории).
Выявление АЦЦП при ревматоидном артрите может указывать на более агрессивную, так называемую эрозивную форму заболевания, которая ассоциируется с более быстрым разрешением суставов и развитием характерных суставных деформаций.
Если результат анализа на АЦЦП оказывается положительным, то прогноз ревматоидного АЦЦП артрита считается менее благоприятным.
1 Исследование крови на АЦЦП
2 Анализ крови на С-реактивный белок
3 Исследование крови на АЦЦП
АЦЦП. Референсные значения
Диапазон нормальных значений для анализа на АЦЦП составляет приблизительно 0-5 ед/мл. Так называемая «АЦЦП норма» может колебаться в зависимости от лаборатории. Значения «АЦЦП нормы» у женщин и у мужчин одинаковые.
Так называемый «Повышенный АЦЦП», например, АЦЦП 7 ед/мл и более, указывает на высокую вероятность заболевания ревматоидным артритом. Результат анализа расцененный как «АЦЦП отрицательный» снижает вероятность заболевания ревматоидным артритом, хотя полностью его не исключает. Оценивать значения АЦЦП и проводить их интерпретацию должен всегда врач-ревматолог, имеющий опыт диагностики и лечения ревматоидного артрита, только ревматолог может учесть все нюансы.
Чтобы сдать анализ на АЦЦП, вам необходимо прийти на обследование натощак.
Показания к назначению анализа:
- ревматоидный артрит;
- ранний синовит;
- остеоартрит;
- ревматическая полимиалгия;
- псориатический артрит;
- болезнь Рейно;
- реактивный артрит;
- саркоидоз;
- склеродерма;
- синдром Шегрена;
- СКВ;
- васкулит;
- ювенильный РА.
Если вы хотите узнать стоимость анализа крови на АЦЦП, позвоните по телефону.
Специалисты контакт-центра сообщат вам цену АЦЦП и объяснят, как готовиться к исследованию.
Анализ на С-реактивный белок
С-реактивный белок (СРБ) – очень чувствительный элемент анализа крови, который быстро реагирует даже на мельчайшее повреждение ткани организма. Присутствие С-реактивного белка в крови является предвестником воспаления, травмы, проникновения в организм бактерий, грибков, паразитов.
СРБ точнее показывает воспалительный процесс в организме, чем СОЭ (скорость оседания эритроцитов). В то же время С-реактивный белок быстро появляется и исчезает – быстрее, чем изменяется СОЭ.
За способность С-реактивного белка в крови появляться в самый пик заболевания его еще называют «белком острой фазы».
При переходе болезни в хроническую фазу С-реактивный белок снижается в крови, а при обострении процесса повышается вновь.
С-реактивный белок норма
С-реактивный белок производится клетками печени и в сыворотке крови содержится в минимальном количестве. Содержание СРБ в сыворотке крови не зависит от гормонов, беременности, пола, возраста.
Норма С-реактивного белка у взрослых и детей одинаковая – меньше 5 мг/ л (или 0,5 мг/ дл).
Анализ крови на С-реактивный белок берется из вены утром, натощак.
1 Анализ крови на уровень мочевой кислоты
2 анализ крови на антинуклеарные антитела
3 Исследование крови на ревматоидный фактор
Причины повышения С-реактивного белка
С-реактивный белок может быть повышен при наличии следующих заболеваний:
- ревматизм;
- острые бактериальные, грибковые, паразитарные и вирусные инфекции;
- желудочно-кишечные заболевания;
- очаговые инфекции (например, хронический тонзиллит);
- сепсис;
- ожоги;
- послеоперационные осложнения;
- инфаркт миокарда;
- бронхиальная астма с воспалением органов дыхания;
- осложненный острый панкреатит;
- менингит;
- туберкулез;
- опухоли с метастазами;
- некоторые аутоиммунные заболевания (ревматоидный артрит, системный васкулит и др.).
При малейшем воспалении в первые же 6-8 часов концентрация С-реактивного белка в крови повышается в десятки раз. Имеется прямая зависимость между тяжестью заболевания и изменением уровня СРБ. Т.е. чем выше концентрация С-реактивного белка, тем сильнее развивается воспалительный процесс.
Поэтому изменение концентрации С-реактивного белка используется для мониторинга и контроля эффективности лечения бактериальных и вирусных инфекций.
Разные причины приводят к разному повышению уровня С-реактивного белка:
- Наличие бактериальных инфекций хронического характера и некоторых системных ревматических заболеваний повышает С-реактивный белок до 10-30 мг/л. При вирусной инфекции (если нет травмы) уровень СРБ повышается незначительно. Поэтому высокие его значения указывают на наличие бактериальной инфекции.
- При подозрении на сепсис новорожденных уровень СРБ 12 мг/л и более говорит о необходимости срочной противомикробной терапии.
- При острых бактериальных инфекциях, обострении некоторых хронических заболеваний, остром инфаркте миокарда и после хирургических операциях самый высокий уровень СРБ – от 40 до 100 мг/л. При правильном лечении концентрация С-реактивного белка снижается уже в ближайшие дни, а если этого не произошло, необходимо обсудить другое антибактериальное лечение. Если за 4-6 дней лечения значение СРБ не уменьшилось, а осталось прежним и даже увеличилось, это указывает на появление осложнений (пневмония, тромбофлебит, раневой абсцесс и др.). После операции СРБ будет тем выше, чем тяжелее была операция.
- При инфаркте миокарда белок повышается через 18-36 часов после начала заболевания, через 18-20 дней снижается и к 30-40 дню приходит к норме. При стенокардии он остается в норме.
- При различных опухолях повышение уровня С-реактивного белка может служить тестом для оценки прогрессирования опухолей и рецидива заболевания.
- Тяжелые общие инфекции, ожоги, сепсис повышают С-реактивный белок до огромнейших значений: до 300 мг/л и более.
- При правильном лечении уровень С-реактивного белка снижается уже на 6-10 день.
Подготовка к ревматологическим анализам
Чтобы анализы показывали объективную информацию, необходимо придерживаться некоторых правил. Сдавать кровь нужно в утренние часы, натощак. Между взятием анализов и приемом пищи должно пройти приблизительно 12 часов. Если мучает жажда, выпейте немного воды, но не сок, чай или кофе. Необходимо исключить интенсивные физические упражнения, стрессы. Нельзя курить и употреблять спиртное.
Многопрофильная клиника «МедикСити» — это диагностика высочайшего уровня, опытные квалифицированные врачи-ревматологи и специалисты более чем 30 специальностей. У нас проводится лечение артрита, артроза, васкулита, красной волчанки, остеопороза, подагры, ревматизма и многих других ревматологических заболеваний. Не откладывайте визит к врачу, обращайтесь при малейших симптомах. Качественная диагностика – это 90% успешного лечения!
Как определить точный показатель мочевой кислоты?
Биохимический анализ крови покажет уровень мочевой кислоты в крови, его проводят как здоровым людям, для возможного выявления заболеваний, так и людям страдающим нарушением обмена веществ – мочекаменной болезнью, диабетом, подагрой и т.д.
Существуют определенные рекомендации для получения точного результата анализа:
- Исключить из рациона питания за 8 часов до сдачи анализа всю высокобелковую еду.
- Не употреблять алкоголь и лекарства за сутки до забора.
- Кровь берётся на голодный желудок.
- Избегать физических нагрузок накануне сдачи анализа.
Берётся кровь из вены. Чаще всего результат готов уже на следующий день. При сниженном результате, назначается повторный анализ. После подтверждения отклонения от нормы, врачом назначается полное обследование и по его результатам ставится диагноз.
Факторы, которые могут повлиять на результат анализа:
- Прием мочегонных препаратов:
- Гормональные лекарственные средства
- Рацион с минимальным содержание белка.
Перед исследованием обязательно следует исключить такие факторы.