Фармакологические свойства препарата Тамифлю
Механизм действия. Противовирусный препарат. Осельтамивира фосфат является пролекарством, его активный метаболит (осельтамивира карбоксилат) эффективный и селективный ингибитор нейраминидазы вирусов гриппа типа А и В — фермента, катализирующего процесс высвобождения вновь образованных вирусных частиц из инфицированных клеток, их проникновения в клетки эпителия дыхательных путей и дальнейшего распространения вируса в организме. Тормозит рост вируса гриппа in vitro и подавляет репликацию вируса и его патогенность in vivo, уменьшает выделение вирусов гриппа А и В из организма. Тамифлю значительно сокращает период клинических проявлений гриппозной инфекции, уменьшает их тяжесть и снижает частоту развития осложнений гриппа, требующих применения антибиотиков (бронхита, пневмонии, синусита, среднего отита), укорачивает время выделения вируса из организма и уменьшает площадь под кривой «вирусные титры-время». У детей в возрасте от года 1 до 12 лет Тамифлю значительно снижает продолжительность заболевания (на 35,8 ч), частоту острого среднего отита. Выздоровление и возвращение к обычной активности наступает почти на 2 дня раньше. При приеме с целью профилактики Тамифлю достоверно (на 92%) снижает заболеваемость гриппом среди контактировавших лиц, на 76% — частоту клинически установленного гриппа во время вспышки заболевания, уменьшает частоту выделения вируса и предотвращает передачу вируса от одного члена семьи к другому. У детей от 1 года до 12 лет профилактический прием Тамифлю снижает частоту лабораторно подтвержденного гриппа с 24 до 4%. Тамифлю не влияет на образование противогриппозных антител, в т.ч. на выработку антител в ответ на введение инактивированной вакцины против гриппа. Резистентность. При приеме Тамифлю с целью профилактики (7 дней), профилактики контактировавших в семье (10 дней) и сезонной профилактики (42 дня) случаев резистентности к препарату не отмечено. У взрослых пациентов/подростков была обнаружена резистентность к осельтамивиру в 0,32% случаев (4/1245) с помощью фенотипирования и в 0,4% случаев (5/1245) с помощью фенотипирования и генотипирования, а у детей от 1 года до 12 лет в 4,1% (19/464) и в 5,4% (25/464) случаев соответственно. У всех пациентов наблюдалось временное носительство ОС-резистентного вируса. Это не влияло на элиминацию вируса. Было обнаружено несколько различных подтип-специфичных мутаций нейраминидазы вирусов. Степень снижения чувствительности зависела от типа мутации, так при мутации 1222V в N1 чувствительность снижалась в 2 раза, а при R292K в N2 — в 30000 раз. Не было обнаружено мутации, снижающих чувствительность нейраминидазы вируса гриппа типа В in vitro. У пациентов, получавших терапию осельтамивиром, зарегистрированными мутациями нейраминидазы N1 (включая H5N1 вирусы), приводящими к резистентности/снижению чувствительности к ОС, были H274Y, N294S (1 случай), E119V (1 случай), R292K (1 случай), и мутациями нейраминидазы N2 — N294S (1 случай) и SASG245-248del (1 случай). В одном случае была обнаружена мутация G402S вируса гриппа В, выразившаяся в снижении чувствительности в 4 раза и в 1 случае — мутация D198N с 10-кратным снижением чувствительности у ребенка с иммунодефицитом. Вирусы с резистентным генотипом нейраминидазы в различной степени отличаются по устойчивости от природного штамма. Вирусы с мутацией R292K в N2 у животных (мышей и хорьков) по инфекционности, патогенности и контагиозности значительно уступают вирусам с мутацией E119V в N2 и D198N в В и незначительно отличаются от природного штамма. Вирусы с мутацией H274Y в N1 и N294S в N2 занимают промежуточное положение. Фармакокинетика Осельтамивира фосфат легко всасывается в ЖКТ и в высокой степени превращается в активный метаболит под действием печеночных и кишечных эстераз. Концентрации активного метаболита в плазме определяются в пределах 30 мин, время достижения Cmax — 2–3 ч, более чем в 20 раз превышают концентрации пролекарства. Не менее 75% принятой внутрь дозы попадает в системный кровоток в виде активного метаболита, менее 5% — в виде исходного препарата. Плазменные концентрации как пролекарства, так и активного метаболита пропорциональны дозе и не зависят от приема пищи. Объем распределения (Vss) активного метаболита — 23 л. После приема внутрь осельтамивира фосфата его активный метаболит обнаруживался в легких, промывных водах бронхов, слизистой оболочке полости носа, среднем ухе и трахее в концентрациях, обеспечивающих противовирусный эффект. Связывание активного метаболита с белками плазмы — 3%. Связывание пролекарства с белками плазмы — 42%, что недостаточно, чтобы служить причиной существенных лекарственных взаимодействий. Осельтамивира фосфат в высокой степени превращается в активный метаболит под действием эстераз, находящихся преимущественно в печени и кишечнике. Ни осельтамивира фосфат, ни активный метаболит не являются субстратами или ингибиторами изоферментов системы цитохрома Р450. Выводится (>90%), в виде активного метаболита преимущественно почками. Активный метаболит не подвергается дальнейшей трансформации и выводится с мочой (>99%) путем клубочковой фильтрации и канальцевой секреции. Почечный клиренс (18,8 л/ч) превышает скорость клубочковой фильтрации (7,5 л/ч), что указывает на то, что препарат выводится еще и путем канальцевой секреции. С калом выводится менее 20% принятого препарата. Т1/2 активного метаболита — 6–10 ч. Фармакокинетика в особых группах Больные с поражением почек. При назначении Тамифлю больным с различной степенью поражения почек значения AUC обратно пропорциональны снижению функции почек. Больные с поражением печени. In vitro у пациентов с печеночной патологией не отмечено ни значительного повышения AUC осельтамивира фосфата, ни снижения AUC активного метаболита. Больные старческого возраста. У больных старческого возраста (65–78 лет) экспозиция активного метаболита в равновесном состоянии на 25–35% выше, чем у более молодых пациентов при назначении аналогичных доз Тамифлю. Т1/2 препарата у пожилых существенно не отличался от такового у более молодых пациентов. Больным старческого возраста коррекции дозы при лечении и профилактике гриппа не требуется. Дети. У детей младшего возраста выведение пролекарства и активного метаболита происходит быстрее, чем у взрослых, что приводит к более низким AUC по отношению к конкретной дозе. Прием препарата в дозе 2 мг/кг обеспечивает такую же AUC осельтамивира карбоксилата, какая достигается у взрослых после однократного приема капсулы с 75 мг препарата (что эквивалентно примерно 1 мг/кг). Фармакокинетика осельтамивира у детей старше 12 лет такая же, как у взрослых.
Инструкция по применению ТАМИФЛЮ® (TAMIFLU®)
Противовирусный препарат. Осельтамивира фосфат является пролекарством активного метаболита (осельтамивира карбоксилата). Активный метаболит является селективным ингибитором фермента нейраминидазы вируса, гликопротеиновых ферментов, находящихся на поверхности вириона. Активность вирусного фермента нейраминидазы важна для освобождения образованных вирусных частиц из инфицированных клеток и дальнейшего распространения вируса в организме.
Осельтамивира карбоксилат in vitro ингибирует нейраминидазы вирусов гриппа A и B. Осельтамивира фосфат ингибирует рост вируса гриппа и подавляет его репликацию in vitro. Пероральный прием осельтамивира ингибирует репликацию и патогенность in vivo вирусов гриппа A и B в испытаниях моделей гриппа на животных, при дозах аналогичных приему человеком 75 мг 2 раза/сут.
Противовирусная активность осельтамивира в отношении гриппа А и В была подтверждена экспериментальными исследованиями с провокационными пробами у здоровых добровольцев.
Значение медианы ингибирующей концентрации (IC50) осельтамивира в отношении фермента нейраминидазы для клинически изолированного гриппа А колебалось от 0.1 нМ до 1.3 нМ, для гриппа В было 2.6 нМ. В опубликованных результатах исследований сообщалось о более высоких значениях IC50 для гриппа В — вплоть до 8.5 нМ.
Клинические исследования
Лечение гриппа
Осельтамивир эффективен только при заболеваниях, вызванных вирусом гриппа. Поэтому статистические данные анализа представлены только для инфицированных гриппом пациентов. В объединенном исследовании популяции, включающей положительных и отрицательных в отношении вируса гриппа пациентов (ITT), первичная эффективность снижалась пропорционально количеству отрицательных в отношении вируса гриппа пациентов. Во всей популяции, получающей лечение, инфекция гриппа подтверждена у 67% (диапазон от 46% до 74%) рекрутированных пациентов. Из всех пожилых пациентов 64% были положительными в отношении вируса гриппа, и из всех пожилых пациентов с хронической сердечной недостаточностью и/или респираторными заболеваниями 62% являлись положительными в отношении вируса гриппа. Во всех клинических исследованиях фазы III пациенты рекрутировались только в период эпидемии гриппа в данной местности.
Взрослые и подростки в возрасте 13 лет и старше.
Были отобраны те пациенты, которые сообщали о проявившихся симптомах заболевания в пределах 36 ч, у которых была лихорадка ≥37.8°, сопровождающаяся хотя бы одним респираторным симптомом (кашель, назальные симптомы, боль в горле) и хотя бы одним системным симптомом (боль в мышцах, озноб/потливость, недомогание, слабость или головная боль). В объединенном анализе всех взрослых и подростков, положительных в отношении вируса гриппа (n=2413), включенных в исследования лечения, назначение осельтамивира 75 мг 2 раза/сут в течение 5 дней снизило среднюю продолжительность гриппа на один день по сравнению с группой плацебо, с 5.2 дня (95% доверительный интервал 4.9-5.5 дня) до 4.2 дня (95% доверительный интервал 4.0-4.4 дня; p ≤ 0.0001).
Доля пациентов, у которых возникли осложнения со стороны нижних дыхательных путей, требующие лечения антибиотиками (в основном бронхит), уменьшилась с 12.7% (135/1063) в группе плацебо до 8.6% (116/1350) у пациентов, получавших лечение осельтамивиром (p =0.0012).
Лечение гриппа в популяциях высокого риска.
Средняя продолжительность гриппа существенно не уменьшилась у лиц пожилого возраста (≥65 лет) и у пациентов с хроническим заболеванием сердца и/или дыхательных путей, получавших осельтамивир 75 мг 2 раза/сут в течение 5 дней. В группе лечения осельтамивиром уменьшилась продолжительность периода температуры на один день. У пациентов пожилого возраста, положительных в отношении вируса гриппа, под действием осельтамивира существенно уменьшилась частота возникновения осложнений со стороны нижних дыхательных путей, требующих лечения антибиотиками (в основном бронхита), с 19% (52/268) в группе плацебо до 12% (29/250) у пациентов, получавших лечение осельтамивиром (p = 0.0156).
У положительных в отношении вируса гриппа пациентов, страдающих хроническими заболеваниями сердца и/или дыхательных путей, комбинированная частота возникновения инфекций нижних дыхательных путей, требующих лечения антибиотиками (главным образом бронхит), в группе плацебо составляла 17% (22/133) и в группе, получавшей осельтамивир, — 14% (16/118) (p = 0.5976).
Лечение гриппа у детей.
В исследовании здоровых в других отношениях детей (65% положительных в отношении гриппозной инфекции) в возрасте 1-12 лет (средний возраст 5.3 года), у которых была лихорадка (≥ 37.8°C) вместе с кашлем или насморком, 67% инфицированных гриппом пациентов были заражены гриппом А и 33% — гриппом В. Лечение осельтамивиром, начатое в течение 48 часов после возникновения симптомов заболевания, существенно уменьшало время, требующееся на лечение болезни (что определялось как одновременное восстановление здоровья и способности к деятельности и отсутствие температуры, кашля и насморка) на 1.5 дня (95% доверительный интервал 0.6-2.2 дня; p < 0.0001) по сравнению с плацебо. Прием осельтамивира уменьшал частоту возникновения острого воспаления среднего уха с 26.5% (53/200) в группе плацебо до 16% (29/183) в группе принимавших осельтамивир (p=0.013).
В другое исследование были включены 334 больных бронхиальной астмой ребенка в возрасте 6-12 лет, из которых 53.6% были позитивны в отношении вируса гриппа. В группе, получавшей лечение осельтамивиром, средняя продолжительность заболевания существенно не уменьшилась. На 6 день (последний день лечения) в данной популяции ОФВ1 увеличивался на 10.8% в группе пациентов, принимавших осельтамивир, по сравнению с 4.7% в группе плацебо (p=0.0148).
Европейское агентство лекарственных средств (EMA) отсрочило необходимость подавать результаты исследований Тамифлю в одной или более подгруппах педиатрической популяции больных гриппом.
Лечение инфекции гриппа B.
В целом, 15% положительной в отношении вируса гриппа популяции заразились гриппом В; по данным различных исследований эта пропорция ранжируется от 1 до 33%. Средняя продолжительность заболевания у пациентов с гриппом В существенно не отличалась между группами лечения в различных исследованиях. Для проведения анализа данные обо всех 504 пациентах, зараженных гриппом В, включенных во все исследования, были объединены. Осельтамивир сокращал время, требуемое для исчезновения всех симптомов, на 0.7 дня (95% доверительный интервал 0.1- 1.6 дня; p=0.022) и продолжительность лихорадки (≥37.8°C), кашля и насморка на один день (95% доверительный интервал 0.4-1.7 дня; p < 0.001), по сравнению с плацебо.
Профилактика гриппа
Эффективность осельтамивира для профилактики гриппа, приобретенного естественным путем, была показана в исследовании профилактики после контакта в семьях и двух сезонных исследованиях профилактики. Во всех этих исследованиях первым показателем эффективности была частота возникновения лабораторно диагностируемого гриппа. Вирулентность вируса гриппа не прогнозируема и варьирует в пределах региона и от сезона к сезону, поэтому варьирует и количество людей, требующих лечения для предупреждения гриппа (number needed to treat — NNT).
Постконтактная профилактика.
В одном исследовании у лиц, находившихся в контакте с больными гриппом (12.6% были вакцинированы против гриппа), начинали применение осельтамивира 75 мг 1 раз/сут, в пределах двух суток после развития симптомов у больного и продолжали в течение 7 дней. Диагноз гриппа у больных был подтвержден в 163 случаях из 377. Осельтамивир существенно уменьшал частоту возникновения клинически выраженного гриппа у лиц, контактировавших со случаями подтвержденного гриппа, с 24/200 (12%) в группе плацебо до 2/205 (1%) в группе осельтамивира (92% уменьшение [95% доверительный интервал (ДИ) 6-16], p≤0.0001]). У лиц, контактировавших со случаями настоящего гриппа, количество случаев, значение NNT составляло 10 (95% CI 9-12) и у всех участников исследования (ITT) 16 (95% CI 15-19), вне зависимости от инфекции в первом случае.
Эффективность осельтамивира для предупреждения гриппа, полученного естественным путем, продемонстрирована в исследовании профилактики после контакта в семьях, где были взрослые, подростки и дети в возрасте от 1 до12 лет, как в качестве источников заражения, так и в качестве контактных лиц. Первичным показателем эффективности этого исследования была частота возникновения в семьях лабораторно и клинически диагностированного гриппа. Профилактика осельтамивиром продолжалась 10 дней. Во всей популяции частота возникновения лабораторно и клинически диагностированного гриппа в семьях уменьшилась с 20% (27/136) в группе не получавших профилактики, до 7% (10/135) в группе, получивших профилактику (62.7% уменьшение [95% ДИ 26-81.2; p=0.0042]). В семьях с источниками заражения гриппом частота возникновения гриппа уменьшилась с 26% (23/89) в группе не получавших профилактики до 11% (9/84) в группе, получавших профилактику (58.5% уменьшение [95% ДИ15.6-79.6; p = 0.0114]).
В соответствии с анализом подгруппы 1-12-летних детей, у них заметно уменьшалась частота возникновения лабораторно и клинически диагностированных случаев гриппа с 19% (21/111) в группе не получавших профилактику до 7% (7/104) в группе, получавших профилактику (64.4% уменьшение (95% ДИ 15.8-85; p=0.0188). Среди детей, которые еще не были заражены в начале исследования, частота возникновения лабораторно и клинически диагностированного гриппа уменьшилась с 21% (15/70) в группе, не получавших профилактику, до 4% (2/47) в группе, получавших профилактику (80.1% уменьшение (95% ДИ 22- 94.9; p=0.0206)). Во всей педиатрической популяции NNT составляло 9 (95% CI 7-24) и 8 (95% ДИ 6, верхняя граница не определяема) соответственно во всей популяции (ITT) и среди педиатрических контактных лиц источников заражения (ITTII).
Профилактика во время эпидемии гриппа среди населения.
В двух других исследованиях принимали участие невакцинированные и здоровые в других отношениях взрослые. Объединенный анализ этих исследований показал, что прием осельтамивира в дозе 75 мг 1 раз/сут в течение 6 недель значительно уменьшал частоту возникновения клинически выраженного гриппа с 25/519 (4.8%) в плацебо группе до 6/520 (1.2%) в группе осельтамивира (76% уменьшение (95% ДИ 1.6-5.7); p=0.0006) во время вспышки гриппа в популяции. NNT в этом исследовании составляло 28 (95% ДИ 24-50).
В исследовании, проведенном среди лиц пожилого возраста, проживающих в домах престарелых, где 80% участников были вакцинированы в соответствующем сезоне, применение осельтамивира в дозе 75 мг 1 раз/сут в течение 6 недель существенно уменьшало частоту возникновения клинически выраженного гриппа с 12/272 (4.4%) в группе плацебо до 1/276 (0.4%) в группе осельтамивира (92% уменьшение 95% [ДИ 1.5-6.6]; p=0,0015. NNT в этом исследовании составляло 25 (95% CI 23-62).
Профилактика гриппа у пациентов с иммунодефицитом.
Двойное слепое плацебо-контролируемое рандомизированное исследование сезонной профилактики гриппа проводилось у 475 пациентов с иммунодефицитом (388 пациентов с трансплантацией паренхиматозных органов (195 — плацебо,193 — осельтамивир), 87 пациентов с трансплантацией кроветворных стволовых клеток (43 — плацебо, 44 — осельтамивир), пациенты с другими иммунодепрессивными состояниями не исследовались), в т.ч. 18 детей в возрасте 1-12 лет. Основным критерием оценки в данном исследовании была частота возникновения лабораторно и клинически диагностированного гриппа, определяющаяся вирусной культурой, и/или 4-кратное увеличение HAI титра. Частота возникновения лабораторно и клинически диагностированного гриппа составила 2.9% (7/238) в группе плацебо и 2.1% (5/237) в группе осельтамивира (95% ДИ — 2.3% — 4.1%; р = 0.772).
Для оценки уменьшения риска возникновения осложнений никаких специфических исследований не проводилось.
Резистентность к осельтамивиру
Клинические исследования.
Риск появления вирусов гриппа со сниженной чувствительностью или выраженной устойчивостью к осельтамивиру был рассмотрен в ходе клинических исследований, спонсированных фирмой Рош. У всех пациентов носителей вируса, устойчивого к осельтамивиру, носительство было временным, клиренс вируса был нормальным, и не наблюдалось клинического ухудшения.
| Популяция пациентов | Пациенты с мутациями чувствительности (%) | |
| Определение фенотипа* | Определение гено- и фенотипа * | |
| Взрослые и подростки | 4/1245(0.32%) | 5/1245(0.4%) |
| Дети (1-12 лет) | 19/464(4.1%) | 25/464 (5.4%) |
*Полное определение генотипа не проводилось во всех исследованиях.
На данный момент отсутствуют доказательства возникновения лекарственной устойчивости, связанной с использованием Тамифлю в клинических исследованиях постконтактной (7 дней), постконтактной в группах домочадцев (10 дней) и сезонной (42 дня) профилактики гриппа у иммунокомпетентных пациентов. В течение 12-недельного исследования профилактики у пациентов с иммунодефицитом резистентность не наблюдалась
Клинические данные и данные наблюдений.
Естественные мутации, связанные со сниженной чувствительностью к осельтамивиру in vitro были обнаружены для вирусов гриппа А и В, выделенных у больных без воздействия осельтамивира. Резистентные штаммы, отобранные во время лечения осельтамивиром, были выделены как у иммунокомпетентных пациентов, так и у пациентов с иммунодефицитом. Пациенты с иммунодефицитом и дети раннего возраста имеют более высокий риск развития устойчивых к осельтамивиру вирусов во время лечения.
Устойчивые к осельтамивиру вирусы, выделенные у пациентов, получавших осельтамивир, и устойчивые к осельтамивиру лабораторные штаммы вирусов гриппа имели мутации нейраминидазы N1 и N2. Мутации устойчивости имели тенденцию быть специфичными к подтипам вируса. С 2007 года устойчивость, связанная с мутацией H275Y сезонных штаммов H1N1 стала широко распространенной. Восприимчивость к осельтамивиру и распространение таких вирусов меняются в зависимости от сезона и местности. В 2008 году H275Y была найдена у > 99% циркулирующих штаммов гриппа H1N1 в Европе. В 2009 году грипп H1N1 («свиной грипп») был почти равномерно чувствителен к осельтамивиру, были отмечены только спорадические сообщения об устойчивости, как при лечебном, так и при профилактическом режиме.
Результаты доклинических исследований
Стандартные доклинические исследования фармакологической безопасности, хронической токсичности и генотоксичности не продемонстрировали вредного воздействия на человека.
Обычные исследования канцерогенности на крысах продемонстрировали зависимую от дозы тенденцию учащения возникновения некоторых опухолей, которые являются типичными для видов грызунов, на которых проводилось исследование. Сравнивая допустимые границы концентраций с концентрациями, которые ожидаются при приеме в дозах предполагаемых для людей, эти данные не изменяют соотношение риска и пользы при применении Тамифлю® по зарегистрированным показаниям.
Изучение тератогенности было проведено на крысах и кроликах соответственно в дозах до 1500 мг/кг/сут и 500 мг/кг/сут. Не отмечалось повреждающего действия на развитие плода. У крыс было проведено исследование фертильности с дозами до 1500 мг/кг/сут, которое не продемонстрировало неблагоприятного влияния на какой-либо пол. В пре- и постнатальном исследовании, проведенном на крысах при дозе 1500 мг/кг/сут отмечалось удлинение родов:
- граница безопасности между концентрацией, достигаемой у человека и наивысшей дозой (500 мг/кг/сут) у крыс была 480-кратной для осельтамивира и 44-кратной для активного метаболита. Концентрация осельтамивира в крови у плода крыс и кроликов составляла примерно 15-20% от материнской.
У лактирующих крыс осельтамивир и активный метаболит выделяются с грудным молоком. Ограниченные данные показывают, что осельтамивир и его активный метаболит выделяются с грудным молоком у человека. На основании данных, полученных в опытах на животных, производные значения составляют 0.01 мг/сут и 0.3 мг/сут.У морских свинок исследовалось возникновение сенсибилизации кожи в отношении осельтамивира с помощью теста «максимизации». Приблизительно у 50% животных, получавших лечение осельтамивиром, возникла эритема. У кроликов отмечалось преходящее раздражение глаз.
Осельтамивира фосфат в очень высоких однократных пероральных дозах (до 1310 мг/кг) не оказывал воздействия на взрослых крыс, однако эти дозы были токсичны у молодых 7-дневных крысят, вызывая в числе прочего и смертельные случаи. Эти эффекты отмечали при дозах 657 мг/кг и более. При применении дозы 500 мг/кг неблагоприятных реакций не отмечено, в т.ч. и при хроническом введении в дозе 500 мг/кг/сут с 7 по 21 день постнатального периода.
Применение препарата Тамифлю
Во время доклинических исследований осельтамивир и активный метаболит проникал в молоко лактирующих крыс. Происходит ли экскреция осельтамивира или активного метаболита с молоком у человека — неизвестно, но их количество в грудном молоке может составлять 0,01 и 0,3 мг/сут соответственно. Так как данных по применению препарата у беременных женщин недостаточно, Тамифлю следует назначать во время беременности или кормящим матерям только в том случае, если возможные преимущества от его применения превышают потенциальный риск для плода или грудного ребенка. Внутрь, во время еды или независимо от приема пищи. Переносимость препарата можно улучшить, если принимать его во время еды. Приготовление суспензии:
- Осторожно несколько раз постучать пальцем по закрытому флакону с тем, чтобы порошок распределился на дне флакона.
- Отмерить 52 мл воды, используя мерный стаканчик, заполняя его до указанного уровня.
- Добавить 52 мл воды во флакон, закрыть колпачком и хорошо встряхивать в течение 15 сек.
- Снять колпачок и вставить в горлышко флакона адаптер.
- Плотно завинтить флакон колпачком для обеспечения правильного расположения адаптера.
На этикетке флакона следует указать дату окончания срока годности приготовленной суспензии. Перед применением флакон с приготовленной суспензией необходимо взбалтывать. Для дозировки суспензии прилагается дозирующий шприц с метками, указывающими уровни доз 30, 45 и 60 мг (см. «Форма выпуска и упаковка»). В случаях, когда у взрослых, подростков ≥12 лет и детей с массой тела >40 кг или ≥8 лет существует проблема с проглатыванием капсул, а порошок для приготовления суспензии для приема внутрь Тамифлю отсутствует, или при наличии признаков «старения» капсул, необходимо открыть капсулу и высыпать ее содержимое в небольшое количество (максимально 1 ч.ложка) подходящего подслащенного продукта питания (шоколадный сироп (с нормальным содержанием сахара или без содержания сахара), мед, светло-коричневый сахар или столовый сахар, растворенный в воде, сладкий десерт, сгущенное молоко с сахаром, яблочное пюре или йогурт) для того, чтобы скрыть горький вкус. Смесь необходимо тщательно перемешать и дать пациенту целиком. Следует проглотить смесь сразу же после приготовления. Подробные рекомендации даны ниже (см.«Экстемпоральное приготовление суспензии Тамифлю»). Стандартный режим дозирования Лечение Прием препарата необходимо начинать не позднее 2 сут от момента развития симптомов заболевания. Взрослые и подростки ≥12 лет По 75 мг (капсулы или суспензия) 2 раза в сутки внутрь в течение 5 дней. Увеличение дозы более 150 мг/сут не приводит к усилению эффекта. Дети >40 кг или ≥8 лет Дети, которые умеют проглатывать капсулы, также могут получать лечение, принимая по 1 капс. 75 мг 2 раза в сутки, в качестве альтернативы к рекомендованной дозе Тамифлю суспензии (см. ниже). Дети ≥1 года
Таблица 1 Рекомендованный режим дозирования Тамифлю суспензии для приема внутрь
Вес, кг | Рекомендованная доза в течение 5 дней (2 раза в сутки, мг) |
| ≤15 | 30 |
| >15-23 | 45 |
| >23-40 | 60 |
| >40 | 75 |
Для дозирования суспензии использовать прилагающийся шприц с метками 30, 45 и 60 мг. Необходимое количество суспензии отобрать из флакона дозирующим шприцем, перенести в мерный стаканчик и принимать внутрь.
Профилактика Взрослые и подростки ≥12 лет По 75 мг 1 раз в сутки в течение не менее 10 дней после контакта с инфицированным. Прием препарата нужно начинать не позднее чем в первые 2 дня после контакта. Во время сезонной эпидемии гриппа — по 75 мг 1 раз в сутки в течение 6 нед. Профилактическое действие продолжается столько, сколько длится прием препарата. Дети >40 кг Дети, которые могут проглатывать капсулы, также могут получать профилактическую терапию, принимая по 1 капс. 75 мг 1 раз в сутки в качестве альтернативы к рекомендованной дозе Тамифлю суспензии (см. ниже). Дети ≥1 года
Таблица 2 Рекомендованный режим дозирования Тамифлю суспензии для приема внутрь
Вес, кг | Рекомендованная доза в течение 10 дней (1 раз в сутки, мг) |
| ≤15 | 30 |
| >15-23 | 45 |
| >23-40 | 60 |
| >40 | 75 |
Для дозирования суспензии использовать прилагающийся шприц с метками 30, 45 и 60 мг. Необходимое количество суспензии отобрать из флакона дозирующим шприцем, перенести в мерный стаканчик и принимать внутрь.
Дозирование в особых случаях Больные с поражением почек Лечение. Больным с Cl креатинина >30 мл/мин коррекция дозы не требуется. У больных с Cl креатинина от 10 до 30 мл/мин дозу Тамифлю следует уменьшить до 75 мг 1 раз в сутки в течение 5 дней. Рекомендации по дозированию у пациентов, находящихся на постоянном гемодиализе или хроническом перитонеальном диализе по поводу терминальной стадии хронической почечной недостаточности, и для больных с Cl креатинина ≤10 мл/мин отсутствуют. Профилактика. Больным с Cl креатинина >30 мл/мин коррекция дозы не требуется. У больных с Cl креатинина от 10 до 30 мл/мин рекомендуется уменьшить дозу Тамифлю до 75 мг через день или 30 мг суспензии ежедневно. Рекомендации по дозированию у пациентов, находящихся на постоянном гемодиализе или хроническом перитонеальном диализе по поводу терминальной стадии хронической почечной недостаточности, и для больных с Cl креатинина ≤10 мл/мин отсутствуют. Больные с поражением печени. Коррекция дозы при лечении и профилактике гриппа у пациентов с нарушением функции печени легкой и средней степени тяжести не требуется. Безопасность и фармакокинетика Тамифлю у пациентов с тяжелыми нарушениями функции печени не изучалась. Больные старческого возраста. Коррекция дозы для профилактики или лечения гриппа не требуется. Дети. Безопасность и эффективность Тамифлю у детей до 1 года не установлены. Экстемпоральное приготовление суспензии Тамифлю В случаях, когда у взрослых, подростков и детей существует проблема с проглатыванием капсул, а порошок для приготовления суспензии для приема внутрь Тамифлю отсутствует или при наличии признаков «старения» капсул, необходимо открыть капсулу и высыпать ее содержимое в небольшое количество (максимально 1 ч.ложка) подходящего подслащенного продукта питания (см. выше) для того, чтобы скрыть горький вкус. Смесь необходимо тщательно перемешать и дать принять пациенту полностью. Следует принять смесь сразу же после приготовления. Если пациентам требуется доза 75 мг, то необходимо следовать следующим инструкциям:
- Одну капсулу 75 мг Тамифлю аккуратно раскрыть над маленькой емкостью и высыпать порошок в емкость.
- Добавить небольшое количество (не более 1 ч.ложки) подходящего подслащенного продукта питания (чтобы скрыть горький вкус) и хорошо перемешать.
- Тщательно перемешать смесь и дать все содержимое емкости пациенту. Следует принять смесь сразу же после приготовления. Если в емкости осталось небольшое количество смеси, то следует ополоснуть емкость небольшим количеством воды и напоить пациента оставшейся смесью.
Если пациентам требуются дозы 30–60 мг, то для правильного дозирования необходимо следовать следующим инструкциям:
- Одну капсулу 75 мг Тамифлю аккуратно раскрыть над маленькой емкостью и высыпать порошок в емкость.
- Добавить в порошок 5 мл воды с помощью шприца с метками, показывающими количество набранной жидкости. Тщательно перемешать в течение 2 мин.
- Набрать в шприц необходимое количество смеси из чашки согласно таблице 3. Нет необходимости в заборе нерастворенного белого порошка, поскольку он является неактивным наполнителем. Нажав на поршень шприца, ввести все его содержимое во вторую емкость. Оставшуюся неиспользованную смесь необходимо выбросить.
- Во вторую емкость добавить небольшое количество (не более 1 ч.ложки) подходящего подслащенного продукта питания, чтобы скрыть горький вкус, и хорошо перемешать.
- Тщательно перемешать смесь и дать все содержимое второй емкости пациенту. Следует принять смесь сразу же после приготовления. Если в емкости осталось небольшое количество смеси, то следует ополоснуть емкость небольшим количеством воды и напоить пациента оставшейся смесью.
Повторяйте данную процедуру перед каждым приемом препарата.
Таблица 3 Рекомендованный режим дозирования суспензии Тамифлю для приема внутрь экстемпорального приготовления
Вес, кг | Рекомендованная доза, мг | Количество смеси на 1 прием, мл |
| ≤15 | 30 | 2 |
| >15-23 | 45 | 3 |
| >23-40 | 60 | 4 |
Опыт применения осельтамивира (тамифлю) при гриппе и ОРВИ у детей
Ежегодно от гриппа и его осложнений умирает более полумиллиона человек [1]. Самым эффективным способом снижения заболеваемости является специфическая вакцинопрофилактика. Но так как вирусы гриппа обладают способностью к антигенной изменчивости поверхностных белков гемагглютинина и нейраминидазы, разработчики вакцин вынуждены ежегодно создавать новые антигенные препараты, выпуск которых занимает как минимум 9 мес, в связи с чем нельзя гарантировать полного соответствия вакцины и циркулирующего штамма [2]. (Кроме того, учитывая возникшую угрозу нового пандемического штамма птичьего гриппа (H5N1), который может появиться достаточно внезапно, встает вопрос о необходимости применения эффективных этиотропных химиопрепаратов.)
В настоящее время класс противогриппозных препаратов включает адамантадины амантадин и римантадин, действие которых направлено на ионные каналы М2 и ингибиторы нейраминидазы осельтамивир и занамивир [3]. Однако адамантадины в настоящее время на 30–60% оказываются неэффективными. Так, за 10 лет наблюдения частота случаев лекарственной устойчивости выросла с 0,4% в 1995 г. до 12,3% в 2004 г. Развитие резистентности к обоим препаратам связано с мутацией вируса гриппа А, в результате которой функция ионного канала белка М2 оказалась защищенной от действия адамантадинов [4, 5, 6, 7, 8].
Напротив, мутации, необходимые для развития устойчивости к ингибиторам нейраминидазы, происходят в труднодоступном участке молекулы фермента нейраминидазы, что снижает ее активность и возможность развития резистентности, обусловливая тем самым активность ингибиторов этого фермента в отношении всех подтипов вирусов А и В.
Первым препаратом в этой группе был занамивир, предназначенный для местного применения в виде ингаляции, но не оказывающий системного воздействия при гриппе, что послужило причиной разработки нового лекарственного средства — осельтамивира (тамифлю). По данным литературы, применение тамифлю при гриппе у взрослых больных уменьшает тяжесть заболевания, сокращает период клинических проявлений, уменьшает частоту осложнений, требующих применения антибактериальных средств [9, 10, 11, 12, 13]. Однако информации по применению тамифлю у детей собрано немного, что послужило целью настоящего исследования по изучению клинической эффективности и безопасности этого препарата при гриппе и других респираторных инфекциях у детей.
Под наблюдением находились 50 детей в возрасте от 12 до 15 лет, 25 из которых получали тамифлю (основная группа) и 25 — общепринятое лечение (группа контроля). К категории часто болеющих относились 34% детей. У 9 детей имелась хроническая патология: у 1 — рецидивирующий обструктивный бронхит, у 1 — бронхиальная астма, у 7 — хронический тонзиллит, у 2 — поллиноз.
По совокупности клинических данных грипп можно было диагностировать у 16 больных основной и у 14 — контрольной групп, парагрипп — у 9 и у 11 больных, аденовирусную инфекцию — у 8 и у 6 больных соответственно.
Препарат тамифлю в дозе 75 мг назначали в остром периоде болезни по 2 раза в день не позднее первых 30 ч заболевания в течение 5 дней на фоне сопутствующей симптоматической терапии. Дети из группы контроля с первого дня обращения к врачу получали антигистаминные, жаропонижающие, муколитические препараты, а 13 из них, помимо симптоматического лечения, получали антибиотики в связи с возникновением у них бактериальных осложнений.
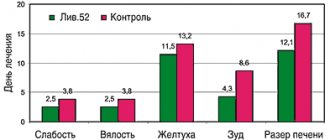
У больных, лечившихся тамифлю, отмечена достоверно меньшая продолжительность клинических симптомов, независимо от тяжести ОРВИ (рисунок, а).
Как видно из приведенных данных, продолжительность лихорадки и других проявлений интоксикационного синдрома (недомогание, снижение аппетита, слабость, сонливость, снижение физической активности) сокращалась в 3 и более раз; ринита — в 2,6 раза; на фоне терапии тамифлю продуктивный кашель с эффектом разжижения мокроты появлялся со 2–3-го дня, а в группе контроля — после 4-го дня. Максимальный клинический эффект среди больных ОРВИ отмечался у 72% детей уже на вторые сутки приема препарата. В эти же сроки у 67% детей отмечалось изменение плотности мокроты в сторону ее разжижения, в то время как в группе контроля эти изменения регистрировались только у 43% детей.
У больных ОРВИ из группы контроля с бактериальными осложнениями продолжительность лихорадки и других проявлений интоксикационного синдрома уменьшились в 4,4 раза; продолжительность ринита — в 3,2 раза; продуктивный кашель с эффектом разжижения мокроты появлялся на фоне лечения тамифлю в среднем со 2-го дня, а в группе контроля — с 5-го дня (рисунок, б).
Переносимость препарата у всех детей была хорошей. Побочных реакций в виде болей в животе, тошноты, рвоты, диспепсических явлений, ощущения комка или инородного тела, сухости/саднения в горле, связанных с получением тамифлю, не отмечалось. На фоне терапии тамифлю не было выявлено аллергических реакций. У детей, страдающих атопическим дерматитом, поллинозом, бронхиальной астмой, не отмечалось также усугубления проявлений заболевания.
Проведенное исследование показало, что препарат тамифлю безвреден, хорошо переносится, эффективен при лечении не только гриппа, но и ОРВИ. Механизм клинического улучшения при ОРВИ на фоне лечения тамифлю не совсем ясен. Поскольку в ходе лечения препаратом (по 75 мг 2 раза в день в течение 5 дней) у всех детей, независимо от этиологии заболевания, отмечали значительное улучшение самочувствия и быструю обратную динамику клинических проявлений, можно допустить, что тамифлю ингибирует не только нейраминидазу, но и другие факторы патогенности вирусов. Несомненно, клинический эффект препарата напрямую связан с подавлением вирусной агрессии, а это, как известно, ведет к уменьшению уровня провоспалительных цитокинов, количества клеток, экспрессирующих CD95+, снижению адгезивной способности мононуклеарных клеток крови, к активации лимфоцитов, целенаправленной поляризации Th-0-лимфоцитов в Th-1, экспрессии на мембране клеток HLA-DR 11 класса, стимуляции фагоцитарной системы макрофагов и нейтрофилов, росту и активации цитотоксических и NK-клеток [14, 15, 16].
Такие сдвиги в иммунной системе способствуют подавлению бактериальной и грибковой флоры, определяя неосложненное течение заболевания.
Наши данные согласуются с информацией других авторов. Так, по данным L. Kaiser (2003), при применении тамифлю не только быстрее разрешаются симптомы основного заболевания, но и снижаются на 55%, по сравнению с плацебо, частота вторичных осложнений со стороны нижних дыхательных путей, а также число госпитализаций. У пациентов повышенного риска частота бактериальных осложнений, требующих назначения антибиотикотерапии, уменьшалась на 34%, а число госпитализаций — на 59% [17].
По данным C. M. Machado (2004), у больных с ослабленным в результате пересадки костного мозга иммунитетом не только отмечалась высокая эффективность при применении тамифлю, но и его хорошая переносимость [18].
В работе R. J. Whitley (2001 г.) показана эффективность тамифлю у детей в возрасте 1 года и старше. У детей, получавших препарат, выздоровление наступало на 36 ч раньше, чем в контрольной группе. При этом на 44% снизилась частота бактериальных осложнений, у детей с бронхиальной астмой наблюдалось достоверное увеличение объема форсированного выдоха за 1 с [19].
На основании результатов нашего исследования можно сделать следующие выводы.
- Осельтамивир (тамифлю) можно считать препаратом выбора при лечении гриппа и других респираторных инфекций.
- Современная этиотропная терапия гриппа и ОРВИ препаратом тамифлю способствует сокращению продолжительности лихорадки, явлений интоксикации, а также сроков купирования катаральных явлений.
- При системной терапии осельтамивиром (тамифлю) не отмечается развитие обструкции дыхательных путей и бактериальных осложнений, что позволяет избежать госпитализации в стационар и отказаться от назначения антибактериальной терапии.
- Случаев гиперчувствительности к тамифлю не выявлено, препарат хорошо переносится и не имеет противопоказаний.
- Осельтамивир (тамифлю) при гриппе и других респираторных инфекциях необходимо назначать по 75 мг 2 раза в день в течение 5 дней у детей старше 12 лет, в остром периоде заболевания — не позднее чем через 48 ч с момента появления первых симптомов.
По вопросам литературы обращайтесь в редакцию.
О. В. Кладова, доктор медицинских наук Т. Ф. Погодина В. Ф. Учайкин, доктор медицинских наук, профессор, академик РГМУ, Москва
Побочные эффекты препарата Тамифлю
Взрослые. Самые частые — тошнота и рвота (обычно после приема первой дозы; носят транзиторный характер и в большинстве случаев не требуют отмены препарата). Побочные действия (≥1%): диарея, бронхит, боли в животе, головокружение, головная боль, кашель, нарушения сна, слабость; боли различной локализации, ринорея, диспепсия и инфекции верхних дыхательных путей. Дети. Самое частое — рвота. Боль в животе, носовое кровотечение, нарушения со стороны органа слуха, конъюнктивит (возникали внезапно, прекращались, несмотря на продолжение лечения, и в подавляющем большинстве случаев не послужили причиной прекращения лечения), тошнота, диарея, астма (включая обострение), острый средний отит, пневмония, синусит, бронхит, дерматит, лимфаденопатия. Постмаркетинговое наблюдение Со стороны кожи и подкожной клетчатки: редко — реакции гиперчувствительности: дерматит, кожная сыпь, экзема, крапивница, очень редко — мультиформная эритема, синдром Стивенса-Джонсона и токсический эпидермальный некролиз, анафилактические и анафилактоидные реакции, отек Квинке. Со стороны печени: очень редко — гепатит, увеличение печеночных ферментов. Со стороны нервно-психической сферы: у пациентов (в основном у детей и подростков), принимавших Тамифлю с целью лечения гриппа, были зарегистрированы судороги и делирий (включая такие симптомы, как нарушение сознания, дезориентация во времени и пространстве, анормальное поведение, бред, галлюцинации, возбуждение, тревога, ночные кошмары). Эти случаи редко сопровождались опасными для жизни действиями. Роль Тамифлю в развитии этих явлений неизвестна. Подобные психоневрологические нарушения так же отмечены у пациентов с гриппом, не получавших Тамифлю. Со стороны ЖКТ: редко наблюдались случаи желудочно-кишечных кровотечений в период лечения Тамифлю (в частности нельзя исключить связь между явлениями исчезали как после выздоровления пациента от гриппа, как и после отмены препарата).
Особые указания по применению препарата Тамифлю
У пациентов (в основном детей и подростков), принимавших Тамифлю с целью лечения гриппа, были зарегистрированы судороги и делирий-подобные психоневрологические нарушения. Эти случаи сопровождались опасными для жизни действиями. Роль Тамифлю в развитии этих явлений неизвестна. Подобные психоневрологические нарушения так же отмечены у пациентов с гриппом, не получавших Тамифлю. Рекомендуется тщательное наблюдение за поведением пациентов, особенно детей и подростков, с целью выявления признаков анормального поведения. Данных по эффективности Тамифлю при любых заболеваниях, вызванных другими возбудителями, кроме вирусов гриппа А и В, нет. При лечении и профилактике гриппа у больных с Cl креатинина от 10 до 30 мл/мин требуется коррекция дозы. Рекомендации по коррекции дозы у больных, получающих гемодиализ или перитонеальный диализ, и у пациентов с Cl креатинина ≤10 мл/мин отсутствуют. Во флаконе 30 г Тамифлю с порошком для приготовления суспензии содержится 25,713 г сорбитола. При приеме 45 мг Тамифлю 2 раза в сутки в организм поступает 2,6 г сорбитола. У пациентов с врожденной непереносимостью фруктозы это количество превышает дневную норму сорбитола. После приготовления суспензию хранить при температуре 2–8 °C в течение 17 дней или при температуре не выше 25 °C в течение 10 дней. Не использовать суспензию по истечении срока хранения.
Взаимодействия препарата Тамифлю
Клинически значимые лекарственные взаимодействия маловероятны. Лекарственные взаимодействия, обусловленные конкуренцией и связыванием с активными центрами эстераз, превращающих осельтамивира фосфат в активное вещество, не представлены. Низкая степень связывания осельтамивира и активного метаболита с белками не дают оснований предполагать наличие взаимодействий, связанных с вытеснением ЛС из связывания с белками. In vitro осельтамивира фосфат и активный метаболит не являются предпочтительным субстратом для полифункциональных оксидаз системы цитохрома Р450 или для глюкуронилтрансфераз (см. «Фармакокинетика»). Оснований для взаимодействия с пероральными контрацептивами нет. Циметидин, неспецифический ингибитор изоферментов системы цитохрома Р450, амоксициллин и парацетамол не влияют на плазменные концентрации осельтамивира и его активного метаболита. Пробенецид приводит к увеличению AUC активного метаболита осельтамивира примерно в 2 раза, но коррекции дозы при одновременном применении с пробенецидом не требуется. При назначении Тамифлю вместе с ингибиторами АПФ (эналаприл, каптоприл), тиазидными диуретиками (бендрофлюазид), антибиотиками (пенициллин, цефалоспорины, азитромицин, эритромицин и доксициклин), блокаторами Н2-рецепторов к гистамину (ранитидин, циметидин), бета-адреноблокаторами (пропранолол), ксантинами (теофиллин), симпатомиметиками (псевдоэфедрин), опиатами (кодеин), кортикостероидами, ингаляционными бронхолитиками и анальгетиками (аспирин, ибупрофен и парацетамол) изменений характера или частоты нежелательных явлений не наблюдалось.
Тамифлю 75 мг №10 капс.
Инструкция по медицинскому применению лекарственного средства Тамифлю Торговое название Тамифлю Международное непатентованное название Осельтамивир Лекарственная форма Капсулы 75 мг Состав Одна капсула содержит активное вещество — осельтамивира фосфата 98,50 (эквивалентно осельтамивиру) (75.00) вспомогательные вещества: крахмал прежелатинизированный, повидон К30, натрия кроскармеллоза, тальк, натрия стеарилфумарат, состав капсулы: корпус – железа (III) оксид черный Е 172, титана диоксид Е 171, желатин; крышечка – железа (III) оксид красный Е 172, железа (III) оксид желтый Е 172, титана диоксид Е 171, желатин; чернила печатные. Описание Твердые желатиновые капсулы, размер № 2, с непрозрачным корпусом серого цвета и непрозрачной крышечкой светло-желтого цвета, с маркировкой синего цвета «ROCHE» на корпусе и «75 mg» на крышечке. Содержимое капсулы — порошок от белого до желтовато-белого цвета. Фармакотерапевтическая группа Противовирусные препараты прямого действия. Ингибиторы нейраминидазы. Код АТС J05AH02 Фармакологические свойства Фармакокинетика После перорального приема осельтамивира фосфат легко всасывается в желудочно-кишечном тракте и в высокой степени превращается в активный метаболит под действием печеночных эстераз. Концентрации активного метаболита в плазме определяются в пределах 30 минут, достигают почти максимального уровня через 2–3 часа после приема и существенно (более, чем в 20 раз) превышают концентрации про-лекарства. Не менее 75% принятой внутрь дозы попадает в системный кровоток в виде активного метаболита, менее 5% – в виде исходного препарата. Плазменные концентрации как про-лекарства, так и активного метаболита пропорциональны дозе и не зависят от приема пищи. Cредний объем распределения (Vss) активного метаболита составляет примерно 23 литров. Связывание активного метаболита с белками плазмы крови незначительно (около 3%). Связывание про-лекарства с белками плазмы крови составляет 42%, что недостаточно, чтобы служить причиной существенных лекарственных взаимодействий. Осельтамивира фосфат в высокой степени превращается в активный метаболит под действием эстераз, находящихся преимущественно в печени и кишечнике. Ни осельтамивира фосфат, ни активный метаболит не являются субстратами или ингибиторами изоферментов системы цитохрома Р450. Всосавшийся осельтамивир выводится, главным образом (>90%), путем превращения в активный метаболит. Активный метаболит не подвергается дальнейшей трансформации и выводится с мочой (>99%). У большинства пациентов период полувыведения активного метаболита из плазмы составляет 6–10 часов. Активный метаболит выводится полностью (>99%) путем почечной экскреции. Почечный клиренс (18,8 л/час) превышает скорость клубочковой фильтрации (7,5 л/час), что указывает на то, что препарат выводится еще и путем канальцевой секреции. С калом выводится менее 20% принятого внутрь радиоактивно меченного препарата. Фармакокинетика в особых группах Больные с поражением почек При назначении Тамифлю по 100 мг 2 раза в сутки в течение 5 дней больным с различной степенью поражения почек площади под кривой «концентрации активного метаболита в плазме – время» (AUC) обратно пропорциональны снижению функции почек. Фармакокинетика осельтамивира у пациентов с терминальной стадией почечной недостаточности (с клиренсом креатинина ≤10 мл/мин), не находящихся на диализе, не изучалась. Больные с поражением печени Исследование in vitro показали, что у пациентов с печеночной патологией величина AUC осельтамивира фосфата значительно не повышена, а AUC активного метаболита не снижена. Больные старческого возраста У больных старческого возраста (65–78 лет) AUC активного метаболита в равновесном состоянии была на 25–35% выше, чем у более молодых пациентов при назначении аналогичных доз Тамифлю. Период полувыведения препарата у пожилых существенно не отличался от такового у более молодых пациентов взрослого возраста. С учетом данных по AUC препарата и переносимости, больным старческого возраста коррекции дозы при лечении и профилактике гриппа не требуется. Дети Фармакокинетику Тамифлю изучали у детей от 1 года и до 16 лет в фармакокинетическом исследовании с однократным приемом препарата и в клиническом исследовании у небольшого числа детей в возрасте 3–12 лет. У детей младшего возраста выведение пролекарства и активного метаболита шло быстрее, чем у взрослых, что приводило к более низким AUC по отношению к конкретной дозе. Прием препарата в дозе 2 мг/кг дает такую же AUC осельтамивира карбоксилата, какая достигается у взрослых после однократного приема капсулы с 75 мг препарата (что эквивалентно примерно 1 мг/кг). Фармакокинетика осельтамивира у детей старше 12 лет такая же, как у взрослых. У детей 6-12 месяцев назначение осельтамивира в дозировке 3 мг/кг дважды в сутки обеспечивает плазменный уровень активного метаболита, аналогичный уровню, демонстрирующему клиническую эффективность у детей старшего возраста и взрослых. Фармакодинамика Противовирусный препарат. Осельтамивира фосфат является пролекарством, его активный метаболит (осельтамивира карбоксилат) конкурентно и избирательно ингибирует нейраминидазу вирусов гриппа типа А и В – фермент, катализирующий процесс высвобождения вновь образованных вирусных частиц из инфицированных клеток, их проникновения в клетки эпителия дыхательных путей и дальнейшего распространения вируса в организме. Осельтамивира карбоксилат действует вне клеток. Угнетает рост вируса гриппа in vitro и подавляет репликацию вируса и его патогенность in vivo, уменьшает выделение вирусов гриппа А и В из организма. Его концентрации, необходимые для подавления активности фермента на 50% (IC50), находятся у нижней границы наномолярного диапазона. При приеме Тамифлю с целью пост-контактной (7 дней) и сезонной (42 дня) профилактики гриппа резистентности к препарату не отмечается. Частота транзиторного выделения вируса гриппа со сниженной чувствительностью нейраминидазы к осельтамивира карбоксилату у взрослых больных гриппом составляет 0.4%. Элиминация резистентного вируса из организма пациентов, получающих Тамифлю, происходит без ухудшения клинического состояния больных. Показания к применению — лечение гриппа у взрослых и детей, включая доношенных новорожденных, у которых наблюдаются симптомы гриппа, когда вирус гриппа циркулирует среди населения. Эффективность была продемонстрирована при начале лечения в течение 2 дней после первого появления симптомов гриппа. — профилактика гриппа у взрослых и детей: — профилактика гриппа у взрослых и детей старше 1 года после случаев контакта с лицами с клинически подтвержденным гриппом, когда вирус гриппа циркулирует среди населения — профилактика гриппа у детей младше 1 года во время пандемии гриппа. Способ применения и дозы Тамифлю принимается внутрь, во время еды или независимо от приема пищи. У некоторых пациентов переносимость препарата улучшается, если его принимают во время еды. Лечение нужно начинать в первый или второй день появления симптомов гриппа. В случаях, когда у взрослых, подростков ≥12 лет и детей с массой тела > 40 кг или ≥8 лет существует проблема с проглатыванием капсул, необходимо открыть капсулу и высыпать ее содержимое в небольшое количество (максимально 1 чайная ложка) подходящего подслащенного продукта питания (шоколадный сироп (с нормальным содержанием сахара или без содержания сахара), мед, растворенный в воде, сладкий десерт, сгущенное молоко с сахаром, яблочное пюре или йогурт) для того, чтобы скрыть горький вкус. Смесь необходимо тщательно перемешать и дать пациенту целиком. Следует проглотить смесь сразу же после приготовления. Стандартный режим дозирования Взрослые и подростки старше 13 лет (с массой тела более 40 кг): Лечение гриппа: Рекомендованный режим дозирования Тамифлю – по одной капсуле 75 мг 2 раза в сутки внутрь в течение 5 дней или по 75 мг суспензии 2 раза в сутки внутрь в течение 5 дней. Профилактика гриппа: Рекомендованная доза Тамифлю для профилактики гриппа после контакта с инфицированным лицом – по 75 мг 1 раз в сутки внутрь в течение 10 дней. Прием препарата нужно начинать не позднее, чем в первые 2 дня после контакта. Рекомендованная доза для профилактики во время сезонной эпидемии гриппа – по 75 мг 1 раз в сутки; показана эффективность и безопасность препарата при приеме его в течение 6 недель. Профилактическое действие продолжается столько, сколько длится прием препарата. Дети от 1 года до 12 лет: Лечение гриппа: Масса тела Рекомендуемая дозировка в течение 5 дней: 10 – 15 кг 30 мг два раза в день 15 – 23 кг 45 мг два раза в день 23 – 40 кг 60 мг два раза в день > 40 кг 75 мг два раза в день Профилактика гриппа: Масса тела Рекомендуемая дозировка в течение 10 дней: 10 – 15 кг 30 мг один раз в день 15 – 23 кг 45 мг один раз в день 23 – 40 кг 60 мг один раз в день > 40 кг 75 мг один раз в день Эффективность Тамифлю для профилактики во время сезонной эпидемии гриппа у детей младше 12 лет не изучалась. Дети до 1 года Лечение гриппа: Рекомендованная доза для детей в возрасте до 1 года составляет 3 мг/кг массы тела дважды в день. Масса тела Рекомендуемая дозировка в течение 5 дней: 3 кг 9 мг два раза в день 4 кг 12 мг два раза в день 5 кг 15 мг два раза в день 6 кг 18 мг два раза в день 7 кг 21 мг два раза в день 8 кг 24 мг два раза в день 9 кг 27 мг два раза в день 10 кг 30 мг два раза в день Данный режим дозирования неприменим к недоношенным новорожденным (т.е., рожденным в срок до 36 недель). По дозированию у данной группы пациентов имеется недостаточное количество данных. Профилактика гриппа: Рекомендованная доза Тамифлю для профилактики гриппа во время пандемии у детей младше 1 года составляет половину лечебной дозы – 3 мг/кг один раз в день в течение 10 дней. Эффективность Тамифлю для профилактики во время сезонной эпидемии гриппа у детей младше 1 года не изучалась. Дозирование в особых случаях Больные с поражением почек Лечение гриппа. Больным с клиренсом креатинина более 30 мл/мин коррекция дозы не требуется. У больных с клиренсом креатинина от 10 до 30 мл/мин дозу Тамифлю следует уменьшить до 75 мг один раз в сутки в течение 5 дней. Пациентам, находящимся на хроническом гемодиализе, Тамифлю может быть назначен в дозе 30 мг перед сеансом диализа. Для поддержания концентрации осельтамивира в плазме Тамифлю в дозе 30 мг должен назначаться после каждого сеанса гемодиализа. При перитонеальном диализе Тамифлю назначается в дозе 30 мг перед сеансом диализа, а затем в течение 5 дней по 30 мг в сутки. У пациентов с терминальной стадией хронической почечной недостаточности (клиренс креатинина менее 10 мл/мин), не находящихся на гемодиализе, фармакокинетика осельтамивира не изучалась. Профилактика гриппа. Больным с клиренсом креатинина более 30 мл/мин коррекция дозы не требуется. У больных с клиренсом креатинина от 10 до 30 мл/мин дозу Тамифлю следует уменьшить до 75 мг через день или же до 30 мг каждый день. Пациентам, находящимся на хроническом гемодиализе, Тамифлю может быть назначен в дозе 30 мг перед сеансом диализа. Для поддержания концентрации осельтамивира в плазме Тамифлю в дозе 30 мг должен назначаться через один сеанс гемодиализа, в конце процедуры. При перитонеальном диализе Тамифлю назначается в дозе 30 мг перед сеансом диализа, а затем каждые 7 дней по 30 мг. Больные с поражением печени Коррекция дозы при лечении и профилактике гриппа не требуется. Больные пожилого возраста Коррекция дозы при лечении и профилактике гриппа не требуется. Экстемпоральное приготовление Тамифлю В случаях, когда у взрослых, подростков и детей существует проблема с проглатыванием капсул, а Тамифлю в лекарственной форме «порошок для приготовления суспензии для приема внутрь» отсутствует или при наличии признаков «старения» капсул, необходимо открыть капсулу и высыпать ее содержимое в небольшое количество (максимально 1 чайная ложка) подходящего подслащенного продукта питания для того, чтобы скрыть горький вкус. Смесь необходимо тщательно перемешать и дать пациенту целиком. Следует проглотить смесь сразу же после приготовления. Если пациентам требуется доза 75 мг, то необходимо следовать следующим инструкциям: 1. Держа одну капсулу 75 мг Тамифлю над маленькой емкостью, аккуратно раскрыть капсулу и высыпать порошок в емкость. 2. Добавить небольшое количество (не более 1 чайной ложки) подходящего подслащенного продукта питания (чтобы скрыть горький вкус) и хорошо перемешать. 3. Тщательно перемешать смесь и выпить ее сразу же после приготовления. Если в емкости осталось небольшое количество смеси, то следует ополоснуть емкость небольшим количеством воды и выпить оставшуюся смесь. Если пациентам требуются дозы 30-60 мг, то для правильного дозирования необходимо следовать следующим инструкциям: 1. Держа одну капсулу 75 мг Тамифлю над маленькой емкостью, аккуратно раскрыть капсулу и высыпать порошок в емкость. 2. Добавить в порошок 5 мл воды с помощью шприца с метками, показывающими количество набранной жидкости. Тщательно перемешать в течение 2 минут. 3. Набрать в шприц необходимое количество смеси из емкости согласно нижеприведенной таблице: Масса тела Рекомендованная доза Количество смеси Тамифлю® на один прием £15 кг 30 мг 2 мл >15-23 кг 45 мг 3 мл >23-40 кг 60 мг 4 мл Нет необходимости в заборе нерастворенного белого порошка, поскольку он является неактивным наполнителем. Нажав на поршень шприца, ввести все его содержимое во вторую емкость. Оставшуюся неиспользованную смесь необходимо выбросить. 4. Во вторую емкость добавить небольшое количество (не более 1 чайной ложки) подходящего подслащенного продукта питания, чтобы скрыть горький вкус, и хорошо перемешать. 5. Тщательно перемешать смесь и выпить ее сразу же после приготовления. Если в емкости осталось небольшое количество смеси, то следует ополоснуть емкость небольшим количеством воды и выпить оставшуюся смесь. Побочные действия Очень часто (>10%) — тошнота, рвота — головная боль Часто (1-10%) — боли в спине — кашель, носовые кровотечения, заложенность носа, назофарингит, бронхит, средний отит, синусит, бронхоспазм, — диарея, боли в эпигастральной области — герпес — раздражительность, утомляемость Нечасто (1-0,1%) — бессонница — аллергические реакции (дерматит) — конъюнктивит — лифмоаденопатия Редко (<0,1%) — реакции гиперчувствительности (включая дерматит, сыпь, экзему, мультиморфную эритему, анафилактические реакции), синдром Стивенса-Джонсона — желудочно-кишечные кровотечения — гепатит, увеличение уровня печеночных ферментов — судороги, делириозные состояния, перевозбуждение. Противопоказания — повышенная чувствительность к осельтамивира фосфату или любому компоненту препарата — хроническая почечная недостаточность (постоянный гемодиализ, хронический перитонеальный диализ, клиренс креатинина ≤10 мл/мин) Лекарственные взаимодействия Информация, полученная в фармакологических и фармакокинетических исследованиях осельтамивира фосфата, позволяет считать клинически значимые лекарственные взаимодействия маловероятными. Лекарственные взаимодействия, обусловленные конкуренцией и связыванием с активными центрами эстераз, превращающих осельтамивира фосфат в активное вещество, в литературе подробно не освещаются. Низкая степень связывания осельтамивира и активного метаболита с белками не дают оснований предполагать наличие взаимодействий, связанных с вытеснением лекарственных средств из связи с белками. Ни осельтамивира фосфат, ни активный метаболит не являются предпочтительным субстратом для полифункциональных оксидаз системы цитохрома Р450 или для глюкуронилтрансфераз. Формальной основы для взаимодействия с пероральными контрацептивами нет. Циметидин, неспецифический ингибитор изоферментов системы цитохрома Р450, не влияет на плазменные концентрации осельтамивира и его активного метаболита. Маловероятны клинически значимые межлекарственные взаимодействия, связанные с конкуренцией за канальцевую секрецию, принимая во внимание резерв безопасности для большинства подобных препаратов, пути выведения активного метаболита осельтамивира (клубочковая фильтрация и анионная канальцевая секреция), а также выводящую способность каждого из путей. Одновременное назначение пробенецида приводит к увеличению AUC активного метаболита примерно в 2 раза. Однако, коррекции дозы при одновременном применении с пробенецидом не требуется. Одновременный прием с амоксициллином не влияет на плазменные концентрации обоих препаратов. Фармакокинетических взаимодействий между осельтамивиром, его основным метаболитом не обнаружено при одновременном приеме с парацетамолом, ацетилсалициловой кислотой, циметидином или антацидными средствами (магния и алюминия гидроксид, кальция карбонат). При назначении Тамифлю вместе с часто применяющимися препаратами, такими как ингибиторы АПФ (эналаприл, каптоприл), тиазидные диуретики, антибиотики (пенициллин, цефалоспорины, азитромицин, эритромицин и доксициклин), блокаторы Н2-рецепторов к гистамину (ранитидин, циметидин), бета-блокаторами (пропранолол), ксантинами (теофиллин), симпатомиметиками (псевдоэфедрин), опиатами (кодеин), кортикостероидами, ингаляционными бронхолитиками и анальгетиками (аспирин, ибупрофен и парацетамол), изменений характера или частоты нежелательных явлений при этом не наблюдалось. Особые указания Данных по эффективности Тамифлю при любых заболеваниях, вызванных другими возбудителями, кроме вирусов гриппа А и В, нет. Детский возраст Детям младше 13 лет с массой тела менее 40 кг рекомендуется использование Тамифлю порошок для приготовления суспензии для приема внутрь. Дети 6-12 месяцев: эффективность Тамифлю у детей младше 1 года не установлена. Однако имеются ограниченные данные по фармакокинетике у детей 6-12 месяцев, согласно которым назначение осельтамивира в дозировке 3 мг/кг дважды в сутки обеспечивает плазменный уровень активного метаболита, аналогичный уровню, демонстрирующему клиническую эффективность у детей старшего возраста и взрослых. Беременность и период лактации Контролируемых клинических исследований по оценке безопасности Тамифлю у беременных не проводилось. Тамифлю следует назначать во время беременности или лактации только в том случае, если возможные преимущества от его применения превышают потенциальный риск для плода или грудного ребенка и проведена оценка безопасности, патогенности конкретного штамма вируса гриппа и состояния здоровья беременной женщины. Особенности влияния на способность управлять транспортными средствами или потенциально опасными механизмами Не влияет Передозировка В настоящее время случаев передозировки не описано, однако предполагаемыми симптомами острой передозировки будут тошнота со рвотой или без нее. Разовые дозы Тамифлю до 1000 мг переносились хорошо, за исключением тошноты и рвоты. Форма выпуска и упаковка По 10 капсул помещают в контурную ячейковую упаковку из пленки поливинилхлоридной пленки/поливинилдихлоридной и фольги алюминиевой. По 1 контурной ячейковой упаковке вместе с инструкцией по медицинскому применению на государственном и русском языках вкладывают в картонную пачку. Условия хранения Хранить при температуре не выше 25 °С. Хранить в недоступном для детей месте! Срок хранения 7 лет Не использовать по истечении срока годности, указанного на упаковке. Условия отпуска из аптек По рецепту Производитель Сенекси САС, Франция Юридический адрес производителя: 52 Rue M. et J. Gaucher, 94120 Fontenay-sous-Bois, France Владелец регистрационного удостоверения Ф. Хоффманн-Ля Рош Лтд., Швейцария Упаковщик Ф. Хоффманн-Ля Рош Лтд., Швейцария Адрес организации, принимающей на территории Республики Казахстан претензии от потребителей по качеству товара и ответственной за фармаконадзор ТОО «Рош Казахстан» 050000, г.Алматы, ул. Кунаева, 77, Бизнес-, 15 этаж Тел., факс: + e-mail,