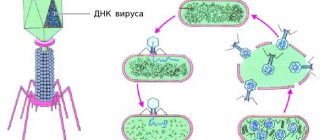
Что такое бактериофаги?
xорошо известно, что бактериофаги умеют адаптироваться к новым условиям благодаря мутациям, но из признаков «живого» им присущи только способность к размножению и передаче потомкам наследственной информации. Именно эти свойства позволили человеку использовать их как альтернативу антибиотикам для борьбы с инфекциями и уничтожения болезнетворных бактерий.
Бактериофаги — это вирусы, мельчайшие природные структуры, похожие на молекулярные кристаллы. Но, в отличие от большинства известных человечеству вирусов, они поражают не высшие организмы (например — человека), а только низшие — одноклеточные, недаром «бактериофаг» буквально переводится как «пожиратель бактерий». Бактериофаги устроены настолько просто, что даже не могут размножаться самостоятельно – для этого им, как и другим вирусам, нужна «чужая» живая клетка.
Коктейли из фагов
Новый виток интереса к фаговой терапии пришелся на последние годы. Дело в том, что антибиотики тоже не стали панацеей при лечении бактериальных инфекций: в наши дни разработка новых препаратов не поспевает за ростом числа бактерий с приобретенной устойчивостью к существующим антибиотикам. Уже сегодня в госпиталях Англии около 40 % стафилококковых инфекций вызвано такими штаммами, а в США от госпитальных инфекций, вызванных лекарственно устойчивыми бактериями, ежегодно умирает около 90 тыс. пациентов. При пересчете на население Земли это число составляет 3—5 млн смертей в год!
ВОЗ предупреждает, что мир вскоре вступит в «постантибиотиковую» эру, когда лечить обычные бактериальные инфекции будет нечем. И на этом фоне фаготерапия выглядит весьма перспективным направлением, развитие которого может привести к созданию эффективных персонализированных методов лечения заболеваний. Для этого есть как необходимые знания о фагах и механизмах их взаимодействия с бактериальными клетками, так и технологии работы с вирусными агентами.
Для фаговой терапии сегодня используют только вирулентные лизирующие фаги, в основном «хвостатые» фаги порядка Caudovirales, а также нитчатые фаги семейств Leviviridae (с одноцепочечным РНК-геномом) и Inoviridae (с одноцепочечным кольцевым ДНК-геномом).
Как говорилось выше, спектры активности фагов обычно очень узки и ограничены одним или несколькими близкородственными видами бактерий. С одной стороны, такая узкая специфичность хороша для терапии, поскольку позволяет устранить конкретный микроорганизм, не нарушая всего бактериального сообщества человеческого организма. С другой стороны, при необходимости экстренного лечения (когда нет времени для выявления конкретной бактерии, вызывающей развитие болезнетворного процесса в ране или на обожженной поверхности) необходимо иметь препарат, поражающий сразу несколько видов бактерий, возможных возбудителей инфекции. Для решения этой проблемы обычно используют коктейли фагов – препараты, содержащие несколько фагов, отличающихся по специфичности.
Такой подход использовал еще д’Эрель. Коктейль д’Эреля, привезенный им из Парижа еще в 1930 г., до сих пор является одним из основных фаговых препаратов: он лежит в основе грузинского пиофага и российского интестифага. В Тбилиси на основе фаговых коктейлей разрабатывались препараты для лечения желудочно-кишечных заболеваний и гнойных ран для массового применения в случае возникновения эпидемий или военных действий. Результаты армейских испытаний и широкого эксперимента по предотвращению детских желудочно-кишечных расстройств, проведенного в Тбилиси, показали хорошую эффективность таких препаратов.
Фаговые коктейли производятся стандартными, и ориентированы они на сообщества бактерий, часто встречающиеся при конкретных заболеваниях. Конечно, более эффективные коктейли получаются в том случае, когда их компоненты подбирают к бактериальному сообществу конкретного пациента. Для получения такого коктейля необходимо протестировать бактерии пациента на чувствительность к фагам из коллекции, чтобы подобрать наиболее эффективные фаговые штаммы. Если нужных фагов в коллекции не окажется, специфичные для бактерий фаги ищут в природных субстратах.
Вообще поиск бактериофагов довольно прост: на бактериальную культуру воздействуют образцами из различных источников: водоемов, почвы, канализационных стоков и т. п. Если бактерии погибают, их отделяют от раствора центрифугированием, а оставшийся раствор тестируют на активность. Затем фаг размножают, выращивая на соответствующей бактериальной культуре. Более того, фаги можно лиофилизировать (высушить в вакууме) и непосредственно использовать в капсулах. В таком виде препарат сохраняют стабильность в течение 14 месяцев при температуре до 55 °С.
Из чего состоит бактериофаг
Типичный фаг состоит из «головы» с плотно упакованной генетической программой, состоящей из нуклеиновых кислот (ДНК или РНК), и «хвоста», с помощью которого «впрыскивает» свои гены в клетку бактерии. Зараженная бактерия начинает с помощью собственных внутриклеточных систем и ресурсов синтезировать белки и нуклеиновые кислоты, необходимые для сборки новых вирусных частиц. Зрелые фаги выходят на поиски новой добычи, а «родительская» бактериальная клетка погибает.
Благодаря последним исследованиям стало понятно, что бактериофаги играют важную для поддержания глобального «микробного баланса» роль в биосфере: каждые двое суток они уничтожают половину мировой популяции бактерий и тем самым препятствуют этим быстро размножающимся организмам покрыть толстым слоем земную поверхность.
Бактериофаги появляются везде, где живут бактерии: на суше и в океанах, в почве и в воде, в растениях и животных. Даже в желудочно-кишечном тракте человека содержится около 1012 бактериофагов – на порядок больше, чем звезд в нашей Галактике! И хотя размер фаговых частиц не превышает 0,0001 мм, биомасса фагов на планете достигает фантастической цифры – 1 млрд тонн. Поэтому эти невидимые глазом, но вездесущие создания называют иногда «темной материей» биосферы.
«Счетчики» бактерий
Бактериофаги служат не только разносторонним терапевтическим и «дезинфицирующим» средством, но и удобным и точным аналитическим инструментом микробиолога. К примеру, благодаря своей высокой специфичности они являются природными аналитическими реагентами для выявления бактерий определенного вида и штамма.
В простейшем варианте такого исследования в чашку Петри с питательной средой, засеянную бактериальной культурой, добавляют по капле различные диагностические бактериофаги. Если бактерия окажется чувствительной к фагу, то на этом месте бактериального «газона» образуется «бляшка» — прозрачный участок с убитыми и лизированными бактериальными клетками.
Анализируя размножение фагов в присутствии целевых бактерий, можно количественно определить численность последних. Так как количество фаговых частиц в растворе возрастет пропорционально числу содержавшихся в нем бактериальных клеток, то для оценки численности бактерий достаточно определить титр бактериофага.
Специфичность и чувствительность такой аналитической реакции достаточно высока, а сами процедуры просты в исполнении и не требуют сложного оборудования. Важно, что диагностические системы, основанные на бактериофагах, сигнализируют о наличии именно живого патогена, тогда как другие методы, такие как ПЦР и иммуноаналитические, свидетельствуют лишь о наличии биополимеров, принадлежащих этой бактерии. Такого типа диагностические методы особенно удобны для использования в экологических исследованиях, а также в пищевой индустрии и сельском хозяйстве.
Сейчас для выявления и количественного определения разных штаммов микроорганизмов применяют специальные референсные виды
фагов. Очень быстрые, работающие практически в режиме реального времени аналитические системы могут быть созданы на основе генетически модифицированных бактериофагов, которые при попадании в бактериальную клетку запускают в ней синтез репортерных флуоресцирующих (или способных к люминесценции) белков, таких как
люцифераза
. При добавлении к подобной среде необходимых субстратов в ней будет появляться люминесцентный сигнал, величина которого соответствует содержанию бактерий в образце. Такие «меченные светом» фаги были разработаны для детекции опасных патогенов — возбудителей чумы, сибирской язвы, туберкулеза, а также инфекций растений.
Вероятно, с помощью модифицированных фагов удастся решить и давнюю задачу глобальной важности — разработать дешевые и быстрые методы детекции возбудителей туберкулеза на ранней стадии заболевания. Задача эта очень сложна, поскольку микобактерии, вызывающие туберкулез, отличаются крайне медленным ростом при культивировании в лабораторных условиях. Поэтому диагностика заболевания традиционными методами может затягиваться на срок до нескольких недель.
Фаговая технология позволяет упростить эту задачу. Суть ее в том, что к образцам анализируемой крови добавляют бактериофаг D29, способный поражать широкий спектр микобактерий. Затем бактериофаги отделяют, и образец перемешивают с быстрорастущей непатогенной культурой микобактерий, также чувствительной к этому бактериофагу. Если в крови первоначально имелись микобактерии, которые были инфицированы фагами, то в новой культуре будет также наблюдаться наработка бактериофага. Таким образом можно выявить единичные клетки микобактерий, а сам процесс диагностики с 2–3 недель сокращается до 2–5 дней (Swift & Rees, 2016).
Преимущества бактериофагов
| Бактериофаги – антибактериальные агенты и природные антисептики | Безопасны и не токсичны, не имеют побочных эффектов, применяются у новорождённых детей, беременных и кормящих женщин |
| Действие бактериофагов не затрагивает полезную микрофлору организма, в отличие от антибиотиков | Бактериофаги совместимы со всеми лекарственными препаратами. Применение бактериофагов не ограничивает использование других лекарств и не влияет на их эффективность |
| Воздействует лишь на чувствительные к ним болезнетворные бактерии, вызывающие инфекционное заболевание, разрушая их изнутри | Бактериофаги выводятся из организма естественным путем |
Бактериофаги что мы знаем о них? Современные возможности фаготерапии в практике врача-педиатра
И.М. ЩЕРБЕНКОВ
, к.м.н.,
ЦЭЛТ, МоскваБактерии, резистентные к большинству или ко всем из всех известных антибиотиков, вызывают все более серьезные проблемы. Это увеличивает риск возврата медицинского сообщества к проблемам того периода, когда антибиотики были неизвестны и широко распространены неизлечимые инфекции и эпидемии. Несмотря на интенсивную работу ведущих химиков и фармацевтов всего мира, за последние 30 лет резко снизился синтез новых классов антибиотиков, и в ближайшее время не предвидится поступления в клиническую практику принципиально новых представителей антибактериальных средств. Есть надежда, что вновь обнаруженная возможность полностью секвенировать микробные геномы и определять молекулярные основы патогенности откроет новые пути лечения инфекционных заболеваний, но все с большим рвением идет поиск других подходов к этой проблеме.
Одним из результатов такого поиска является вновь возникший интерес к возможностям терапевтического использования бактериофагов (от бактерии и греч. phagos пожиратель; букв. пожиратели бактерий) специфических вирусов, которые атакуют только бактерии и убивают патогенные микроорганизмы. Бактериофаги обладают способностью проникать в бактериальные клетки, репродуцироваться в них и вызывать их лизис.
История изучения и применения бактериофагов
В 1896 г. Эрнест Ханкин сообщил, что воды рек Ганга и Джамна в Индии обладают значительной антибактериальной активностью, которая сохранялась после прохождения через фарфоровый фильтр с порами очень малого размера, но устранялась при кипячении. Наиболее подробно изучал он действие неизвестной субстанции на Vibrio cholerae и предположил, что она ответственна за предупреждение распространения эпидемий холеры, вызванных употреблением воды из этих рек. Однако в последующем он не объяснил этот феномен.
В 1898 г. впервые перевиваемый лизис бактерий (сибиреязвенной палочки) наблюдал русский микробиолог Н.Ф. Гамалея.
Официально бактериофаги были открыты почти через 20 лет независимо друг от друга Ф. Туортом совместно с А. Лондом и Ф. д’Эрелем как фильтрующиеся, передающиеся агенты разрушения бактериальных клеток. Английский ученый Ф. Туорт в 1915 г. описал явление лизиса у гнойного стафилококка и открыл первый «вирус, пожирающий бактерии», когда наблюдал любопытное дегенеративное изменение лизис в культурах стафилококков из лимфы теленка. С его именем связано название «феномен Туорта». В 1917 г. Феликс д’Эрель делает аналогичное открытие, именно он дал им название «бактериофаги», используя суффикс «фаг» не в его прямом смысле «есть», а в смысле развития за счет чего-то.
В 1980-е гг. эффективность лечения антибиотиками значительно понизилась, бактерии активно вырабатывают лекарственную устойчивость. Чтобы создать новый сильнодействующий антибиотик, фармацевтические компании сегодня должны в среднем потратить 10 лет и 800 млн долл. Это послужило поводом к повышенному интересу к фаговой терапии. В начале 2000-х гг. Гленн Моррис, сотрудник Университета Мэриленд (США), совместно с НИИ бактериофагов, микробиологии и вирусологии в Тбилиси наладил испытания фаговых препаратов для получения лицензии на их применение в США. И уже в июле 2007 г. бактериофаги одобрены для использования в США. На протяжении последних нескольких лет исследования свойств бактериофагов проводятся в России, Грузии, Польше, Франции, Германии, Финляндии, Канаде, США, Великобритании, Мексике, Израиле, Индии, Австралии. Характеристика фагов
Применение современных электронных микроскопов, а также усовершенствование методов приготовления препаратов для электронной микроскопии позволили более детально изучить тонкую структуру фагов. Оказалось, что она весьма разнообразна и у многих фагов более сложна, чем структура вирусов растений и ряда вирусов человека и животных. Бактериофаги, как и другие вирусы, несут свою генетическую информацию в форме ДНК либо РНК. Большинство бактериофагов имеют хвостики, кончики которых прикреплены к конкретным рецепторам, таким как молекулы углеводов, белков и липополисахаридов на поверхности бактерии-хозяина. Бактериофаг впрыскивает свою нуклеиновую кислоту в хозяина, где он использует генетический механизм хозяина, чтобы реплицировать свой генетический материал, и считывает его, чтобы сформировать новый фагокапсульный материал для создания частичек нового фага. Число фагов, произведенных в течение единичного цикла инфекции (размер выхода), варьирует между 50 и 200 новыми фаговыми частицами.
Фаги обладают строгой специфичностью, т. е. способны паразитировать только в определенном виде микроорганизмов: стрептококках, стафилококках и т. д. Фаги с более строгой специфичностью, которые паразитируют только на определенных представителях данного вида, называются типовыми. Фаги, которые лизируют микроорганизмы близких видов, например видов, входящих в род возбудителей дизентерии (шигелл), называются поливалентными.
Лизогенизация бактерий сопровождается изменением их морфологических, культуральных, ферментативных, антигенных и биологических свойств. Так, например, нетоксигенные штаммы коринебактерий дифтерии в результате лизогенизации превращаются в токсигенные.
Практическое использование фагов
Фаготерапия (применение бактериальных вирусов для лечения бактериальных инфекций) была проблемой, весьма интересующей ученых еще 60 лет назад. Открытие пенициллина и других антибиотиков в 1940-х гг. обеспечило более результативный и многосторонний подход к подавлению вирусных заболеваний и спровоцировало к закрытию работ в данной области.
В связи с катастрофически возрастающей антибиотикорезистентностью и отсутствием в ближайшей перспективе новых антибактериальных средств возродился активный интерес к фаготерапии.
Научные данные последних десятилетий доказывают, что в отличие от антибиотиков препараты бактериофагов имеют следующие положительные качества:
• размножаясь, они самостоятельно регулируют свою численность (увеличивая или уменьшая ее), поскольку размножаются только до тех пор, пока имеются чувствительные бактерии, а затем постепенно элиминируются из организма и окружающей среды; • они гораздо более специфичны, чем большинство антибиотиков; будучи нацелены на конкретные проблемные бактерии, вызывают гораздо меньшее повреждение нормального микробного баланса организма. Бактериальный дисбаланс, или «дисбиоз», вызванный лечением многими антибиотиками, может привести к серьезным вторичным инфекциям с участием достаточно резистентных бактерий, увеличивающим затраты на лечение и летальность. Специфические проблемы, возникающие в результате, включают инфекции, вызванные псевдомонадами, трудно поддающиеся лечению, и Clostridium difficile, причину серьезной диареи и псевдомембранозного колита; • фаги имеют возможность использовать в качестве мишеней рецепторы на бактериальной поверхности, участвующие в патогенезе, а это означает, что вирулентность любых резистентных к ним мутантов ослаблена; • в отношении фаговой терапии описано мало побочных эффектов; • фаговая терапия была бы особенно применима для лиц с аллергией к антибиотикам; • должным образом селекционированные фаги можно легко использовать профилактически, способствуя предотвращению бактериальных заболеваний у людей или животных при контакте с микробами, либо для санации больниц и борьбы с госпитальными инфекциями; • фаг можно использовать либо независимо, либо в сочетании с другими антибиотиками, с целью уменьшения вероятности развития резистентности бактерий; • фаги не воздействуют на нормофлору кишечника и препараты эубиотиков и протобиотиков, что дает возможность для их совместного применения.
Обладая широким спектром антибактериальной активности и клинической эффективности, бактериофаги эффективны против лекарственно-устойчивых организмов, что предоставляет возможность расценивать их как аналоги или заменители антибиотиков и средства противосептической терапии.
Фаготерапия может использоваться профилактически с целью борьбы с распространением инфекционного заболевания там, где источник идентифицирован на ранней стадии, или там, где вспышки случаются внутри сравнительно закрытых организаций, таких как школы или детские сады.
Активность лечебно-профилактических бактериофагов при инфекционных болезнях пищеварительной системы, гнойно-септических заболеваниях кожных покровов, кровеносной системы, дыхательной системы, опорно-двигательного аппарата, мочеполовой системы (более 180 нозологических единиц заболеваний, вызванных бактериями Klebsiella, Escherichiae, Proteus, Pseudomonas, Staphylococcus, Streptococcus, Serratia, Enterobacter) довольно высока – от 72 до 90% – и часто является единственным эффективным лечебным средством. Также это касается штаммов больничного происхождения, характеризующихся множественной устойчивостью к антибиотикам.
Препараты бактериофагов
Лечебно-профилактические препараты бактериофагов составлены из поликлональных патогенных бактериофагов обширной сферы действия, действенных относительно антибиотикоустойчивых бактерий. По составу различают поливалентные (активные по отношению к различным видам и сероварам одного возбудителя) и комбинированные (с содержанием фагов к нескольким возбудителям) бактериофаги, что позволяет получить лечебный эффект при наличии микробных ассоциаций. ФГУП «НПО «Микроген» Минздрава России выпускает большой спектр лекарственных бактериофагов: стафилококковый, стрептококковый, коли, протейный, синегнойный, клебсиеллезный, брюшнотифозный, дизентерийный, сальмонеллезный. Имеются и их комбинированные формы: колипротейный бактериофаг, интести бактериофаг (смесь стерильных фильтратов фаголизатов бактерий: Shigella Flexneri 1-6 серогруппы В, Sonnei серогруппы D; Salmonella paratyphi A,B, Typhimurium, Choleraesuis, Oranienburg, Enteritidis, наиболее распространенных серологических групп E. coli – 0111, 055, 026, 125, 0119, 0128, 018, 044, 025, 020, Proteus (vulgaris, mirabilis), Staphylococcus, Pseudomonas, Enterococcus – титр фага не менее 1 х 106).
Препараты бактериофагов представляют собой стерильный фильтрат бактериальных фаголизатов, их прописывают для применения внутрь, местно для орошения повреждений и слизистых, введения в полости матки, мочевого пузыря, уха, придаточных пазух, а также в дренированные полости – брюшную, плевральную, а также в полости нарывов и гнойников после удаления экссудата. Бактериофаги способны стремительно проникать в кровоток, лимфатическую систему, а удаляются из организма вместе с мочой. Соответствие препаратов бактериофагов нынешней атиологической структуре возбудителей достигается производством штаммов, или штаммов-продуцентов, или синтезированного материала, не подлежащего каким-либо трансформациям. Такая пластичность бактериофаговых препаратов обеспечивает продолжительный эффект первичной фагоустойчивости возбудителей. Применение бактериофагов для лечения инфекционных заболеваний инициирует факторы специфического и неспецифического иммунитета, что в особенности результативно для терапии длительных инфекционных заболеваний, возникших в результате ослабления иммунитета на фоне депрессивного расстройства при бактерионосительстве. Научными исследованиями, во время клинических наблюдений, методом эксперимента выявлена несостоятельность плазмид передавать антибиотикам иммунитет к токсигенности профилактико-терапевтическим препаратам бактерионосительства, потому что они являются поликлональными комплексами вирулентных бактериофагов.
При использовании бактериофагов в крупных клиниках целесообразно включать в состав производственных штаммов, на которых готовятся коммерческие препараты, госпитальные штаммы возбудителей гнойно-воспалительных заболеваний, характерных для данного стационара. Отечественными неонатологами показана высокая эффективность фаготерапии гнойно-септических инфекций у детей раннего возраста. Помимо литического действия на микробы, отмечают их значение в механизме антитоксического, клеточного и гуморального иммунитета. Изучение возможности применения бактериофагов как альтернативы антибиотикотерапии для лечения острой кишечной инфекции (ОКИ) у детей в возрасте до 3 лет, проводимое на кафедре детских инфекционных болезней КНМУ, показало высокую эффективность поливалентного Интести-бактериофага. Был сделан вывод о возможности проведения этиотропной терапии поливалентным Интести-бактериофагом без включения антибиотиков больным ОКИ в легкой и средне-тяжелой форме даже в условиях общего кишечного отделения.
Дисбиоз как актуальная проблема у детей
В последние годы актуальной задачей в педиатрии остается рациональная фармакотерапия дисбиозов различного генеза. В особенности актуальна проблема дисбиоза кишечника у детей раннего возраста. Результаты современных исследований свидетельствуют о наличии дисбактериоза кишечника I-II степени у 50% здоровых детей грудного возраста, III-IV степени — у 20-25% детей. Нарушения микробиоценоза кишечника наблюдают практически при всех заболеваниях детского возраста. При формировании дисбактериоза усугубляется общее состояние пациента, снижается резистентность организма к инфекционным и антигенным агентам, толерантность к пищевым продуктам. Все это создает фон для более тяжелого течения заболеваний, возникновения осложнений, перехода острых форм в хронические. Дети первого полугода жизни особенно подвержены дисбиозу, что обусловлено транзиторной недостаточностью ферментов (в основном лактазы), незрелостью вегетативной нервной системы (ВНС), регулирующей моторику кишечника, несформированностью иммунных механизмов.
Основными причинами возникновения дисбиоза кишечника в детском возрасте являются:
• несвоевременное начало и неправильное ведение лактации; • ранний переход и нерациональное искусственное вскармливание на первом году жизни ребенка и нарушение режима питания в старшем возрасте; • острые кишечные инфекции и заболевания пищеварительного канала неинфекционного характера; • нерациональное применение антибиотиков и других химиотерапевтических препаратов; • аллергическая предрасположенность; • снижение естественной резистентности организма.
Лечение пациентов с дисбиозом кишечника следует проводить дифференцированно и начинать с выявления основного заболевания, без лечения которого признаки дисбиоза рецидивируют. Длительность одного курса лечения детей индивидуальна и колеблется от 10 сут. до 1,52 мес. Повторные курсы проводят после промежуточного бактериологического контроля (исследование кала) не ранее, чем через 2 нед. после окончания курса терапии. Суммарная длительность восстановления (до уровня устойчивой клинической компенсации) зависит от многих сопутствующих факторов и составляет 69 мес.
В современной детской гастроэнтерологии используется широкий арсенал препаратов для коррекции нарушенного микробиоценоза кишечника. В клинической практике педиатры и гастроэнтерологи для коррекции дисбиоза всe чаще используют бактериофаги. Применяют коли-протейный, стафилококковый, синегнойный, поливалентный дизентерийный, сальмонеллезный, комбинированный (смесь стафилококкового, стрептококкового, коли, синегнойного, протейного бактериофагов), поливалентный пиобактериофаг, интестифаг и др. Применение специфических бактериофагов позволяет оптимальным образом осуществить селективную деконтаминацию, проводимую при ряде патологических состояний с целью санирующего эффекта, а также для восстановления нормального микробиоценоза. Являясь безвредным биологическим методом лечения, бактериофаготерапия может применяться у детей раннего возраста. Для получения положительных результатов использования бактериофагов необходимо предварительное исследование чувствительности к ним микроорганизмов.
Коли-протейный бактериофаг жидкий мы применяем при лечении детей с дисбиозом, обусловленным энтеропатогенной кишечной палочкой (эшерихией) и протеем (мирабилис или вульгарным). Бактериофаг назначаем внутрь или в клизме. Суточная доза препарата для применения внутрь: детям в возрасте до 6 мес. 5 мл 3 раза в сутки внутрь и 10 мл 1 раз в сутки в клизме вместо одного из приемов через рот; от 6 мес. до 1 года 1015 мл 2 раза в сутки внутрь и 20 мл 1 раз в сутки в клизме; в возрасте 13 лет 1520 мл 2 раза в сутки внутрь и 40 мл 1 раз в сутки в клизме; старше 3 лет 20 мл 2 -3 раза в сутки внутрь и 40-60 мл 1 раз в сутки в клизме. Внутрь бактериофаг назначают за 1-1,5 ч до еды. Детям первого месяца жизни бактериофаг разводят кипяченой водой в 2 раза. Детям старше 6 мес. за 5-10 мин до введения препарата дают 10-20 мл (в зависимости от возраста) 2-3%-ного раствора натрия гидрокарбоната для нейтрализации желудочного сока. Курс лечения составляет 5-10 сут. в зависимости от степени выраженности дисбиотических нарушений.
В клизме препарат целесообразно применять при отсутствии синдрома мальабсорбции: детям до 6 мес. — 20 мл, от 6 мес. до 3 лет — 30-40 мл, старше 3 лет — 40–50 мл. Препарат вводят 1 раз в сутки 23 курсами продолжительностью 3-4 сут. С интервалом между курсами 3 сут. Противопоказаний к применению препарата нет. Назначение бактериофага не исключает применения других ЛС.
Стафилококковый бактериофаг жидкий мы назначаем внутрь в суточной дозе: детям до 6 мес. — 20 мл, 6 мес. — 3 года — 40 мл, старше 3 лет — 100 мл. Вводят в 2 приема, натощак, за 1,5-2 ч до еды. В клизме в этих же дозах следует вводить 1 раз в сутки по той же схеме.
Поскольку мы в реальной клинической практике при дисбиозах встречаемся с одновременным ростом различных представителей патогенной микрофлоры, важно назначение в подобных случаях с учетом данных бактериологических исследований комбинированных бактериофагов — смеси стафилококкового, стрептококкового, коли, синегнойного, протейного бактериофагов. Их назначают детям в возрасте до 3 лет по 3-5 мл 3 раза в сутки внутрь и 10 мл 1 раз в сутки в клизме; старше 3 лет — 5-10 мл 3 раза в сутки внутрь и 10 мл 1 раз в сутки в клизме. Внутрь назначают за 1 ч до еды. Возможно дополнительное введение комбинированного фага в высокой клизме по 5-20 мл. Курс лечения 5-15 сут.
Интестифаг содержит фаголизаты кишечной палочки, шигеллезы сальмонелл, УПМ. Назначают внутрь за 1 ч до еды детям в возрасте до 3 лет по 3-5 мл 3 раза в сутки внутрь и 10 мл 1 раз в сутки в клизме; детям старше 3 лет — по 5-10 мл 3 раза в сутки внутрь и 10 мл 1 раз в сутки в клизме. Курс лечения 5-6 сут.
Поливалентный пиобактериофаг, или секстифаг — смесь фаголизатов кишечной палочки, клебсиеллы, синегнойной палочки, стафилококка, стрептококка, протея. Данный препарат отличается наиболее высокой степенью очистки от бактериальных метаболитов, что значительно улучшает его вкусовые качества и делает средством первого выбора у детей до года. Назначают: детям в возрасте до 3 лет — 3-5 мл 3 раза в сутки внутрь и 10 мл 1 раз в сутки в клизме; старше 3 лет — 5-10 мл 3 раза в сутки внутрь и 10 мл 1 раз в сутки в клизме. Внутрь применяют за 1 ч до еды. Курс лечения 5-15 сут.
Применение фагов предшествует назначению кислотообразующих препаратов (пребиотиков, пробиотиков и др.). Заключение
Препараты бактериофагов эффективны при лечении болезней, вызванных антибиотикоустойчивыми штаммами микроорганизмов, в частности при лечении паратонзиллярных гнойников, воспалений пазух носа, а также гнойно-септических инфекций, реанимационных больных, хирургических заболеваний, циститов, пиелонефритов, холециститов, гастроэнтероколитов, дисбактериоза кишечника, воспалительных заболеваний и сепсиса новорожденных. При обширно распространенном формировании стабильности к антибиотикам у патогенных бактерий необходимость в новых антибиотиках и альтернативных технологиях контроля за микробными инфекциями завоевывает все большую значимость. Бактериофагам, вероятно, еще предстоит исполнить свою роль в лечении инфекционных заболеваний как при их независимом применении, так и в сочетании с антибиотико-терапией.
Литература
1. Антибиотики-убийцы: [история открытия, польза и вред, противопоказания, ищем замену, когда нет выхода]. М.: Эксмо, 2007. 2. Приворотский В.Ф., Лупова Н.Е., Шильникова О.В. Логика построения корригирующих медикаментозных программ нарушенного микробиоценоза кишечника у детей // РМЖ. 2007. №1. С. 6–9. 3. Бельмер С.В. Антибиотик-ассоциированный дисбактериоз кишечника // РМЖ. 2004. Т. 12. №3. С. 148–151. 4. Методы нормализации пищеварения у детей с дисбактериозом: пособие для врачей / под ред. академика РАМН А.А. Баранова. М., 2005. С. 38–39. 5. Заболевания кишечника. Справочник для практических врачей «Ремедиум-врач». М.: ООО «Издательство «Ремедиум». С. 74–76. 6. Государственный реестр лекарственных средств. М.: МЗиСР (интернет версия www.drugreg.ru). 7. Нижевич А.А., Хасанов Р.Ш., Нуртдинова Н.М., Очилова Р.А., Логиновская В.В., Калметьева Л.Р. Антибиотик-ассоциированный дисбактериоз кишечника у детей // РМЖ. 2007. №1. С. 12–15. 8. Щербаков П.Л., Цветков П.М., Нечаева Л.В. Профилактика диареи, связанной с приемом антибиотиков у детей // Вопросы современной педиатрии. 2004. Т. 3. №2. 9. Корман Д.Б. Основы противоопухолевой химиотерапии. М.: Практическая медицина, 2006. 10. Зеленин К.Н. Возникновение и развитие химиотерапии. 11. Урсова Н.И. Дисбактериоз кишечника у детей: руководство для практических врачей / под ред. Г.В. Римарчук. М.: «Компания БОРГЕС», 2006. 12. Ларчини Д., Паренти Ф. Антибиотики / пер. с англ. Ю.В. Дудника. М.: Мир, 1985. 13. Клинико-иммунологическая эффективность иммунобиологических препаратов / под ред. М.П. Костинова и И.В. Медуницына. М.: Миклош, 2004. С. 195–206. 14. Стент Г. Молекулярная биология вирусов бактерий / пер. с англ. М., 1965. 15. Хейс У. Генетика бактерий и бактериофагов / пер. с англ. М., 1965. 16. Шлегель Г. Общая микробиология / пер. с нем. М., 1987. С. 142.
Применение бактериофагов
Сразу после открытия бактериофагов, препараты на их основе стали использовать для борьбы с инфекционными болезнями человека. Однако в результате изобретения антибиотиков и недостатка знаний о бактериофагах их лечебный потенциал не был реализован.
Спустя полстолетия бактериофагами заинтересовались молекулярные биологи. Они выяснили, что эти простые «наноустройства» с короткими генетическими программами являются удобными объектами для экспериментальных исследований по изучению устройства и работы генома. Дальнейшее изучение фагов и механизмов, с помощью которых бактерии защищаются от врагов, открыло науке один из самых эффективных инструментов редактирования генома – CRISPR-CAS, основанный на системе «бактериального иммунитета».
Фаги нашли применение в разных сферах человеческой деятельности, включая био- и нанотехнологии. Например, как простые системы для наработки белков с заданными свойствами или как основа для создания материалов с заданной архитектурой в каталитической химии.
В качестве «умных» молекулярных устройств их используют для транспорта лекарств в организме и как диагностические сенсоры – например, для выявления патогенных бактерий в продуктах питания. Препараты фагов применяются для дезинфекции в сельском хозяйстве и в пищевой промышленности. Это увеличивает экологическую чистоту продуктов.
Но все-таки медицина, как и столетие назад, остается главной областью применения этих врагов бактерий. С ростом лекарственной устойчивости бактерий к химическим антибиотикам возросло значение фаготерапии для профилактики и лечения инфекционных болезней человека.
Фаговые антибиотики
В терапевтических целях фаги необязательно использовать напрямую. За миллионы лет эволюции бактериофаги разработали арсенал специфических белков — инструментов для распознавания целевых микроорганизмов и манипуляций с биополимерами жертвы, на основе которых можно создавать противобактериальные препараты. Наиболее перспективными белками такого типа являются ферменты эндолизины, которые фаги используют для разрушения клеточной стенки при выходе из бактерии. Сами по себе эти вещества являются мощными антибактериальными средствами, нетоксичными для человека. Эффективность и направленность их действия можно повысить, изменив в них адресующие структуры — белки, специфически связывающиеся с определенными бактериями.
Большинство бактерий делятся по устройству клеточной стенки на грамположительные, мембрана которых покрыта очень толстым слоем пептидогликанов, и грамотрицательные, у которых слой пептидогликана расположен между двумя мембранами. Использование природных эндолизинов особенно эффективно в случае грамположительных бактерий (стафилококков, стрептококков и др.), поскольку пептидогликановый слой у них расположен снаружи. Грамотрицательные бактерии (синегнойная палочка, сальмонеллы, кишечная палочка и др.) являются менее доступной мишенью, поскольку ферменту, чтобы добраться до внутреннего пептидогликанового слоя, необходимо проникнуть сквозь внешнюю бактериальную мембрану.
Для преодоления этой проблемы были созданы так называемые артилизины — модифицированные варианты природных эндолизинов, содержащие поликатионные или амфипатические пептиды, которые дестабилизируют внешнюю мембрану и обеспечивают доставку эндолизина непосредственно к пептидогликановому слою. Артилизины обладают высокой бактерицидной активностью и уже показали свою эффективность при лечении отитов у собак (Briers et al., 2014).
Примером модифицированного эндолизина, избирательно действующего на определенные бактерии, является препарат P128 канадской компании GangaGen Inc
. Он представляет собой биологически активный фрагмент эндолизина, соединенный с лизостафином — адресующей белковой молекулой, которая связывается с поверхностью клеток стафилококков. Полученный химерный белок обладает высокой активностью против разных штаммов стафилококка, в том числе обладающих множественной лекарственной устойчивостью.
Современная история
К настоящему времени самый большой опыт фаготерапии имеют специалисты из Тбилиси и специализированного центра Института иммунологии и экспериментальной терапии им. Л. Хиршфельда (Вроцлав, Польша), где в небольших количествах производятся препараты бактериофагов для испытаний.
Польские исследователи изначально делали акцент на персонализированную терапию. Они использовали фаготерапию для экспериментального лечения пациентов с хроническими заболеваниями, которым не помогают антибиотики. Через центр прошли уже тысячи пациентов, многие из которых были полностью излечены.
Результаты этих клинических испытаний доказали высокую эффективность фагов при лечении инфекционных легочных заболеваний: для подавления инфекции в горле, носу и в легких достаточно однократного интраназального введения препарата. Не менее эффективно фаги элиминируют патогенные бактерии из желудочно-кишечного тракта. Высокая эффективность бактериофагов была также продемонстрирована практически во всех случаях гноеродной язвы диабетической стопы, заболеваний легких, мастита, урогенитальных инфекциях. Список таких заболеваний можно продолжить, при этом важно отметить, что ни в одном из испытаний не наблюдалось каких-либо побочных эффектов, вызванных бактериофагами.
В качестве специфичных агентов, уничтожающих бактерии, бактериофаги сегодня находят применение в терапии заболеваний не только людей, но и животных, а также для защиты растений и при консервации пищевой продукции. Так, в 2006 г. FDA разрешила применение бактериофаговых коктейлей для обработки мясных и других сельскохозяйственных продуктов. В этом случае фаги получили статус пищевых добавок. Они также были разрешены к применению в качестве средства дезинфекции. Препараты фагов (в виде аэрозолей) были успешно испытаны в экспериментах по защите сельскохозяйственных птиц на крупных фермах, а также в рыбоводческих хозяйствах
В Англии фаговые препараты были успешно испытаны для лечения хронического отита, трудно излечимого заболевания вследствие образования так называемых бактериальных биофильмов – лекарственно-устойчивых микробных пленок. Во Франции –колыбели фаговой терапии – исследования в этой области сейчас почти не ведутся, хотя до последнего времени Институт Пастера делал фаговые коктейли на заказ.
В промышленных масштабах фаговые препараты сегодня производит российская компания Микроген. Подобные лекарства можно купить в аптеках в России, Белоруссии и на Украине. Фаговые препараты производства Микроген и Тбилисского центра для лечения ожоговых инфекций были успешно испытаны и в Бельгии.
Тем не менее до сих пор в большинстве стран применение бактериофагов в терапии официально не разрешено: это касается как FDA, американского Управления по контролю качества пищевых продуктов и лекарственных препаратов, так и аналогичных европейских агентств. На территории Евросоюза фаги для лечения больных используют только в вышеупомянутом польском Институте иммунологии и экспериментальной терапии.
Поэтому лечение заинтересованных больных проводится в режиме медицинского туризма. (Калифорния, США) направляет пациентов из разных стран, страдающих от хронических заболеваний, вызванных лекарственно устойчивыми бактериями, либо в Центр фаговой терапии в Тбилиси, либо в свою клинику в Мексике.