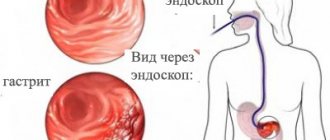
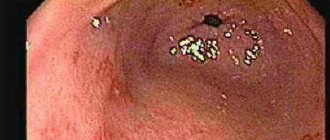
Очень часто на прием приходят пациенты, которым по поводу болей в верхней половине живота, тяжести после еды в подложечной области, отрыжки была проведена гастродуоденоскопия и сделано заключение, на основании которого врачом ставится диагноз «атрофический гастрит». Возникает тревога у человека, что делать и не может ли этот гастрит перейти в рак желудка?
Сегодня попытаемся ответить на вопрос, какие методы помогут подтвердить наличие атрофического гастрита и как лечить таких пациентов.
Среди болезней желудка наиболее часто встречаемым и выставляемым практическими врачами диагнозом является «хронический гастрит».
Хронический гастрит занимает центральное место среди болезней желудка, является наиболее распространенным заболеванием желудочно-кишечного тракта. Считается, что треть взрослого населения страдает хроническим гастритом, но только 10-15% обращается к врачам. Важным является то, что хронический гастрит предшествует или сопровождает серьезные по течению и прогнозу болезни желудка — язвенную болезнь, рак желудка, а также близко лежащих органов пищеварительной системы.
Атрофический гастрит – что это
Что мы понимаем под атрофическим гастритом? В основе лежат атрофические процессы в слизистой оболочке желудка, воспалительные и дистрофические процессы, которые приводят к функциональной недостаточности слизистой. Атрофия желез слизистой оболочки желудка заключается в уменьшении численности клеток, продуцирующих ферменты (пепсины) и париетальные клетки, выделяющие соляную кислоту, и клеток, которые вырабатывают фактор Кастла.
Анатомия желудка
Условно в желудке различают несколько отделов:
- кардиальный отдел – самый начальный, куда пища поступает из пищевода,
- дно — самая верхняя куполообразная часть желудка, расположенная в самом верху желудка и где всегда имеется немного воздуха,
- тело желудка (фундальный отдел), где вырабатываются ферменты и соляная кислота и находится пища во время переваривания,
- выходной отдел или пилорический отдел желудка (антральный отдел), который заканчивается пилорическим сфинктером, ограничивающим полость желудка и отделяющим его от 12-перстной кишки.
Атрофия клеток желудка может затрагивать все отделы желудка, и тогда мы говорим о тотальном поражении органа или затрагивать конкретные отделы – фундальный (поражение тела желудка), антральный (выходной отдел желудка), или избирательно поражать часть клеток желудка. Клинические проявления атрофии в разных отделах желудка будут разные.
Известно, что желудок — это полый орган, куда пища попадает из ротовой полости и где происходит желудочное переваривание пищи: депонирование пищи, механическая и химическая переработка пищи и эвакуация ее из желудка в кишечный тракт.
Цитология желудка
В слизистой каждого отдела имеются различные клетки, отвечающие за переваривание пищи и участие в кроветворении:
- обкладочные (или париетальные) и главные клетки тела желудка, которые вырабатывают соляную кислоту,
- пепсиногены, которые под действием соляной кислоты переходят в активный фермент пепсин, переваривающий белки пищи,
- химозин и липаза, переваривающие молоко,
- фактор Кастла (гастромукопротеин), который отвечает за участие желудка в кроветворении и обмене витамина В12. Фактор Кастла связывается с витамином В12 белковой пищи в присутствии кальция и переносит витамин В12 в кишечник, где он всасывается в организм. При недостатке выработки фактора Кастла развивается В12-дефицитная анемия (снижение гемоглобина крови).
Добавочные слетки слизистой оболочки желудка образуют слизь практически во всех отделах желудка. Эта слизь выполняет защитную функцию от желчи, лекарств, которые принимает пациент, соляной кислоты.
В выходном отделе желудка имеются эндокринные клетки — G клетки, которые вырабатывают стимулятор образования пепсиногенов, соляной кислоты, отвечают за состояние моторной функции желудка.
Атрофический гастрит — причины развития
Наиболее частой причиной, вызывающей атрофический гастрит в настоящее время, считается инфекция Helicobacter pylori. В желудке развивается поверхностный гастрит и при длительном существовании инфекции переходит в атрофический.
Инфекция желудка ассоциируется с поражением антрального отдела желудка в виде ограниченного или тотального поражения этого отдела – атрофический гастрит антрального отдела и тела желудка. Развитие атрофических процессов в желудке может быть результатом возрастных изменений слизистой, генетических особенностей, обусловленных гипо- или атрофией слизистой желудка, лекарственным поражением желудка, длительным приемом антисекреторных препаратов (ИПП).
Аутоиммунный атрофический гастрит, когда организм начинает вырабатывать антитела против своих клеток слизистой оболочки желудка встречается достаточно редко.
Первые признаки
Заболевание сопровождают характерные признаки локального и общего характера:
- отрыжка;
- тошнота;
- срыгивание;
- ощущение тяжести и давления в подложечной зоне после приема пищи;
- неприятное ощущение в ротовой полости (особенно по утрам);
- изжога;
- жжение в эпигастрии.
Сразу после еды возникает боль тупого характера, в эпигастральной зоне; причем болевое ощущение увеличивается в положении стоя и при ходьбе. Очень часто наблюдаются кишечные диспепсии: урчание, метеоризм. При пониженной кислотности обычно возникает диарея, которая значительно обостряется после выпитого молока или съеденной жирной пищи.
Как подтвердить диагноз «атрофический гастрит»
Диагноз хронического атрофического гастрита является морфологическим. Если проводится эндоскопическое обследование, то при подозрении на атрофические процессы в желудке должны быть взяты биопсии слизистой оболочки желудка и дана гистологическая интерпретация изменений в ней.
В морфологическом диагнозе должны быть учтены: поражение отдела желудка, состояние желез, выраженность и глубина воспаления и перестройки слизистой (метаплазия, дисплазия). Клинический диагноз «хронический атрофический гастрит» без морфологического подтверждения не имеет смысла.
Наиболее точным методом диагностики является эндоскопическое исследование с биопсией. Однако в связи с неравномерностью распространения атрофических процессов в слизистой оболочке желудка гистологические исследования могут давать ложноотрицательные результаты. Кроме того, биопсия является дорогим и трудоемким методом и не может проводиться каждому пациенту, а само эндоскопическое исследование является серьезным инвазивным методом исследования.
В настоящее время существует альтернатива биопсии слизистой оболочки желудка — скрининговый метод исследования «сывороточная биопсия», способный объективно отражать функциональное состояние слизистой оболочки желудка и его морфологическую основу по образцам сыворотки крови.
Сывороточная биопсия или Гастропанель (или тестовая панель) обеспечивает простой и достоверной путь для получения большой информации о структуре и функции слизистой оболочки желудка, с большой чувствительностью и специфичностью выявить пациентов, имеющих атрофический гастрит и тех, кто нуждается в дальнейшем обследовании – эндоскопическом исследовании желудка. Если тестовая панель выявляет атрофический гастрит, то проведение эндоскопического исследования обязательно с онконастороженностью.
Как проводится Гастропанель
Забор крови для определения маркеров атрофического гастрита проводится утром натощак и через 20 минут после белкового завтрака. Забор крови проводится в сывороточные пробирки, они центрифугируются для проведения анализов.
По анализу сыворотки крови определяются маркеры хронического атрофического гастрита. Маркерами атрофии слизистой оболочки фундального и антрального отделов желудка являются:
- Пепсиноген I, Пепсиноген II и их соотношение,
- Гастрин-17 и Гастрин-17, стимулированный после белкового завтрака,
- определение антител к хеликобактер пилори Ig G.
Тесты основаны на технологии иммуноферментного анализа.
Кроме того,
- определяются антитела к париетальным клеткам тела желудка при аутоиммунном атрофическом гастрите с высоким риском нарушений, связанных с дефицитом витамина В12, для чего определяется уровень витамина В12.
- Определяется гомоцистеин как фактора риска сосудистых и тромбоэмболических заболеваний.
- Для уточнения хеликобактерной инфекции проводится дополнительный тест острой фазы инфекции, определяются антитела Ig A и IgM.
К какому врачу обратиться?
При необходимости диагностики и лечения атрофического гастрита пациентов из Москвы приглашаем в медицинский в Химках. Преимущества лечения в нашем отделении:
- Гастрит диагностируется быстро, точно с минимальной потерей времени и нервов пациента. Предусмотрена возможность проведения гастроскопии во сне.
- После определения точной формы заболевания, степени его развития и других особенностей, гастроэнтерологи назначат комплексный курс эффективного лечения.
- Возможности современного эндоскопического оборудования
- По желанию пациента гастроскопия проводится в состоянии медикаментозного сна.
- Доступно: прием врача от 1500 рублей
- Удобно: работаем ежедневно с 8:00 до 21:00
- Быстро: проведем всю диагностику на первом приеме
- Полно: есть все необходимое оборудование
Несколько слов о сывороточных маркерах
Мы имеем диагностический алгоритм выявления заболеваний желудка, который показано проводить всем пациентам, имеющим боль или дискомфорт в верхних отделах живота.
Пепсиногены
Различают семь изоформ предшественников пепсина, из которых пять обозначают как группу Пепсиноген I главных клеток тела желудка и Пепсиноген II, равномерно секретируемый железами всего желудка и 12-перстной кишки. Образовавшиеся в желудке пепсиногены всасываются в кровь и определение сывороточного уровня их является общепризнанным маркером атрофического гастрита «серологическая биопсия».
Снижение уровня Пепсиногена I говорит о степени выраженности атрофического гастрита тела желудка, а поскольку активизация Пепсиногена I в активный пепсин происходит при участии соляной кислоты, то по уровню Пепсиногена I можно условно представить уровень кислотности желудка. Пепсиноген II вырабатывается во всех отделах желудка и в 12-перстной кишке. По мере увеличения тяжести атрофии уменьшается соотношение сывороточного уровня Пепсиногена I и Пепсиногена II, что свидетельствует о тяжести атрофии и распространении процесса.
Гастрин
Гастрин-17, вырабатываемый в выходном отделе желудка после стимуляции клеток различными факторами (растяжение желудка, белковой пищи). В случае атрофии слизистой антрального отдела желудка секреция Гастрина-17 снижается. Чтобы оценить наличие и тяжесть атрофического процесса в желудке, необходимо проведение пробы со стимуляций белком, снижение которой показывает степень выраженности атрофии, в случае атрофии слизистой антрального отдела желудка секреция Гастрина-17 пропорционально снижается. У пациентов с выраженным атрофическим гастритом в области антрального отдела желудка риск развития рака желудка в 90 раз выше, чем у людей с нормальной слизистой желудка.
Гомоцистеин
Гомоцистеин — ранний маркер клеточного функционального дефицита В12, В6, фолиевой кислоты вследствие развития атрофического гастрита и других причин – возраст, курение, хеликобактерная инфекция и др. При атрофическом гастрите уровень гомоцистеина повышается в крови и становится токсичным для организма. При сдаче крови на гомоцистеин следует отказаться за 1 день до исследования от белковой пищи, витаминов, гормональных контрацептивов. Этот тест может быть дополнением к Гастропанели или самостоятельным тестом при других заболеваниях.
О.Я. Бабак, д.м.н., профессор, директор Института терапии им. Л.Т. Малой АМН Украины, г. Харьков
Под атрофическим гастритом понимают прогрессирующий воспалительный процесс слизистой оболочки желудка, характеризующийся утратой желудочных желез. Клинико-морфологической особенностью атрофического гастрита являются уменьшение числа специализированных гландулоцитов, обеспечивающих секреторную функцию желудка, и замещение их клетками более простыми, в том числе вырабатывающими слизь. Обширная атрофия слизистой оболочки тела желудка, как правило, ассоциируется с гипосекрецией соляной кислоты и нарушением выработки пепсиногена.
Что сегодня известно об атрофическом гастрите? Наиболее частыми этиологическими факторами, вызывающими атрофический гастрит, признаны инфекция Helicobacter Pylori (Н.Pylori) и аутоиммунный гастрит. Причем, с Н. pylori связывают возникновение подавляющего большинства атрофических гастритов. Бактерии Н. рylori, персистируя на желудочном эпителии, вызывают хронический хеликобактерный поверхностный гастрит. Длительно существующий поверхностный хеликобактерный гастрит без соответствующего лечения трансформируется в атрофический. Атрофический гастрит клинически, как правило, в течение длительного времени ничем себя не проявляет, поэтому диагноз хронического гастрита, скорее, морфологический, нежели клинический. Основным методом диагностики атрофического гастрита является эндоскопическое исследование. При эндоскопии производят осмотр пищевода, желудка, двенадцатиперстной кишки. При выраженной атрофии слизистая оболочка желудка имеет характерные отличия в сравнении с таковой при, например, поверхностном гастрите. Окончательный диагноз позволяет установить морфологический анализ биоптатов слизистой оболочки желудка, взятых во время эндоскопии. Морфологически атрофия определяется уменьшением числа функционирующих специализированных клеток желудка. Доказано, что при Н. pylori-ассоциированном гастрите процессы атрофии чаще возникают при инфицировании определенными штаммами (Cag A+ и Vac A+) Н. pylori. Одним из морфологических признаков атрофического гастрита является кишечная метаплазия, которая традиционно рассматривалась как предраковое изменение слизистой оболочки желудка. Другие методы исследования – рентгенография желудка, ультразвуковое исследование брюшной полости и компьютерная томография – в плане диагностики атрофического гастрита неинформативны.
Чего нужно опасаться при атрофическом гастрите? Каков прогноз болезни? Гипотетически наличие атрофического гастрита при естественном течении может иметь два сценария. Первый – длительно существующий хронический гастрит приводит к значительному уменьшению кислотообразующей функции желудка, требующему заместительной терапии, без которой будут наблюдаться признаки нарушения пищеварительной функции. Второй вариант – в результате длительного хронического персистирующего воспаления в слизистой оболочке желудка, характерного для Н. pylori-ассоциированного гастрита, происходит нарушение клеточного обновления в желудке, что способствует появлению клеток-мишеней для влияния на них канцерогенных веществ, в дальнейшем – к клеточным мутациям. В результате нормальный клеточный эпителий желудка замещается метапластическим, диспластическим и неопластическим. По определению ВОЗ, под дисплазией понимают такие клеточные изменения, при которых часть эпителия замещена клетками с различной степенью атипии. В международной классификации эпителиальных неоплазий пищеварительного тракта (2000) дисплазия – это неоплазия, другими словами – опухоль. Итак, атрофический гастрит может трансформироваться в рак желудка. Наибольшую опасность в плане развития рака представляет атрофический гастрит с пониженной кислотообразующей функцией желудка (частота возникновения рака – до 13%). Среди известных в настоящее время молекулярных механизмов, лежащих в основе наследственной предрасположенности к раку желудка, выделены: индукция экспрессии TGF-β1, частичный полиморфизм кластера гена IL-1 (IL-1β). В результате развития атрофии слизистой оболочки желудка снижается ее противоопухолевая защита, создаются условия для активного воздействия канцерогенов. При возникновении тяжелой атрофии эпителия тела желудка риск развития рака желудка повышается в 5 раз в сравнении с таковым при неатрофическом гастрите. Бактерии Н. pylori относят к биологическим канцерогенам в отношении рака желудка. Большинство исследователей считают, что Н. pylori – это основной этиологический фактор развития хронического гастрита, который является обязательным звеном в каскаде процессов, приводящих к раку желудка. На основании анализа результатов многоцентровых исследований Международное агенство по изучению рака при ВОЗ еще в 1994 году рекомендовало считать инфекцию Н. pylori абсолютным канцерогеном для человека. В настоящее время рак желудка рассматривается как конечный результат длительного многоступенчатого и многофакторного процесса, в котором клеточные изменения слизистой оболочки желудка обусловлены нарушениями микроокружения. Этот процесс называют именем описавшего его автора – каскадом Корреа (1995). Он включает хронический гастрит, кишечную метаплазию, дисплазию и рак. Н. рylori-ассоциированный желудочный канцерогенез – многоэтапный процесс, характеризующийся развитием хронического гастрита – первой ступени в эволюционном каскаде. Последующие изменения приводят к формированию атрофии, тонкокишечной (I и II типы) и толстокишечной (III тип) метаплазий и дисплазии желудочного эпителия, в итоге – к аденокарциноме желудка. Именно атрофический гастрит занимает срединное положение в цепи вышеперечисленных изменений на пути к раку желудка.
Как избежать трансформации атрофического гастрита в рак желудка? Ответ на данный вопрос состоит из равных по значимости частей: как можно раннее выявление предраковых изменений, их адекватное лечение и предупреждение (профилактика) проявления последних. При наблюдении больных хроническим гастритом важно уловить тот момент, когда возникает и начинает прогрессировать атрофия слизистой оболочки желудка, причем желательно это проводить простым информативным и неинвазивным способом.
Своевременное выявление атрофии слизистой оболочки желудка – первый диагностический этап выявления риска по раку желудка.
Многочисленные исследования последних лет показали, что очаги полной и неполной кишечной метаплазии слизистой оболочки желудка нельзя расценивать в качестве достоверного маркера повышенного риска развития рака желудка. Исследования свидетельствуют, что значительно важнее оценка не типа метаплазии, а ее объема. Так, при большом объеме метаплазии, превышающем 20% поверхности желудочного эпителия, создаются реальные условия для развития дисплазии с последующим образованием аденокарциномы желудка. Следовательно, риск развития рака желудка повышается при тяжелой атрофии желудочного эпителия, характеризующейся обширными очагами кишечной метаплазии. Как же на практике определить площадь такого поражения? Следует помнить, что данные изменения происходят на клеточном уровне, и при обычной эндоскопии их распознать невозможно. Доступным и эффективным способом диагностики метапластических изменений в слизистой оболочке желудка является метод хромогастроскопии – прижизненная окраска слизистой желудка красителем (чаще метиленовым синим), проводимая во время эндоскопического исследования. Данная методика основана на поглощении красителя очагами кишечной метаплазии, что позволяет оценить их размеры, выполнить прицельную биопсию для гистологического анализа биоптата слизистой и выявить возможную дисплазию или метаплазию. Вместе с тем морфологическая диагностика атрофического гастрита сопряжена с рядом трудностей. Сложность постановки диагноза атрофии морфологическим методом обусловлена тем, что на ранних стадиях процесс никогда не бывает диффузным, следовательно, результаты гастробиопсии могут способствовать гипер- и гиподиагностике. При воспалении может изменяться микроскопическая картина и неадекватно оцениваться проявления атрофического гастрита из-за ложного вывода о потере желез. Высока и субъективность методики. Все это заставляет искать другие надежные пути тестирования атрофических изменений слизистой оболочки желудка. Разработан ряд малоинвазивных гематологических тестов (тестовая панель Biohit), позволяющих избежать ошибок диагностики, дать совокупную оценку состояния слизистой оболочки желудка, степени ее атрофии и потери нормальных желез и клеток в антральном отделе и теле желудка. Во время проведения эндоскопического исследования обязательно должна проводиться детекция на наличие Н. pylori. При этом наиболее целесообразным следует признать уреазный или гистологический методы (из гастробиоптатов) исследования. Определение уровня сывороточного пепсиногена (S-PGІ) или соотношения содержания пепсиногена I к пепсиногену II (PGI/PGII) – неэндоскопический метод диагностики атрофического гастрита с поражением тела желудка. С увеличением степени атрофии слизистой оболочки тела желудка (потеря нормальных кислотообразующих желез) уровни S-PGI и PGI/PGII постепенно снижаются. Определение уровня гастрина в сыворотке крови, преимущественно гастрина-17 (S-G-17), может быть использовано в качестве индикатора морфологического состояния слизистой оболочки антрального отдела желудка. То есть снижение S-G-17 является биохимическим маркером атрофического гастрита с поражением антрального отдела желудка (потеря антральных G-клеток). Снижение уровней S-G-17 и S-PGI можно рассматривать как результат прогрессирующего атрофического гастрита с потерей нормальных желез и клеток слизитой оболочки тела и антрального отдела желудка. G-17 практически полностью синтезируются и секретируются G-клетками антрального отдела желудка. Эти клетки являются компонентами нормальных антральных желез, в случае прогрессирования атрофического гастрита их количество уменьшается на фоне поражения антральных желез и появления кишечной метаплазии. При Н. pylori-ассоциированном гастрите имеется тенденция к возрастанию серологических уровней G-17 и PGI. Низкая внутрижелудочная кислотность способствует увеличению серологического уровня G-17, и наоборот. Перманентная длительная гипо- или ахлоргидрия приводят к чрезвычайно высоким уровням G-17 в крови. Особенно часто это наблюдается при пониженной кислотности (атрофический гастрит с поражением тела желудка) в сочетании с сохраненной слизистой оболочкой антрального отдела. Такая клиническая картина наиболее характерна для аутоиммунного атрофического гастрита. Если в антральном отделе имеются сопутствующие признаки атрофии слизистой оболочки (мультифокальный атрофический гастрит), тогда содержание S-G-17 не возрастает, и тестовая панель показывает низкие значения уровней S-PGI и S-G-17. Совокупная точность тестовой панели в диагностике атрофического гастрита – около 80% (при сопоставлении с результатами эндоскопии и биопсии). Данная тестовая панель является малоинвазивной альтернативой первоначального обследования пациентов с подозрением на желудочную атрофию и дисплазию. Она позволяет надежно выявлять пациентов с различными формами гастрита, определять локализацию и этиологию патологического процесса, оценивать вероятность развития рака желудка и выстраивать дальнейшую тактику ведения больного. Учитывая связь возникновения атрофии желудочного эпителия и кишечной метаплазии с инфекцией Н. pylori, становится очевидным выбор метода лечения и профилактики дальнейшего прогрессирования процесса. Методом выбора является антихеликобактерная терапия. В 2002 году японские исследователи убедительно доказали возможность регрессии метапластических изменений слизистой оболочки желудка после успешного уничтожения бактерий Н. pylori. С помощью хромоскопии им удалось установить, что в течение пяти лет после проведения успешной антихеликобактерной терапии размеры очагов кишечной метаплазии уменьшились почти в 2 раза в сравнении с исходными. В последующих исследованиях подтвердилась целесообразность такого терапевтического подхода. В настоящее время не вызывает сомнений необходимость проведения антихеликобактерной терапии пациентам с атрофическим гастритом. Предварительные данные нескольких многоцентровых исследований по мониторингу Н. pylori-ассоциированного предрака и рака желудка свидетельствуют в пользу реверсии воспаления слизистой оболочки желудка и связанных с ней атрофии, кишечной метаплазии и генетической нестабильности. В связи с этим в идеале пациентам с Н. pylori-позитивным хроническим атрофическим гастритом необходимо проводить эрадикационную терапию, а при отсутствии эффекта – исследование с целью выявления маркеров генетической нестабильности и тщательный мониторинг. Данная рекомендация нашла отражение в международных рекомендациях по диагностике и лечению заболеваний, ассоциированных с Н. pylori – Маастрихтском консенсусе 3 (2005). Для уничтожения бактерий Н. pylori, как и в Маастрихтском консенсусе 2 (2000), рекомендованы трех- и четырехкомпонентные схемы антибактериальных препаратов в сочетании с ингибиторами протонной помпы (ИПП) в стандартных дозах: ИПП + кларитромицин + амоксициллин и ИПП + тетрациклин + метронидазол (фуразолидон) + коллоидный висмут. Вместе с тем следует помнить, что полное восстановление структуры слизистой оболочки при тяжелой атрофии до нормы требует длительного времени, и в ряде случаев, по всей видимости, это не возможно. В случаях, когда предопухолевые процессы не подвергаются обратному развитию либо прогрессируют, необходимо применять более радикальные методы лечения, используя арсенал современных эндоскопических операций, вплоть до резекции слизистой оболочки желудка. Главная цель первичной профилактики атрофического гастрита – своевременное и эффективное лечение поверхностного хеликобактерного гастрита. Для этого используют стандартные схемы антихеликобактерной терапии, в соответствии с рекомендациями Маастрихтских консенсусов 2 (2000) и 3 (2005). Важным моментом является последующий контроль за успешностью этой терапии. Контроль необходимо проводить с использованием неинвазивных методов (дыхательного уреазного или стул-теста). При неудачной эрадикации проводить повторные курсы лечения. Кроме того, доказано, что, придерживаясь здорового режима питания, можно снизить онкологический риск (прогрессирование атрофии), что подтверждено в исследованиях, проведенных в ряде стран. Рекомендуется избегать употребления консервированных, маринованных и копченых продуктов, отказаться от курения и употребления крепких спиртных напитков (особенно в сочетании с жирной, жареной, копченой и соленой пищей), исключить переедание. Необходимо контролировать массу тела, выполнять активные физические нагрузки, употреблять больше свежих овощей (в том числе лук и чеснок), фруктов и натуральных соков, витаминов А, С, b-каротина, зелени, круп грубого помола, молочных продуктов. В некоторых развитых странах Европы и США внедрение здорового образа жизни привело к снижению заболеваемости раком желудка в несколько раз, сегодня это заболевание в этих странах считается редким, составляя лишь 3% среди злокачественных новообразований. Мониторирование – постоянное наблюдение с периодическим повторным обследованием – абсолютно обязательно для пациентов с атрофическим гастритом Итак, в настоящее время очевидна необходимость особого внимания к атрофическому гастриту. Комплексное применение современных методов исследования – эндоскопического, морфологического, гематологического (тестовой панели) и других – способствует его точной диагностике. Использование эффективных методов лечения и профилактики атрофического гастрита, устранение условий, которые способствуют его развитию, представляют сегодня реальную возможность улучшить прогноз этого заболевания, устранить риск развития рака желудка.
Литература 1. Е.Г. Бурдина, Е.М. Майорова, Е.В. Григорьева, И.И.Тимофеева, О.Н. Минушкин // Гастрин-17 и пепсиноген І в оценке состояния слизистой оболочки желудка // Российский медицинский журнал, 2006, №2, с. 9-11. 2. Х. Ваананен, М. Ваухконен, Т. Хэлске, И. Каариянен, М. Расмуссен, Х. Тунтури-Хихнала, Дж. Коскенпато, М. Сотка, М. Турунен, Р. Сандстрем, М.Ристиканкаре, А. Юссила, П. Сиппонен // Неэндоскопическая диагностика атрофического гастрита на основании анализа крови: корреляция между результатами гистологического исследования желудка и уровнями гастрина-17 и пепсиногена І в сыворотке // Клинические перспективы гастроэнтерологии, гепатологии, 2003, № 4, с. 26-32. 3. В.Д. Пасечников, С.З. Чуков, С.М. Котелевец / Профилактика рака желудка на основе эрадикационной терапии предопухолевых заболеваний // Российский журнал гастроэнтерологии, гепатологии, колопроктологии, 2003, № 4, с. 11-19. 4. А.А. Шептулин, В.А. Киприанис / Диагностика и лечение инфекции Helicobacter pylori: основные положения согласительного совещания «Маастрихт – 3» // Российский журнал гастроэнтерологии гепатологии колопроктологии, 2006, № 2, с. 88-91. 5. Kim N., Lim S. H., Lee K.H. et al. Long-term effects of Helicobacter pylori eradication on intestinal metaplasia in patients with duodenal and behign gastric ulcers Dig. Dis. Sci. – 2000. – Vol. 45. – 1754-1762. 6. Malfertheiner P., Megraud F., O’Morain C. еt al. Current concepts in the management of Helicobacter pylori infection – The Maastricht 2 Concensus Report // Aliment. Pharmacol. Ther. – 2002. – Vol. 16. – P. 167-180.
Достоинства Гастропанели для постановки диагноза «атрофический гастрит»
Таким образом, Гастропанель позволяет ответить на следующие вопросы:
- есть ли у пациента атрофический гастрит, в каком отделе желудка локализуются изменения,
- оценить риск развития рака желудка и язвенной болезни,
- страдает ли пациент гастритом, вызванным хеликобактер пилори,
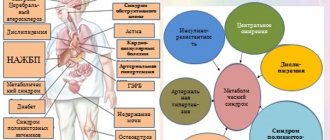
- выявить аутоиммунный гастрит или атрофический гастрит с поражением тела желудка, что может определять риск развития дефицита витамина В12, который может быть связан с многими заболеваниями (атеросклероз, поражение сосудов мозга и сердца, депрессию, полиневропатии, деменцию и др.)
Какие же достоинства Гастропанели можно отметить: это простой неинвазивный серологический тест, отмечена высокая чувствительность, специфичность, безопасность и удобство для пациента, быстрое получение результатов, отвечает принципам доказательной медицины.
Симптомы
Чем больше снижена кислотность, тем отчетливее будут проявляться симптомы гастрита с пониженной кислотностью:
- Признаки избыточного размножения бактерий — урчание, неустойчивый стул, непереносимость молока, вздутие в животе. Если гастрит сопровождается частыми поносами, то может наступить похудание, развиться признаки дефицита минералов или витаминов.
- Дистрофия — признаки дефицита витаминов группы В, а также С, Е, Д, белковая недостаточность (похудение, «полированный» или обложенный густым белым налетом язык).
- Диспепсия — ухудшение аппетита, чувство тяжести или переполнения в желудке, отрыжка тухлой пищей, плохой запах изо рта (кокосмия), неприятный привкус, тошнота.
- Тупые, усиливающиеся после еды, без четкой локализации, ноющие боли, которые возникают вследствие растяжения желудка.
- Развитие анемии за счет снижения всасываемости железа и витамина В12 (из-за фактора Касла).
Так как воспаление желудка затрагивает и другие отделы системы пищеварения, то часто гипоацидный гастрит сопровождается такими заболеваниями, как энтероколит, холецистит, панкреатит.
Что делать, если у вас выявили атрофический гастрит
Несколько слов о принципах лечения хронического атрофического гастрита. Подходы к лечению индивидуальные, всё зависит от выраженности атрофических процессов, наличия хеликобактера, дефицита витамина В12.
Проблемой будет заниматься врач, который назначит:
- лечение,
- повторные исследования на предмет контроля лечения,
- повторные консультации для оценки клинических проявлений заболевания и коррекции лечения.
Наиболее трудно устранить аутоиммунные механизмы поражения слизистой желудка, вопрос назначения гормональных препаратов встает только при сопровождении гастрита анемией. Эрадикационная терапия хеликобактер пилори имеет свои особенности. Прежде всего встает вопрос о кислотности желудочного сока, и чаще лечение проводят без антисекреторных препаратов. Исследование кислотности желудочного сока рН-метрическим методом проводят в настоящее время редко (чаще суточное мониторирование в условиях стационара), но возможна ориентация кислотности по уровню Пепсиногена I.
Высокий уровень Пепсиногена, периодические изжоги у пациента могут свидетельствовать о сохраненной секреции желудка. При атрофическом гастрите при гипо или анацидном состоянии с поражением тела и выходного отдела желудка исключаются антисекреторные препараты и эрадикация хеликобактекр пилори проводится антибиотиками. Эффективная эрадикация инфекции улучшает процессы в слизистой желудка, и ее возможно рассматривать как профилактику развития рака желудка.
Диагностика
Диагностированием и лечением гастритов с низкой кислотностью занимается гастроэнтеролог и врач-эндоскопист. Специалист проводит осмотр пациента и проводит ряд обследований:
- морфологические исследования;
- рентгенографию желудка;
- эзофагогастродуоденоскопию;
- эндоскопическую биопсию;
- гастроскопию;
- определение уровня пепсиногена;
- зондирование желудка с внутрижелудочной рН-метрией;
- исследование желудочного сока;
- диагностирование pylori с помощью метода ИФА кала, ПЦР-исследования, выявления антител в крови и дыхательного теста на данный микроорганизм.
Цель данных исследований – не спутать заболевание с другими патологиями, и поставить точный диагноз. По результатам обследований гастроэнтеролог назначает схему лечения. Если требуется, лечащий врач направляет на консультацию к диетологу, который составляет соответствующую диету. В отдельных случаях для устранения сопутствующих заболеваний требуется консультация других специалистов узкой направленности (кардиолога, терапевта).
Питание при хроническом атрофическом гастрите
Строгого ограничения в питании нет, но необходимо знать, что некоторые продукты ощелачивают желудок (в основном белковая пища) и еще больше снижают кислотность желудочного сока, и есть продукты, которые стимулируют её (овощные и фруктовые соки, овощи, фрукты).
Чаще всего врачи назначают диету 2, цель которой механическое щажение слизистой желудка и сохранение химических раздражителей.
Но врачебный опыт показывает, что строгих ограничений не требуется. Необходимый режим питания – еда малыми порциями с препаратами заместительной терапии позволяет иметь хорошее желудочное пищеварение, при котором в желудке переваривается и белковая пища.
Атрофический гастрит — лечение
Заместительная терапия
Проведение заместительной терапии включает применение препаратов соляной кислоты и ферментов желудочного сока:
- Натуральный желудочный сок — препарат животного происхождения, по составу соответствующий желудочному соку человека, содержит соляную кислоту и ферменты. Применяется по 1-2 столовые ложки (15 – 30 мл) во время еды или после еды 2-3 раза в день.
- Ацидин-пепсин, содержащий бетаин гидрохлорид, который гидролизуется в желудке с выделением свободной соляной кислоты и фермента пепсина. Перед употреблением таблетки (500 мг) растворяют в 50-100 мл воды и применяют во время еды. Эти препараты применяются через соломинку.
- Абомин – препарат содержит сумму протеолитических ферментов желудка и получается из слизистой оболочки желудка телят и ягнят. Применяется по 1 таблетке (по 0,2 г с содержанием в 1 табл. 50 000 ЕД) 2 — 3 раза в день во время еды в течение 1- 3 месяцев.
Стимулирующая терапия
Некоторые средства, стимулирующие секрецию желудочного сока:
- Минеральная вода (Ессентуки N17, Нарзан) применяют в теплом виде за 15-20 минут до еды, курс 2-3 недели два раза год.
- Отвар шиповника, капустный, томатный, морковный, лимонный соки по 50 мл, разведенные кипяченой водой 1:1 перед едой, чередовать.
- Лекарственные сборы: подорожник, зверобой, полынь, чабрец в равных соотношениях.
- Широко используется Плантаглюцид — гранулы листьев подорожника для приготовления суспензии, для чего берется 1/1 -1 чайная ложка (½-1 г) на ¼ стакана теплой воды и применяется за 30 минут до еды 2-3 раза в день, курс лечения 3-4 недели, для профилактического лечения 1-2 месяца. Плантаглюцид активизирует желудочную секрецию, обладает обволакивающим, регенераторным, противовоспалительным и спазмолитическим действием.
- Сбор фитотерапевта Михальченко С.И.:
Состав: дягиль, тысячелистник, одуванчик, береза, вахта трёхлистная, подорожник, тмин, кровохлебка, солодка голая, дымянка лекарственная, календула, ромашка аптечная. Применение: 1 десертную ложку смеси залить 500 мл кипятка, настаивать в термосе по объему ночь, процедить. Принимать по 150 мл 3 раза в день за час до еды. Перед употреблением подогреть, разбавив горячей водой. Хранить в холодильнике. Прием: 10 дней прием — 2 дня перерыв, 3-4 месяца.
В период относительной ремиссии атрофического гастрита главными препаратами являются средства заместительной и стимулирующей терапии, которые влияют на секреторную недостаточность желудка.
Диета и правильное питание
Если у вас гастрит с пониженной кислотностью, обязательна строгая диета. В нее стоит включить:
- Крупы и макароны. Разрешается рис, гречка, овсянка, манная крупа.
- Супы – на нежирном курином или рыбном бульоне, овощные, вермишелевые, крупяные, с фрикадельками.
- Нежирное мясо (курятина, говядина, кролик, индейка). Рыба (судак, хек, минтай, щука).
- Яйца – не более 2 штук в день.
- Приправы и соусы – растительное масло, соль, зелень.
- Овощи – свекла, тыква, морковь, помидоры, кабачки, капуста цветная.
- Молочные продукты – творог, сметана, неострый сыр, молоко, йогурт.
- Сладкое – галетное печенье, пастила, зефир, мармелад.
- Фрукты и ягоды – в протертом виде (кисели, компоты, желе, суфле).
- Напитки – чай, отвар шиповника, некрепкий кофе.
- Хлебобулочные изделия – вчерашний белый хлеб, несдобные сухари.
Из рациона исключить:
- Выпечку, сладости, свежий хлеб.
- Супы с грибами и на жирных бульонах.
- Бобовые культуры, ячневую, кукурузную и пшенную кашу.
- Крупнозернистые и с грубой кожицей ягоды, сухофрукты.
- Острые соусы, покупные заправки, майонез.
- Жирное мясо и рыбу.
- Огурцы, болгарский перец, капусту, репу, редис, грибы. Нельзя соленья и маринады.
- Фастфуд, алкоголь, газированные напитки, пакетированные соки.
Важно, чтобы питание было дробным – 5-6 раз в день. Перекусывать лучше овощным или фруктовым пюре или молочными продуктами.
Диета при гастрите с пониженной кислотностью достаточно лояльная – пациент не будет страдать от голода, но одновременно и не будет испытывать чувство переедания. Если предложенного рациона питания придерживаться длительное время, то симптомы гастрита будут появляться все реже и наступит длительная ремиссия.