Форма выпуска
Выпускается в виде растительного сбора, который выглядит как небольшие желто-коричневые кусочки растительного сырья с вкраплениями желтого, белого, зелёного или коричневого цвета. Характерен сильный аромат. Водная вытяжка горько-сладкая.
Лекарство расфасовывают в пакеты по 50 г или в маленькие пакетики по 1,5 г. В картонную пачку помещают пакет на 50 г или 20 пакетиков по 1,5 г.
В маленьких пакетиках находится растительное сырьё, которое измельчено сильнее, почти до порошкообразной консистенции.
Фармакодинамика и фармакокинетика
Фармакодинамика
То, как влияет Фитогастрол (желудочно-кишечный сбор) на организм человека, обусловлено свойствами растений, входящих в его состав:
- листья перечной мяты стимулируют секрецию желудочного сока, повышают эффективность пищеварительного процесса;
- корень солодки содержит вещество глицеризин, которое способствует заживлению язв и предотвращает их появление;
- цветы ромашки стимулируют регенерационные процессы;
- плоды укропа огородного содержат целый комплекс биологически активных веществ (эфирное масло, флавоноиды, каротин, фитонциды, сахара, витамин C и другие), что обуславливает желчегонное, спазмолитическое, мочегонное действие, помогает справиться с газообразованием в кишечнике, повышает секреторную активность желудочных желез;
- комплекс биологически активных веществ, содержащийся в корневищах аира, влияет на окончания вкусовых рецепторов, вызывая повышение аппетита, повышает качество пищеварительного процесса, усиливает рефлекторную секрецию желудочного сока, повышает желчевыделение, повышает тонус желчного пузыря, стимулирует мочеотделение.
Фармакокинетика
Не изучена.
Сбор желудочно-кишечный Фитогастрол N20 фильтр-пакеты
Латинское название
Phytogastrol
Действующее вещество: Аира корневища + Мяты перечной листья + Ромашки аптечной цветки + Солодки корни + Укропа огородного плоды (Acori calami rhizomata + Menthae piperitae folia + Chamomillae recutitae flores + Glycyrrhizae radices + Anethi graveolentis fructus)
Состав
Каждый грамм сбора содержит по 200 мг действующих веществ: цветов ромашки, листьев мяты перечной, плодов укропа огородного, корневищ аира и корней солодки.
Форма выпуска
Выпускается в виде растительного сбора, который выглядит как небольшие желто-коричневые кусочки растительного сырья с вкраплениями желтого, белого, зелёного или коричневого цвета. Характерен сильный аромат. Водная вытяжка горько-сладкая.
Лекарство расфасовывают в пакеты по 50 г или в маленькие пакетики по 1,5 г. В картонную пачку помещают пакет на 50 г или 20 пакетиков по 1,5 г.
В маленьких пакетиках находится растительное сырьё, которое измельчено сильнее, почти до порошкообразной консистенции.
Фармакологическое действие
Является растительным препаратом, влияющим на пищеварительную систему. Обладает спазмолитическим, противовоспалительным, обволакивающим, желчегонным действием и способен корректировать работу желудочных желез.
Фармакодинамика и фармакокинетика
Фармакодинамика
То, как влияет Фитогастрол (желудочно-кишечный сбор) на организм человека, обусловлено свойствами растений, входящих в его состав:
листья перечной мяты стимулируют секрецию желудочного сока, повышают эффективность пищеварительного процесса;
корень солодки содержит вещество глицеризин, которое способствует заживлению язв и предотвращает их появление;
цветы ромашки стимулируют регенерационные процессы;
плоды укропа огородного содержат целый комплекс биологически активных веществ (эфирное масло, флавоноиды, каротин, фитонциды, сахара, витамин C и другие), что обуславливает желчегонное, спазмолитическое, мочегонное действие, помогает справиться с газообразованием в кишечнике, повышает секреторную активность желудочных желез;
комплекс биологически активных веществ, содержащийся в корневищах аира, влияет на окончания вкусовых рецепторов, вызывая повышение аппетита, повышает качество пищеварительного процесса, усиливает рефлекторную секрецию желудочного сока, повышает желчевыделение, повышает тонус желчного пузыря, стимулирует мочеотделение.
Фармакокинетика
Не изучена.
Показания к применению
Желудочный сбор Фитогастрол показан при различных заболеваниях пищеварительного тракта, например, при колитах, гастритах, функциональной диспепсии. Обычно используется в комплексе с другими лекарствами.
Противопоказания
Применение Фитогастрола противопоказано при:
повышенной чувствительности к одному или нескольким ингредиентам, входящим в состав сбора;
калькулёзном холецистите;
обострении язвенной болезни желудка и двенадцатиперстной кишки;
лечении пациентов младше 12 лет;
во время беременности и кормления грудью.
Побочные действия
Могут появиться симптомы аллергии. В таком случае нужно проконсультироваться с врачом, как принимать Фитогастрол в дальнейшем и стоит ли это делать.
Фитогастрол, инструкция по применению (Способ и дозировка)
Столовую ложку сбора пересыпают в эмалированную или стеклянную посуду, заливают стаканом кипятка, закрывают и 15 минут держат на кипящей водяной бане. Затем охлаждают в течение 45 мин, процеживают и отжимают. К настою доливают воду так, чтоб его объем стал равным 200 мл.
2 пакетика кладут в стеклянную или эмалированную посуду, добавляют стакан кипятка, настаивают 15 минут. Потом пакетики отжимают, а объём раствора доводят до 200 мл.
Пить нужно по половине стакана за полчаса до еды. Приём повторяют трижды за день. Длительность курса лечения подбирается лечащим врачом индивидуально для каждого пациента, так как зависит от характера болезни.
Перед тем, как выпить часть раствора, его необходимо хорошо взболтать. Хранить готовый раствор можно только в холодильнике и не дольше 2 суток.
Передозировка
Не было сообщений о передозировке.
Взаимодействие
Не известно.
Условия продажи
Без рецепта.
Условия хранения
Необходимо хранить в оригинальной упаковке в сухо прохладном месте.
Срок годности
2 года (сухой сбор), 2 суток (приготовленная водная вытяжка).
Детям
Не применяют для лечения пациентам младше 12 лет.
При беременности и лактации
Нежелательно назначать беременным и женщинам, кормящим грудью, так как ещё не проводились клинические исследования относительно безопасности использования Фитогастрола для таких категорий пациентов.
Фитогастрол, инструкция по применению (Способ и дозировка)
Столовую ложку сбора пересыпают в эмалированную или стеклянную посуду, заливают стаканом кипятка, закрывают и 15 минут держат на кипящей водяной бане. Затем охлаждают в течение 45 мин, процеживают и отжимают. К настою доливают воду так, чтоб его объем стал равным 200 мл.
2 пакетика кладут в стеклянную или эмалированную посуду, добавляют стакан кипятка, настаивают 15 минут. Потом пакетики отжимают, а объём раствора доводят до 200 мл.
Пить нужно по половине стакана за полчаса до еды. Приём повторяют трижды за день. Длительность курса лечения подбирается лечащим врачом индивидуально для каждого пациента, так как зависит от характера болезни.
Перед тем, как выпить часть раствора, его необходимо хорошо взболтать. Хранить готовый раствор можно только в холодильнике и не дольше 2 суток.
Грибковые поражения желудочно-кишечного тракта
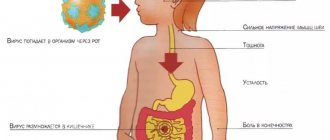
Сегодня человечество переживает эпидемию оппортунистических инфекций, среди которых микозам принадлежит одно из ведущих мест. По данным ВОЗ, в последнее десятилетие около 20% населения мира страдает микозами [1]. Микозы – инфекционные заболевания, этиологическим возбудителем которых являются грибы. Чаще всего микозом болеют люди, имеющие первичные или вторичные иммунодефицитные состояния [2]. Микоз относится к оппортунистическим инфекциям [3, 4]. Грибы – низшие растения (более 100 тыс. видов), лишенные хлорофилла, поэтому для их существования требуются готовые органические вещества. Подавляющее большинство грибов относится к сапрофитам, меньшая часть из них – паразиты человека и животных. Около 500 видов грибов могут вызывать инфекционные болезни у человека. Чаще всего у человека встречаются дрожжеподобные С. albicans [5]. Кандидоз – антропонозный микоз, характеризующийся поражением слизистых оболочек и кожи. Поражения у человека вызывают С. albicans (более 90% поражений), С. tropicalis, С. krusei, С. lusitaniae, С. parapsilosis, С. kefyr, С. guilliermondii и др. [6–8]. В начале XX в. кандидозы наблюдали сравнительно редко. С началом применения антибиотиков и по настоящее время заболеваемость кандидозами значительно возросла и продолжает расти. Немаловажное значение в развитии кандидозов имеет неблагоприятная экологическая обстановка, оказывающая отрицательное воздействие на иммунную систему организма человека [9]. Кандидоз обычно возникает эндогенно в результате дисфункций иммунной системы и дисметаболических расстройств в организме. В последние годы кандиды являются наиболее распространенными возбудителями оппортунистических микозов [4]. При поражении организма кандидами возможно развитие тяжелых висцеральных форм, чаще с вовлечением легких и органов пищеварения и других систем организма. Кандидоз может носить системный характер и стать диссеминированным (массивный рост возбудителя в организме) и принять картину грибкового сепсиса с поражением всех органов (почек, сердца, селезенки, мозга), а иногда с развитием септического шока [10]. Чаще эта форма кандидоза поражает больных с последней стадией рака и СПИДа [11, 12]. Этиология и патогенез
Наиболее часто встречающийся возбудитель микозов С. albicans – нормальный комменсал полости рта, ЖКТ, влагалища и иногда кожи. С. albicans относятся к условно-патогенным микроорганизмам с высоким уровнем носительства и с выраженной тенденцией к его повышению: если в 1920-е гг. носительство на слизистой ротовой полости составляло10%, то в 1960–1970-е гг. возросло до 46–52% [13]. Во многих исследованиях показано, что любые нарушения резистентности организма или изменения нормального микробного ценоза кишечника могут приводить к развитию заболевания – кандидоза [14]. Кожные покровы и слизистые оболочки являются «открытыми системами» макроорганизма, непрерывно контактирующими с окружающей средой. В свою очередь Candida spp. широко распространены в природе, часто контаминируют почву, воду, продукты питания, бытовые поверхности. Частый контакт человека с Candida spp. объясняет значительную распространенность транзиторного кандидоносительства в популяции людей. По статистическим данным, среди населения стран Европы кандиды выделяются в кале у 65–80%. Как условно-патогенный представитель микрофлоры человека грибы не представляют серьезную угрозу здоровью иммуннокомпетентного человека [15]. В то же время на фоне увеличения числа пациентов с нарушениями в системах антимикробной резистентности наблюдается значительный рост заболеваемости кандидозом [16]. Многие исследователи связывают рост кандидозов с факторами риска, к которым относят детский и старческий возраст, терапию глюкокортикостероидами и антибактериальными препаратами, интенсивную цитостатическую полихимиотерапию, сахарный диабет и другие заболевания эндокринной системы, СПИД, тяжелые истощающие заболевания, нарушение трофологического статуса, генетически детерминированные иммунодефициты [17–19]. Первичное инфицирование организма человека кандидами происходит при прохождении через родовые пути матери, о чем свидетельствуют высокая частота выделения Candida у новорожденных (до 58%) и почти полное совпадение видового состава Candida у ребенка и матери. Инфицированию способствует увеличенная частота носительства и кандидоза влагалища в последней трети беременности. Имеются сведения о передаче грибов рода Candida при кормлении грудью [20]. Грибы, паразитирующие на коже человека, питаются частицами эпидермиса, роговыми массами ногтевых пластинок, а продукты их жизни – белки вызывают аллергическую реакцию. Фактором патогенности грибов рода Candida является их способность к адгезии и инвазии с последующим цитолизом ткани, а затем и к лимфогематогенной диссеминации [21]. Candida spp. способны к инвазивному процессу в слизистых оболочках, в первую очередь представленных многослойным плоским эпителием, реже – однослойным цилиндрическим. Чаще всего инвазивный микотический процесс наблюдается в полости рта, пищеводе, желудке и кишечнике. Доказано, что даже без внедрения вглубь эпителия Candida spp. [22] могут вызывать патологию – неинвазивную форму кандидоза. Контакт поверхностных и корпускулярных антигенов гриба с имммунокомпетентными клетками макроорганизма может привести к выработке повышенных количеств специфических IgE и сенсибилизированных лимфоцитов, что служит патогенетической основой для микогенной сенсибилизации. Аллергенами у Candida albicans являются и первичные метаболиты – алкогольдегидрогеназа и кислый P2-протеин. Это потенциально опасно в плане развития микогенных аллергических заболеваний: специфической бронхиальной астмы, атопического дерматита, крапивницы. Резорбция в кишечнике продуктов метаболизма грибов рода Candida – его плазмокоагулаза, протеазы, липофосфорилазы, гемолизин и эндотоксины могут вызвать специфическую интоксикацию и вторичный иммунодефицит [23]. За счет взаимодействия с представителями облигатной нормобиоты и условно-патогенными микроорганизмами Candida spp. могут индуцировать дисбиоз и микст-инфекцию слизистых оболочек. Ключевым фактором начала инфекционного кандидозного процесса является нарушение неспецифической и специфической резистентности организма как на местном, так и на общем уровне [23]. К факторам неспецифической резистентности традиционно относят адекватный баланс десквамации и регенерации эпителиоцитов, мукополисахариды слизи, нормальную микробиоту слизистых оболочек (Bifidobacterium spp., Lactobacillus spp., Escherichia coli, Peptostreptococcus spp.), перистальтическую активность и кислотно-ферментативный барьер пищеварительного тракта. Показано, например, что лечение больных препаратами, содержащими бифидобактерии, значительно снижает содержание грибов рода Candida в кале больных [24]. К неспецифическим факторам относят также секреторный IgA, лизоцим, трансферрин, компоненты комплемента. Однако наиболее важны число и функция полиморфноядерных мононуклеарных фагоцитов, в частности их способность к хемотаксису, аттракции, килингу и презентированию грибкового антигена. Именно в условиях нейтропении развиваются жизнеугрожающие формы кандидоза, включая висцеральные поражения (печени, желчного пузыря, поджелудочной железы) [11]. Специфический иммунный ответ при кандидозе представлен наработкой специфических противокандидозных антител классов IgA, IgG, IgM, инактивирующих ферменты инвазии и эндотоксины гриба, а также вместе с компонентами комплемента участвующих в опсонизации [25, 26]. Конфликт между факторами патогенности гриба и факторами антифунгальной резистентности приводит к развитию той или иной формы кандидоза. Механизмы патогенеза 2-х принципиально различных форм кандидоза (инвазивного и неинвазивного) легли в основу классификации кандидоза кишечника.
Клинические формы
Для практических целей необходимо выделять 3 формы поражения: – инвазивный диффузный; – фокальный (вторичный при язве двенадцатиперстной кишки, неспецифическом язвенном колите); – неинвазивный (так называемый кандидозный дисбиоз) [27]. Довольно часто кандидоз органов пищеварения протекает в виде микст-инфекции: Candida-бактериальной, Candida-герпетической, Candida-протозойной, что делает клиническую картину заболевания довольно вариабельной. Частота микст-инфекции при дисбиозе кишечника с повышенной пролиферацией грибов рода Candida, по некоторым данным, составляет 63%. При этом чаще обнаруживают ассоциацию со значительным количеством бактерий с так называемым протеолитическим основным путем метаболизма (условно-патогенными): Escherichia coli, Ristella, Clostridium perfringens, Klebsiella, Morganella, Bacteroides, Staphylococcus aureus, Pseudomonas aeruginosa [28]. Среди всех локализаций кандидоза пищеварительного тракта
орофарингеальная локализация
занимает 1-е место [29]. Кандидозный стоматит у новорожденных — распространенное заболевание. В первые дни после рождения слизистые ребенка устойчивы к грибам. В дальнейшем недостаточная секреция IgA и постепенное снижение антимикробного иммунитета, переданного от матери, приводят к высокой заболеваемости [30, 31]. Оральный (орофарингеальный) кандидоз – широко распространенный микоз у лиц, страдающих различными формами иммунодефицитов, прежде всего СПИДом и гемобластозами, причем гастроинтестинальная локализация кандидоза у больных СПИДом может быть источником кандидемии, которая у таких больных при других локализациях кандидоза встречается всего в 1% случаев [32, 33]. Частым микозом пищеварительного тракта является
кандидоз пищевода,
который регистрируют как у иммунокомпетентных, так и (гораздо чаще) у иммунокомпрометированных лиц [34]. Кандидозный эзофагит в стационарах общего профиля встречается у 1,3–2,8% больных, в отделениях трансплантации — у 4%, при диссеминированном карциноматозе — у 2,8–6,7%. Это заболевание протекает часто без субъективных жалоб и выявляется случайно при «сплошных» исследованиях населения в 1–7% случаев. Иногда больные отмечают боль и дискомфорт при прохождении твердой и жидкой пищи, дисфагию, гиперсаливацию. По глубине поражения эндоскопически выделяют 4 типа — от легкого отека, гиперемии, единичных белых налетов < 1 мм в диаметре до массивного воспаления, деформации и кровоточивости слизистой, изъязвлений, вплоть до перфорации. Сравнительной оценкой различных методов диагностики кандидоза пищевода показано, что в 95% случаев кандидоз был выявлен при анализе соскобов и только в 39% – при анализе материала биопсий [35].
Микозы желудка,
в т. ч. и кандидоз, при отсутствии какой-либо другой патологии соматической или бактериальной этиологии отмечают редко [36–38]. Их доля среди всех случаев кандидоза верхнего отдела пищеварительного тракта составляет лишь 5,2%. Гораздо чаще (до 17–30%) Candida spp. находят в биоптатах гастродуоденальных язв, а также при хронических гастритах [39]. Однако лишь находки псевдомицелиальных структур гриба, а не отдельных непочкующихся клеток, при морфологическом исследовании окрашенных по Романовскому – Гимзе или PAS-методом цитологических и/или гистологических препаратов, достоверно подтверждают диагноз кандидоза желудка. В последние годы Candida spp. часто выделяют в ассоциации с Helicobacter pylori, причем стандартная противохеликобактерная терапия способствует увеличению частоты кандидоза желудка [40]. Подавляющее большинство Candida spp., выделенных от больных (65,6%), обладали высокой или умеренной вирулентностью. При выделении из желудочного сока больных гастродуоденальными заболеваниями ассоциации Candida spp. и Helicobacter pylori можно предполагать более тяжелое течение заболевания, а планируемую антибактериальную терапию необходимо проводить совместно с антифунгальной [39].
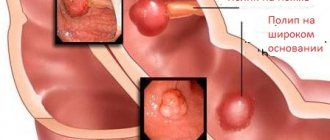
Кандидоз кишечника
как изолированная форма заболевания бывает нечасто. Обычно он является продолжением кандидоза желудка и верхнего отдела пищеварительного тракта. Кандидоз кишечника нередко сопровождается диареей. Различают диареи различной этиологии [40] с сопутствующим выделением Candida и кандидозные диареи (КД), при которых Candida является единственным выделяемым возбудителем. Основным предрасполагающим фактором риска КД, особенно у госпитализированных больных, является антибиотикотерапия. Другие факторы риска: эндокринные нарушения, иммунные дисфункции, неоплазмы, стероидная терапия; играет роль и пожилой возраст больных [41]. У больных КД чаще выделяют С. albicans, далее – C. krusei, C. tropicalis, C. kefyr, C. stellatoidea, C. guilliermondii, C. parapsilosis, C. lusitaniae [41]. В тех случаях, когда Candida является компонентом нормальной биоты кишечника, его рост и размножение подавляются микроорганизмами кишечника, где гриб присутствует в стабильном количестве и не размножается [35]. При подавлении бактериобиоты антибиотиками отмечается размножение дрожжей с образованием у них ростовых трубок и появлением мицелиальных структур. По данным Т.В. Толкачевой с соавт. [13], частота выделения дрожжевых грибов из кишечника иммунокомпрометированных больных сохраняется высокой, достигая в последние 2 года 63–65%. Соотношение частоты выявления штаммов C. albicans и non-albicans составляет 52,5%. Среди последних доминируют C. krusei (40%), C. glabrata (28%) и C. kefyr (15,6%) [42]. Отмечено увеличение частоты встречаемости ассоциации из 2-х видов Candida non-albicans и расширение видового спектра дрожжевых грибов, колонизирующих кишечник больных гемобластозами. Кандидоз толстого кишечника – редкое заболевание, чаще он регистрируется в ассоциации с другими кишечными патогенами бактериальной природы [43]. В последние годы выдвинута гипотеза о том, что хронический кишечный кандидоз является, возможно, этиологическим фактором формирования синдрома хронической усталости [44]. Признаки микогенной сенсибилизации выявляют у 10,4% больных с дисбиозом кишечника с избыточным ростом грибов рода Candida. Диагноз устанавливают при наличии следующих критериев, таких как: флатуленция, абдоминальный дискомфорт, изменения консистенции и частоты стула, признаки умеренной интоксикации и тенденция к обострению аллергических заболеваний.
Грибковому поражению билиарной системы
способствуют предшествующие дискинезия желчевыводящих путей, диспанкреатизм, лямблиоз, холестаз, гипотония желчного пузыря и другие поражения. При этих состояниях создаются благоприятные условия для размножения грибов и других микроорганизмов. Причиной кандидозного холецистита могут быть камни в желчных протоках, которые часто являются «резервуаром» для грибов, некоторые авторы даже называют их «грибковыми тельцами» или «кандидозными камнями». Микозы желчевыводящих путей встречаются чаще, чем принято считать.
Диагностика
Диагностика кандидоза с помощью чисто клинических методов невозможна ввиду того, что его клинические проявления не имеют абсолютной специфичности. В подавляющем большинстве случаев современная клинико-лабораторная инструментальная база позволяет провести высококачественное обследование и помочь клиницисту в постановке диагноза, а также назначить эффективное лечение инфекций, вызванных грибами. В последние годы за счет эндоскопических технологий расширились возможности диагностики грибкового эзофагита и гастрита. При эзофагогастродуоденоскопии обращают внимание на гиперемию и изъязвления слизистой, наличие белых налетов и пленок, сужение просвета пищевода, скопление слизи [45]. Во время этой процедуры в обязательном порядке следует брать материал для микробиологического исследования, т. к. не всегда этиология этих проявлений – грибковая. Причем информативность исследования налетов выше, чем биоптатов (95% по сравнению с 39%). Особенно перспективны видеоинформационные эндоскопические исследования с цифровой регистрацией и анализом изображения. Четкое разграничение неизмененных и патологических тканей, анализ гистохимических процессов в слизистой оболочке пищеварительного тракта возможны с помощью эндоскопической спектроскопии и флюоресцентной эндоскопии [46]. Видео- и колоноскопия, хромоэндоскопия на фоне «лекарственного» сна по технологии «Диантек» отличаются высоким качеством исследования, безболезненностью манипуляций и отсутствием стресса и страха у пациентов [8]. Следует, однако, подчеркнуть, что инвазивные манипуляции при воспаленной слизистой ЖКТ небезопасны, могут способствовать грибковой и бактериальной диссеминации, а иногда приводят к травме и перфорации стенки пищевода или желудка. Эндоскопическая ультрасонография с допплеровским картированием, контрастным усилением тканевых и сосудистых структур перспективна, она позволяет детально дифференцировать все слои стенки пищеварительного тракта. Неинвазивные методы — виртуальная эндоскопия, позволяющая получить 3-мерное изображение, магнитно-резонансное исследование — имеют большое будущее [47]. Изучение гастродуоденальной моторики с помощью сцинтиграфии и электрогастрографии также важно для диагностики и назначения дополнительных лекарственных средств, т. к. нарушение двигательной функции желудка, «застой» в ЖКТ создают условия для размножения грибов и бактерий. Колоноскопия дает возможность оценить состояние слизистой кишечника, наличие белого налета, язвенных дефектов и т. д. В перспективе в гастроэнтерологии будут внедряться методы, в основе которых лежат новые научно-практические исследования: иммуноферментный анализ фекальных антигенов, ПЦР и даже генетическое тестирование [5, 47]. Лабораторное подтверждение грибкового заболевания ЖКТ возможно при микроскопировании и/или культуральном исследовании смывов со слизистых оболочек полости рта и пищевода, содержимого желудка и кишечника, патологических пленок, налетов и др. Количественная оценка грибов в биосубстратах должна проводиться в сопоставлении с клинической симптоматикой, с учетом наличия фоновых заболеваний, микст-инфекции и т. д. [48]. Например, обнаружение на слизистых единичных колоний Candida не является основанием для постановки диагноза «кандидоз» у иммунокомпетентных пациентов. В кале диагностическую значимость приобретает количество колоний (более 105–106). По-другому, с более низким диагностическим порогом, интерпретируются результаты посевов у иммуносупрессированных лиц, при нейтропении у больных СПИДом и в отделениях интенсивной терапии [49, 50]. Следует также обращать внимание на способность грибов к вегетации и образованию мицелия, т. к. это является одним из лабораторных признаков, подтверждающих диагноз кандидоза. Гистологическое (окраска по Гомори–Гроккоту, ШИК-реакция) и цитологическое (окраска по Романовскому – Гимзе) исследования биоптатов позволяют обнаружить тканевые формы грибов. Многими авторами эти методы рассматриваются как наиболее достоверные. Кроме того, мицелий и псевдомицелий в тканях служат подтверждением наличия инвазивной формы грибковой инфекции ЖКТ [51]. Микробиологическое исследование порций желчи, полученных при многофракционном дуоденальном зондировании, позволяет дифференцировать грибковую от бактериальной или функциональной патологии двенадцатиперстной кишки, желчного пузыря, желчевыводящих путей и печени.
Заключение
Таким образом, на сегодняшний день кандидоз является наиболее часто встречающимся типом грибковой инфекции. Люди с ослабленным иммунитетом должны воспринимать любые проявления кандидоза серьезно и обращаться к врачу при первых признаках заболевания для проведения терапии.
Аналоги
Совпадения по коду АТХ 4-го уровня: Верона
Фибс
Гастрикумель
Тиреоидеа Композитум
Берлитион
Тиолепта
Желудочный сбор
Эспа-Липон
Пивные дрожжи
Липоевая кислота
Шиповника сироп
Октолипен
Тиоктацид
Тиогамма
Фигурин
Аналоги Фитогастрола:
- Актовегин;
- Алоэ сок;
- Алоэ Экстракт.
Цена Фитогастрола, где купить
Фитогастрол можно купить по цене около 75 рублей в российских аптеках или за 25 гривен в аптеках Украины.
- Интернет-аптеки РоссииРоссия
- Интернет-аптеки УкраиныУкраина
ЗдравСити
- Фитогастрол (Желудочно-кишечный сбор) ФармаЦвет 2г фильтр-пак. 20 шт.АО Красногорсклексредства
106 руб.заказать
Аптека Диалог
- Фитогастрол сбор (Желудочно-кишечный) (ф/п 2г №20)Красногорсклексредства
90 руб.заказать
- Фитогастрол сбор (Желудочно-кишечный) (50г)Красногорсклексредства
75 руб.заказать
показать еще
Аптека24
- Фитогастрол сбор 1.5 г в пакетиках №20 ПрАТ»Ліктрави»,м. Житомир,Україна
33 грн.заказать
Лекарственные сборы — смеси нескольких видов измельченного, реже – цельного, растительного сырья. В состав сборов входят различные части растений: корни, кора, трава, листья, цветки, плоды, семена. Многокомпонентные лекарственные растительные сборы давно используются в медицинской практике, что объясняется эффективностью и мягкостью их действия, отсутствием, как правило, нежелательных побочных явлений при длительном применении, а также удобством приготовления. В России имеются достаточная сырьевая база по многим видам лекарственных растений, опыт их производства и клинического применения. Лекарственные растительные сборы являются наиболее популярной и широко используемой формой переработки лекарственного растительного сырья.
Композиции из лекарственного растительного сырья, иногда с добавлением минеральных веществ, с глубокой древности применялись в медицине всего мира. Особенно популярны сборы в восточной медицине: китайской, тибетской и др. Прописи этих сборов отличаются сложностью состава, большим числом компонентов, относящихся к различным морфологическим группам сырья. В народной медицине России сборы применялись менее широко, т. к. предпочтение отдавалось индивидуальным лекарственным растениям.
Многокомпонентные смеси из лекарственного растительного сырья обладают ценными преимуществами перед другими фитопрепаратами: возможность обеспечить основной фармакологический эффект в сочетании с комплексным воздействием на организм больного в целом, мягкость действия и отсутствие, как правило, нежелательных побочных явлений. Они достаточно просты в промышленном производстве и относительно дешевы.
Лечение многокомпонентными лекарственными растительными сборами обычно более эффективно, чем одиночными растениями. При составлении сбора необходимо учитывать индивидуальные особенности больного и наличие сопутствующих заболеваний. При выборе сбора нужно знать показатели артериального давления и учитывать основную тенденцию его изменения. Например, при выборе сбора для больного холециститом с артериальной гипертензией необходимо, чтобы в сбор входили растения не только с желчегонным, но и с гипотензивным действием, иначе лечение может спровоцировать гипертонический криз, ухудшить общее состояние. Кроме того, следует учитывать склонность к запорам либо поносам; соответственно, эффект должен быть слабительного или вяжущего характера. Действие лекарственного растительного сырья во многом зависит от доз. Корень ревеня, например, в больших дозах применяется как слабительное средство, а в малых, наоборот, оказывает закрепляющее действие. Различные дозы пряно-горького сырья стимулируют или угнетают выделение желудочного сока. Некоторые растения действуют на мускулатуру матки и могут быть опасными при беременности. Растительные сборы и средства не рекомендуется принимать во время менструаций. Лекарственное растительное сырье обладает разносторонним действием. Этим объясняется тот факт, что в прописях, разных по назначению, часто встречаются одинаковые компоненты, но в разных количествах и различных сочетаниях. Предусмотреть нежелательное побочное действие лекарственных растений может только врач после всестороннего обследования больного.
В зависимости от входящих в состав сбора видов сырья на его основе готовят настои или отвары. Если в состав сбора входят пахучие эфирномасличные растения, то из них, как правило, готовят настой. Кипячение при этом не допускается, т. к. эфирные масла являются летучими веществами, испаряющимися вместе с водой. Лекарственные сборы содержат различные биологически активные соединения, которые одновременно с лечением основного заболевания дополнительно обогащают организм различными витаминами, минеральными соединениями и другими компонентами растений, способствующими повышению сопротивляемости организма, благотворно влияющими на центральную нервную систему, улучшающими процессы кроветворения, нейтрализующими шлаки и ускоряющими выведение их из организма. Воздействие на физиологические процессы осуществляется в этом случае природными, более приемлемыми для организма органическими веществами. Аллергические осложнения при лечении лекарственными растительными сборами наблюдаются гораздо реже, чем при применении других медикаментов (например, химического происхождения). Разностороннее воздействие биологически активных веществ растений часто достигает цели. Так, при назначении сложного сбора при заболеваниях печени вещества бессмертника усиливают секрецию желчи, желудочного и панкреатического сока, повышают тонус желчного пузыря, изменяют химический состав желчи. Вещества, содержащиеся в кукурузных рыльцах, благотворно влияют на обмен веществ, улучшают желчеотделение. Вещества барбариса уменьшают и снимают боли, что связано с присутствием алкалоида берберина, обладающего спазмолитическим действием. С той же целью часто в такой сбор вводят и лист мяты перечной.
Кроме органических веществ сборы содержат макро- и микроэлементы, которые участвуют в обмене веществ, находятся в функциональном взаимодействии с ферментами, витаминами, гормонами и другими биологически активными веществами. Марганец, медь, цинк, кобальт в микродозах стимулируют выработку антител, повышают сопротивляемость организма. Медь, железо, цинк, кобальт уменьшают проницаемость биологических мембран. При лечении больного многокомпонентными лекарственными сборами в организм вводятся белки, аминокислоты, углеводы, липиды, ферменты, витамины, органические кислоты, спирты, альдегиды и кетоны, сложные эфиры фосфорной кислоты и других кислот, фитостерины, смолистые и дубильные вещества, гликозиды, терпеноиды, кумарины, амиды и амины, бетаины, холин и холиновые сложные эфиры, пурины и пиримидины, алкалоиды, горькие вещества и многие другие.
Наиболее популярны следующие лекарственные растительные сборы: антимикробный, желудочно-кишечный, урологический, грудной, успокоительный, желчегонный, противосклеротический, спазмолитический, ветрогонный, мочегонный, противоастматический.
Заболевания желудочно-кишечного тракта довольно широко распространены, на их долю приходится 35–37 % общей заболеваемости населения. Наиболее распространенными среди них являются гастриты, язвенная болезнь, энтероколиты. Терапия воспалительных и деструктивных заболеваний желудочно-кишечного тракта направлена на коррекцию нарушений желудочной секреции, моторной функции желудка и кишечника, кишечного пищеварения, а также предусматривает воздействие на измененную слизистую оболочку желудка и кишечника. Применение синтетических лекарственных препаратов не всегда оказывает должное воздействие при указанной патологии; кроме того, возможно развитие побочных реакций и осложнений. В таких случаях, а также для профилактики обострений хронических заболеваний желудочно-кишечного тракта весьма перспективны растительные сборы. Желудочно-кишечный сбор – это комбинированный препарат растительного происхождения, содержащий пять видов растительного лекарственного сырья. Настой сбора обладает спазмолитическим, противовоспалительным, желчегонным седативным, регенерирующим действием. Эффект обусловливают содержащиеся в цветках ромашки эфирное масло, полисахариды, флавоноиды; эфирное масло из листьев мяты, основными компонентами которого является ментол, флавоноиды, витамины; эфирное масло из плодов укропа.
Воспалительные заболевания бронхов в настоящее время широко распространены и являются одной из наиболее частых причин потери работоспособности. Антибиотикотерапия, применяемая для их лечения, нередко приводит к развитию аллергии, формированию резистентности микроорганизмов с потерей чувствительности к антибиотикам при последующих курсах лечения, развитию дисбактериоза и росту числа грибковых заболеваний. Опыт клинического применения грудного сбора демонстрирует его эффективность и целесообразность использования при инфекционно-воспалительных процессах в бронхах в качестве вспомогательного или альтернативного лекарственного средства, свободного от нежелательных побочных явлений. Лечебный эффект сбора обусловлен антибактериальным эффектом цветков ромашки, побегов багульника, цветков календулы, отхаркивающим и обволакивающим действием корней солодки, травы фиалки и побегов багульника, противовоспалительными и спазмолитическими эффектами корней солодки, цветков ромашки, календулы и листьев мяты.
В последнее время наблюдается значительный рост распространенности состояний, вызванных повышенной физической или умственной нагрузкой, воздействием неблагоприятных факторов окружающей среды, растущими информационными нагрузками, стрессами. В таких условиях развивается хроническое переутомление, которое приводит к развитию бессонницы, повышенной нервной возбудимости, раздражительности, неврастении, сердечно-сосудистых неврозов, тахикардии, истерии, мигрени, вегетососудистой дистонии, климактерических расстройств, артериальной гипертензии. Лекарственных растений, обладающих успокоительным действием, достаточно много. Седативное, спазмолитическое, гипотензивное действие успокоительного сбора обусловлено входящими в него лекарственными травами. Эффект определяют содержащиеся в траве пустырника эфирные масла, сапонины, дубильные вещества, алкалоиды; в листьях мяты перечной – ментол; в корневищах с корнями валерианы – сложный эфир борнеола и изовалериановой кислоты, свободная валериановая и другие органические кислоты, алкалоиды (валерин и хатинин), дубильные вещества, сахара; в корнях солодки – ликуразид, тритерпены, глицирризиновая кислота и флавоноиды; в траве чабреца – эфирное масло, дубильные и горькие вещества; в траве душицы – тимол, флавоноиды, дубильные вещества; в шишках хмеля – эфирное масло, органические кислоты, алкалоиды, флавоноиды, лупулин; в траве донника – кумарины, мелилотозид, полисахариды.
Приготовление из сборов лекарственных растений настоев и отваров принципиально не отличается от получения этих препаратов из сырья отдельных лекарственных растений. В конкретных указаниях по приготовлению из сборов настоев и отваров обычно приводится такое соотношение: 1–2 столовая ложка смеси на 200 мл воды.
Во всех случаях для полного извлечения действующих веществ воды берут гораздо больше, чем при приготовлении аналогичных лекарств в условиях аптеки. Поэтому принимают изготовленное лекарство чаще всего не ложками, а по 1/3–1/2 стакана. Если настой или отвар готовят ежедневно, он не подвергается микробной контаминации и может храниться при комнатной температуре в течение дня. При большем количестве его следует хранить в холодильнике, но не более двух суток.
Обычно при лечении лекарственными растениями улучшение наступает через несколько дней, но стойкого эффекта удается достичь лишь при длительном и регулярном применении лекарственных трав. Отсутствие положительного эффекта в течение 2–3 недель, как правило, является основанием для замены сбора. Курс лечения сборами должен определять лечащий врач при постоянном наблюдении за здоровьем больного.
При лечении хронических больных сборами растений их принимают длительное время. Во избежание привыкания к ним и снижения эффективности лечебного воздействия рекомендуют после каждого курса лечения (1,0–1,5 месяца) делать перерыв на 1–2 недели. По тем же соображениям желательно после 2–3 курсов лечения одним из сборов перейти на лечение другим, обладающим аналогичным действием.
Информация об авторах: Самылина Ирина Александровна – доктор фармацевтических наук, профессор, член-корреспондент РАМН, директор НИИ фармации; заведующая кафедрой фармакогнозии ММА им. И.М. Сеченова. Тел.; Сорокина Алла Анатольевна – доктор фармацевтических наук, профессор кафедры фармакогнозии ММА им. И.М. Сеченова. Тел.; Пятигорская Наталья Валерьевна – кандидат фармацевтических наук, доцент, заместитель директора НИИ фармации по научной работе. Тел.