Основной целью УЗИ аорты брюшной полости является выявление аневризмы или атеросклеротического поражения аорты и поражения её крупных ветвей: селезёночной, печёночной, почечных и брыжеечных артерий. УЗИ брюшной аорты является неинвазивным методом диагностики, имеющим высокую ценность для выявления многих сосудистых заболеваний. Результаты УЗИ очень зависят от технологии обследования, качества аппаратуры и квалификации специалиста. На сегодняшний день низкая цена на УЗИ аорты и органов брюшной полости, простота и безопасность исследования делают его незаменимым для первичного выявления аневризмы брюшной аорты.
Инновационный сосудистый центр специализируется на сосудистой хирургии, поэтому мы стремимся проводить диагностику сосудистой патологии на самом высоком уровне. В нашем центре есть отличные стационарные и мобильные УЗИ-аппараты, позволяющие детально изучать структуру стенки аорты и её ветвей, а также выявлять аневризмы. Специалисты нашего медицинского центра настроены на работу именно с сосудистой патологией, поэтому выявляют её значительно лучше, чем врачи УЗИ общего профиля.
Подготовка к исследованию
Для успешного проведения УЗИ брюшной полости необходима подготовка, направленная на снижение количества газов в кишечнике, которые мешают увидеть забрюшинные органы, в том числе аорту. Правила подготовки для осмотра брюшной аорты и её ветвей на УЗИ несложные:
- За 2 дня до обследования исключить из рациона бобовые, картофель, капусту, дыню, молочные продукты питания, газировку и все блюда с высоким содержанием углеводов. Эти продукты могут вызывать повышенное газообразование.
- Накануне УЗИ начинайте принимать лекарства, способствующие улучшению работы кишечника. Для этих целей подходит приём эспумизана или обычного активированного угля.
- Вечером накануне процедуры желательно пропустить ужин, а утром – завтрак.
Аневризмы брюшной и грудной аорты
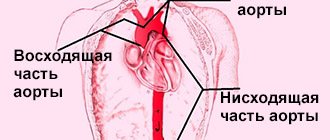
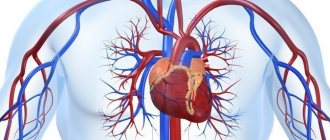
Аорта является самой большой артерией человеческого организма, по которой кровь, насыщенная кислородом, течет от левого желудочка. От нее отходят ветви к различным внутренним органам и тканям, а на уровне таза она делится на две подвздошных артерии, которые кровоснабжают нижние конечности. Аорту можно подразделить на грудной и брюшной отделы, находящиеся в соответствующих полостях. Иногда под действием различных факторов стенка этого сосуда истончается, и за счет давления крови образуется выпячивание (аневризма). Так как при этом могут развиться различные осложнения, пациентам необходимо оказать медицинскую помощь.
Этиология
Аневризма брюшной аорты в большинстве случаев протекает на фоне атеросклеротического поражения ее стенки, которое наблюдается более чем в 80% случаев. Гораздо реже причиной истончения мышечного слоя являются воспалительные заболевания (туберкулез, ревматизм, сифилис), сопровождающиеся поражением сосудов. Неспецифический аортоартериит возникает на фоне других инфекционных заболеваний.
Врожденная патология строения соединительной ткани (фиброзно-мышечная дисплазия, синдром Марфана) также играет большую роль в развитии этого патологического процесса.
В связи с развитием сосудистой хирургии в последние десятилетия все чаще причиной аневризмы являются операции на брюшном отделе аорты:
- ангиопластика, когда при помощи специального баллона увеличивают диаметр артерии;
- удаление тромбов и атеросклеротических бляшек вместе с внутренней оболочкой (эндартерэктомия);
- истончение стенки в месте соединения при аорто-бедренном протезировании.
Однако в большинстве случаев осложнений хирургического вмешательства образуется ложная аневризма, стенки которой выполнены не сосудом, а окружающими тканями. Факторами риска формирования аневризмы брюшной полости являются курение, ожирение, мужской пол, отягощенная наследственность (наличие подобных заболеваний у ближайших родственников) и гипертоническая болезнь.
Проявления и осложнения
Симптомы аневризмы довольно длительное время могут отсутствовать и появляются лишь при значительном увеличении ее в размере, либо при развитии различных осложнений.
В первом случае пациенты жалуются на ощущение пульсации в животе, выбухание передней брюшной стенки в горизонтальном положении. Особенно это характерно для худощавых людей. Болевой синдром при этом обычно принимается за почечную или печеночную колику. Помимо этого могут наблюдаться дисфункции внутренних органов вызванных внешним сдавлением:
- расслоении аневризмы. При расслоении аневризмы происходит образование ложного хода, кровоток по которому отсутствует;
- нарушаются процессы пищеварения (изжога, ухудшение перистальтики, запор);
- со стороны выделительной системы нередко развиваются гематурия, задержка мочи;
- при воздействии на сосуды, идущие к яичкам, может развиваться варикоцеле или ишемия;
- при сдавлении нервных корешков и сплетений появляются симптомы ишиаза и радикулита, характеризующихся болью в пояснице и нижних конечностях.
Одним из наиболее частых осложнений является расслоение стенки аорты с образованием второго просвета, который обычно слепой, то есть в нем отсутствует полноценный кровоток. Как правило, это является продолжением дефекта, возникшего на уровне грудного отдела.
Расслаивающая аневризма характеризуется следующими признаками:
- Ухудшение кровотока различных внутренних органов. При этом нарушается их функция, так, при поражении мезентериальных артерий развивается некроз кишки, почечных – острая почечная недостаточность. Если нарушено кровоснабжение нижних конечностей, возникает перемежающаяся хромота.
- Боль обычно довольно интенсивная и связана с воздействием на чувствительные нервные рецепторы, находящиеся в стенке сосуда, и в органах, подвергшихся ишемии. Она локализуется в области передней брюшной стенки, но может отдавать и в спину.
- Могут появляться неврологические нарушения в виде парезов и параличей, а также периферической полинейропатии.
Разрыв аневризмы брюшной аорты сопровождается внезапным снижением повышенного артериального давления, потливостью, болью в животе и поясничной области, появляются признаки двигательного возбуждения и слабость. Если не предпринять экстренных мер, то пациент погибает в течение короткого времени от массивного кровоизлияния в брюшную полость.
Аневризмы грудной аорты развиваются обычно вследствие дегенеративных изменений ее стенки и относятся чаще к истинным аневризмам. По этиологии аневризмы делятся на: 1) невоспалительные (атеросклеротические, травматические, послеоперационные, ятрогенные); 2) воспалительные (сифилитические, ревматические, при неспецифическом аортоартериите, микотические); 3) врожденные (при синдроме Марфана, кистозном медионекрозе, коарктации аорты, врожденной извитости дуги аорты). По локализации различают: 1) аневризмы синусов Вальсальвы; 2) аневризмы синусов Вальсальвы и восходящей аорты; 3) аневризмы восходящей аорты; 4) аневризмы восходящей аорты и дуги аорты; 5) аневризмы дуги аорты; 6) аневризмы дуги аорты и нисходящей аорты; 7) аневризмы нисходящей аорты;  торакоабдоминальные аневризмы. По виду аневризмы делят на истинные, ложные и расслаивающие, а по форме — на мешковидные и диффузные (веретенообразные).
торакоабдоминальные аневризмы. По виду аневризмы делят на истинные, ложные и расслаивающие, а по форме — на мешковидные и диффузные (веретенообразные).
Аневризмы грудной аорты наблюдаются преимущественно у мужчин. Клиническая картина скудная. Иногда аневризма является случайной находкой. Симптоматика зависит от локализации, величины и протяженности аневризмы. Ведущий симптом у 1/3 больных -боль за грудиной, в шее, спине, между лопатками. У другой 1/3 больных ведущий симптом — одышка, стридор, сухой кашель. Почти у половины больных отмечается артериальная гипертензия. Иногда наблюдается осиплость голоса, брадикардия, симптом Горнера, ишемические нарушения со стороны головного мозга. Сосудистые шумы выявляются у 75% больных.
Диагностика аневризм на догоспитальном этапе затруднена. 40-50% больных госпитализируются с ошибочным диагнозом. Точный топический диагноз дает рентгенологический метод, при котором выявляется расширение тени средостения, кальциноз стенки аневризмы, отклонение пищевода при контрастировании его барием. Наиболее ценными методами исследования являются компьютерная и магнитно-резонансная томография, с помощью которых выявляются локализация и размеры аневризмы. Аортография подтверждает диагноз. Дифференциальный диагноз проводится с опухолями и кистами средостения.
Прогноз при нелеченых аневризмах неблагоприятный. В течение трех лет после установления диагноза умирает 37,7%, через 5 лет — 54% больных. Причины смерти: разрыв аневризмы (35-40%), сердечная недостаточность (20-36%), сдавление трахеобронхиального дерева, пневмония (14-20%).
Как проходит УЗИ брюшной аорты и её ветвей
Принцип ультразвукового сканирования брюшной полости заключается в обработке отражённого от органов ультразвукового сигнала. Это позволяет оценить структуру и размеры данного органа. Ультразвуковое обследование аорты брюшной полости не является опасным и не приносит никаких неприятных ощущений. Сам процесс диагностики включает всего несколько этапов:
- В кабинете УЗИ диагностики пациент располагается на кушетке справа от врача и открывает живот.
- Доктор смазывает специальный датчик и живот пациента прозрачным гелем, который снижает сопротивляемость тканей и помогает ультразвуковой волне проникать внутрь.
- Затем специалист медленно передвигает датчик по брюшной стенке и записывает результаты наблюдений.
Возможности ультразвуковых приборов позволяют не только оценить размеры, форму и структуру стенки сосуда, но и исследовать характеристики кровотока. Это достигается с помощью доплерографии и цветного допплеровского картирования. Доплерография основана на регистрации ультразвукового сигнала от движущихся эритроцитов и изменении скорости этого сигнала в зависимости от приближения или удаления этих частиц к датчику. Скорость кровотока, определяемого доплерографией, является показателем проходимости сосудов ниже места исследования или в местах сужения сосуда. В суженых местах она значительно усилена; если же существует препятствие для оттока крови ниже места исследования, то скорость снижается.
Частота встречаемости гломусных опухолей (ГО) составляет менее 2% среди всех опухолей мягких тканей [1—3]. Как правило, ГО представляет единичное образование, реже сопровождается множественным поражением различных частей тела [3—6].
Описаны случаи и нетипичной локализации: в щитовидной железе [7], трахее [8], легких [9], костях [10], пищеводе [11], желудке [12], кишечнике [13], почке[14], на брюшине [15], интраневрально [16] и интравенозно [17].
Характерными симптомам ГО являются выраженный болевой синдром, повышение чувствительности к холоду и локальная болезненность при пальпации образования. При типичной локализации образования эти симптомы дают возможность поставить диагноз практически в 90% случаев. Из дополнительных методов исследования наибольшей чувствительностью обладает МРТ. Для большинства ГО характерно доброкачественное течение, однако описаны редкие примеры, характеризующиеся злокачественным потенциалом. Так, А. Folpe и соавт. [18] разработали критерии злокачественности: глубокое расположение опухоли, размер более 20 мм, присутствие атипичных митозов, сочетание умеренной и высокой степени ядерной и митотической активности, более пяти митозов на 50 полей зрения.
Лечение больных с интрадермальными ГО хирургическое. Радикальные операции приводят к полному излечению. Частота рецидивов, по данных разных авторов, составляет от 12 до 33% [18—26].
За 25 лет в нашей клинике это первый случай забрюшинной ГО.
Приводим клинический случай.
Пациентка Г
., 59 лет, при обследовании по месту жительства выявлена забрюшинная опухоль, в связи с чем в одной из клиник Москвы выполнено лапароскопическое удаление опухоли. Через 3 мес при контрольном обследовании выявлен рецидив опухоли, в связи с чем обратилась в РОНЦ им. Н.Н. Блохина. При иммуногистохимическом исследовании установлено, что образование имеет строение Г.О. При компьютерной томографии (КТ) грудной клетки и брюшной полости установлено, что у больной по сути продолженный рост опухоли. Новообразование расположено парааортально слева на уровне позвонков LII—LIV размерами 8×5×7 см. Опухоль инфильтрирует левый мочеточник, поясничную мышцу, брыжейку сигмовидной кишки, циркулярно охватывает аорту от левой почечной артерии до бифуркации, инфильтрирует поясничные артерии, тесно прилежит к нижней полой вене (рис. 1).
Рис. 1. Компьютерная томограмма брюшной полости.
25.11.15 больная оперирована. При ревизии отдаленных метастазов в брюшной полости не выявлено.
Первым этапом острым путем мобилизована правая и левая половина толстой кишки, визуализированы нижняя полая вена, аорта, мочеточники. Далее выполнена резекция сигмовидной кишки. Аорта выделена выше опухоли, визуализированы левые почечная артерия и вена. Последние перевязаны и пересечены. Затем выделены правая и левая подвздошные артерии, мобилизован инфраренальный сегмент аорты вместе с опухолью и перевязаны поясничные артерии (рис. 2).
Рис. 2. Этап выделения инфраренального отдела аорты, общие подвздошные артерии взяты на держалки. 1 — правая общая подвздошная артерия; 2 — левая общая подвздошная артерия; 3 — опухоль.
Опухоль единым блоком с аортой, левой почкой и сигмовидной кишкой удалена (рис. 3). Выполнено протезирование аорты и общих подвздошных артерий (рис. 4). Время ишемии нижних конечностей составило 20 мин. Время операции 3 ч. Кровопотеря 400 мл.
Рис. 3. Удаленный макропрепарат. 1 — опухоль; 2 — просвет инфраренального отдела аорты; 3 — левая почка; 4 — сигмовидная кишка.
Рис. 4. Вид операционного поля после сосудистой реконструкции.
При проведении иммуногистохимического исследования использовали антитела к виментину, aSMA, Н-кальдесмону, кальпонину, десмину, миогенину, СD10, CD31, CD34, D2−40, панцитокератину АЕ1/АЕ3, EMA, CD56, CD57, CD68, CD117, S100 протеину, GFAP, HMB45, Melan A, к рецепторам эстрогенов и прогестерона, Ki-67.
Выявлена экспрессия в большинстве опухолевых клеток: виментин (+++), Н-кальдесмон (+++) и кальпонин (+++), а в части опухолевых клеток отмечается экспрессия десмина, рецепторов эстрогенов (5%) и прогестерона (10%). Индекс пролиферации в опухолевых клетках Ki-67 составил 1% (рис. 5).
Рис. 5. Гистологические признаки злокачественной гломусной опухоли. Окраска гематоксилином и эозином. а, б — атипичные гломусные клетки окружают дилатированные кровеносные сосуды, ×100; в — опухоль состоит из круглых клеток с выраженным ядрышком, с высокой митотической активностью, ×400; г — опухоль прорастает стенку аорты, ×50.
Реакции на остальные иммуногистохимические маркеры в опухолевых клетках отрицательные [6—15].
Установлено, что образование представляет собой злокачественную ГО низкой степени дифференцировки FNCLCC (2/1/0 =3/8 баллов) с поражением стенки аорты, не доходя 0,2 см до ее интимы, парааортальной клетчатки и брыжейки ободочной кишки, подрастанием в стенку левого мочеточника, с метастазами в 2 из 6 лимфатических узлов и метастазом (размером 5×4×3 см) в брыжейке толстой кишки. В стенке толстой кишки, в левой почке, парааортальных лимфатических узлах, краях резекции аорты и большом сальнике элементы опухолевого роста не найдены.
При контрольном обследовании через 6 мес после операции признаков прогрессирования заболевания не выявлено.
Исходя из опубликованных данных, прогноз доброкачественных ГО удовлетворительный, при длительности наблюдения от 4 до 60 мес ни один больной доброкачественной ГО легкого не умер от прогрессирования заболевания [19].
Прогноз при злокачественной ГО, естественно, хуже, что обусловлено прогрессированием заболевания в различные сроки после операции. При Г.О. легкого чаще всего метастазы появляются в легких, при ГО желудка — в печени. По данным литературы, при лечении больных с ГО как в адъювантном, так и в лечебном режиме использовали следующие схемы химиотерапии: адриамицин/CDDP, доксорубицин [7, 27]. После проведения 4 курсов химиотерапии доксорубицином у больного со злокачественной ГО верхней доли правого легкого и множественными метастазами отмечен полный регресс опухоли. Больной прожил 15 мес после диагностирования системного прогрессирования и начала проведения химиотерапии [27]. Схему адриамицин/CDDP использовали в адъювантном режиме у больного со злокачественной ГО щитовидной железы, безрецидивный период при этом составил 30 мес [7].
Ниже приводим сводные данные по безрецидивной выживаемости и локализации метастазов у больных со злокачественными ГО нетипичной локализации (см. таблицу).
Безрецидивная выживаемость и локализация метастазов у больных со злокачественными ГО нетипичной локализации
Единственным методом лечения больных с местно-распространенной гломусной опухолью является радикальное хирургическое лечение.
Конфликт интересов отсутствует.
Интерпретация данных УЗИ брюшного отдела аорты
Во время УЗИ аорты и брюшных сосудов врач изучает размер аорты и её просвет, насколько равномерно она окрашивается при доплеровском картировании. Расширение брюшной аорты более 4 см говорит в пользу аневризмы. Ультразвуковая диагностика позволяет оценить состояние артерий почек, кишечника, печени и желудка. Можно выявить расширение артерий внутренних органов. При осложнённых аневризмах возможно выявление забрюшинной гематомы при разрыве, жидкости в брюшной полости, тромбоза аорты или висцеральных артерий. Часто на хорошем УЗИ-сканере удаётся выявить расслоение стенки сосуда, её надрывы и атеросклеротические бляшки. УЗИ брюшного отдела аорты и висцеральных ветвей длится около 25-40 минут. После обследования можно сразу возвращаться к обычным занятиям.
Аневризма аорты — симптомы и лечение
Лечение аневризм аорты направлено на предотвращение её разрыва. Оно бывает консервативным и хирургическим.
Консервативное лечение
Главное предназначение консервативной терапии — это снижение артериального давления и силы сокращения сердца, а также коррекция сопутствующих заболеваний, например ишемической болезни сердца, диабета, болезней почек и т. д. [1]
Хирургическое лечение
Современные хирургические методики лечения аневризм аорты делятся на эндоваскулярные и традиционные оперативные вмешательства.
Эндоваскулярный метод — дистанционная имплантация специальных трубчатых протезов (стент-графтов) в зону поражения аорты изнутри через катетер, установленный в бедренную артерию. Этот способ лечения выполняется под местной или регионарной анестезией, он малотравматичный, малоболезненный и сокращает время пребывания в стационаре, а также снижает летальность. Все чаще и чаще в практике сосудистой хирургии при лечении аневризм грудного и брюшного отдела аорты используются малоинвазивные эндоваскулярные технологии, хотя сбрасывать со счетов открытые хирургические вмешательства пока ещё рано [4].
Большие операции при грудных аневризмах относят к одним из самых сложных в медицине. Они выполняются в специализированных кардиохирургических центрах на выключенном сердце при искусственном кровообращении. Технология проведения операции заключается в замене расширенного участка аорты на специальный трубчатый протез, который вшивается на место аневризматического мешка [5][10]. Хирург делает разрез, обеспечивая доступ к аневризме, иссекает поражённую часть и замещает её протезом. Но в некоторых случаях, например после травмы, аорту можно сшить конец в конец без использования протеза.
Аневризмы брюшной аорты с диаметром более 5,5 см у мужчин и 5,2 см у женщин обладают высоким риском разрыва, поэтому требуют немедленной консультации сосудистого хирурга для определения показаний к оперативному лечению. Оно проводится в сосудистых отделениях доступом через переднюю брюшную стенку (лапаротомия) и также имеет своей целью замену поражённого сегмента аорты на протез. В некоторых медицинских центрах освоено лапароскопическое лечение аневризм, не требующее разрезов [4][7].
При оперативном лечении таких тяжелейших заболеваний (как и при других лечебных и диагностических вмешательствах) есть вероятность осложнений. Также стоит отметить, что далеко не во всех областных, краевых и республиканских медицинских центрах есть специалисты, которые работают на открытом сердце.